氮是地球上含量丰富的一种元素,氮及其化合物对我们的生产、生活有重要的影响。请回答下列问题:
I.利用化学原理对氮氧化物进行处理。
(1) 还原法消除氮氧化物,已知:
还原法消除氮氧化物,已知:
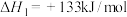 ,
, 的燃烧热
的燃烧热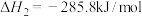 ,在催化剂存在下,
,在催化剂存在下, 还原
还原 生成液态水和氮气的热化学方程式为
生成液态水和氮气的热化学方程式为___________ 。
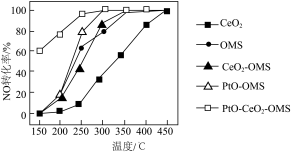
(2)汽车中的三元催化器能使尾气中的NO和CO发生反应转化为无污染的气体,主要反应的化学方程式为 。下图为相同时间内不同温度下汽车尾气中NO的转化率的变化情况。该反应最佳的催化剂与温度为
。下图为相同时间内不同温度下汽车尾气中NO的转化率的变化情况。该反应最佳的催化剂与温度为___________ 、___________ 。
Ⅱ.某些硝酸盐分解,也会产生氮氧化物,已知如下反应:
a.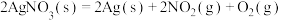
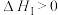
b.
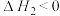
(3) 温度时,在2L的恒容密闭容器中投入0.05mol
温度时,在2L的恒容密闭容器中投入0.05mol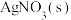 并完全分解,5分钟时反应达到平衡,测得混合气体的总物质的量为0.06mol:
并完全分解,5分钟时反应达到平衡,测得混合气体的总物质的量为0.06mol:
①下列情况能说明体系达到平衡状态的是___________ (填字母)。
A.混合气体的平均相对分子质量不再改变 B. 的质量不再改变
的质量不再改变
C.混合气体的密度不再改变 D. 的浓度不再改变
的浓度不再改变
②若达到平衡时,混合气体的总压强 ,反应开始到5min内
,反应开始到5min内 的平均反应速率为
的平均反应速率为___________  。在该温度下
。在该温度下 的平衡常数
的平衡常数
___________  (结果保留3位有效数字)。[提示:用平衡时各组分分压替代浓度计算的平衡常数叫压强平衡常数
(结果保留3位有效数字)。[提示:用平衡时各组分分压替代浓度计算的平衡常数叫压强平衡常数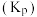 ,组分的分压
,组分的分压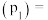 平衡时总压
平衡时总压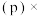 该组分的体积分数
该组分的体积分数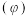 ]。
]。
③实验测得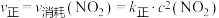 ,
,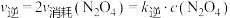 ,
, 、
、 为速率常数且只受温度影响。则化学平衡常数K与速率常数
为速率常数且只受温度影响。则化学平衡常数K与速率常数 、
、 的数学关系是
的数学关系是
___________ 。若将容器的温度改变为 时,其
时,其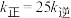 ,则
,则
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
I.利用化学原理对氮氧化物进行处理。
(1)
 还原法消除氮氧化物,已知:
还原法消除氮氧化物,已知:
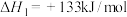 ,
, 的燃烧热
的燃烧热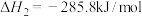 ,在催化剂存在下,
,在催化剂存在下, 还原
还原 生成液态水和氮气的热化学方程式为
生成液态水和氮气的热化学方程式为(2)汽车中的三元催化器能使尾气中的NO和CO发生反应转化为无污染的气体,主要反应的化学方程式为
 。下图为相同时间内不同温度下汽车尾气中NO的转化率的变化情况。该反应最佳的催化剂与温度为
。下图为相同时间内不同温度下汽车尾气中NO的转化率的变化情况。该反应最佳的催化剂与温度为
Ⅱ.某些硝酸盐分解,也会产生氮氧化物,已知如下反应:
a.
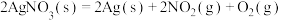
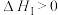
b.

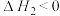
(3)
 温度时,在2L的恒容密闭容器中投入0.05mol
温度时,在2L的恒容密闭容器中投入0.05mol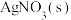 并完全分解,5分钟时反应达到平衡,测得混合气体的总物质的量为0.06mol:
并完全分解,5分钟时反应达到平衡,测得混合气体的总物质的量为0.06mol:①下列情况能说明体系达到平衡状态的是
A.混合气体的平均相对分子质量不再改变 B.
 的质量不再改变
的质量不再改变C.混合气体的密度不再改变 D.
 的浓度不再改变
的浓度不再改变②若达到平衡时,混合气体的总压强
 ,反应开始到5min内
,反应开始到5min内 的平均反应速率为
的平均反应速率为 。在该温度下
。在该温度下 的平衡常数
的平衡常数
 (结果保留3位有效数字)。[提示:用平衡时各组分分压替代浓度计算的平衡常数叫压强平衡常数
(结果保留3位有效数字)。[提示:用平衡时各组分分压替代浓度计算的平衡常数叫压强平衡常数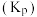 ,组分的分压
,组分的分压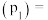 平衡时总压
平衡时总压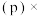 该组分的体积分数
该组分的体积分数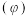 ]。
]。③实验测得
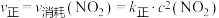 ,
,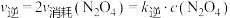 ,
, 、
、 为速率常数且只受温度影响。则化学平衡常数K与速率常数
为速率常数且只受温度影响。则化学平衡常数K与速率常数 、
、 的数学关系是
的数学关系是
 时,其
时,其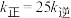 ,则
,则
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
更新时间:2023-11-25 21:57:32
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】全球大气  浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。回答下列问题:
(1)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为: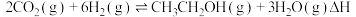
①通过表格中的数值可以推断:该反应在________ (填“高温”、“低温”或“任何温度”)下能自发进行。
② 的平衡转化率与氢碳比
的平衡转化率与氢碳比 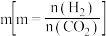 及压强、温度的关系分别如图 a和图 b所示。
及压强、温度的关系分别如图 a和图 b所示。

图a中氢碳比 从大到小的顺序为
从大到小的顺序为___________ 。图b中压强从大到小的顺序为___________ 。
(2)反应
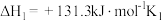
反应
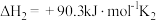
反应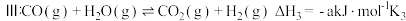
①
___________ ,
___________ (用 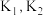 表示)。
表示)。
②研究表明,反应 Ⅲ的速率方程为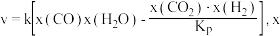 表示反应气体的物质的量分数,
表示反应气体的物质的量分数, 为平衡常数(用平衡分压代替平衡浓度计算),
为平衡常数(用平衡分压代替平衡浓度计算), 为反应的速率常数。当恒压
为反应的速率常数。当恒压 ,只发生反应Ⅲ:COg+H2Og⇌CO2g+H2gΔH3=-akJ⋅mol-1K3且
,只发生反应Ⅲ:COg+H2Og⇌CO2g+H2gΔH3=-akJ⋅mol-1K3且 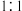 加料时,平衡转化率为 b,求反应物转化率为
加料时,平衡转化率为 b,求反应物转化率为 时的反应速率
时的反应速率
___________ (用含 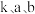 的计算式表示,不用化简)。
的计算式表示,不用化简)。
(3)已知 时,大气中的
时,大气中的  溶于水存在以下过程:
溶于水存在以下过程:
①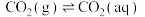
②
溶液中 的浓度
的浓度 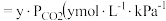 为比例系数,此题可看为常数)。当大气压强为
为比例系数,此题可看为常数)。当大气压强为 ,大气中
,大气中 的物质的量分数为
的物质的量分数为 时,溶液中
时,溶液中 的浓度为
的浓度为_______  (忽略
(忽略 和水的电离)。
和水的电离)。
 浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。回答下列问题:(1)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:
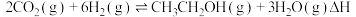
温度/  | 400 | 500 |
平衡常数  | 9 | 5.3 |
②
 的平衡转化率与氢碳比
的平衡转化率与氢碳比 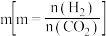 及压强、温度的关系分别如图 a和图 b所示。
及压强、温度的关系分别如图 a和图 b所示。
图a中氢碳比
 从大到小的顺序为
从大到小的顺序为(2)反应

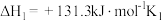
反应

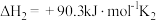
反应
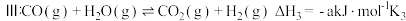
①


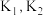 表示)。
表示)。②研究表明,反应 Ⅲ的速率方程为
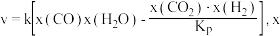 表示反应气体的物质的量分数,
表示反应气体的物质的量分数, 为平衡常数(用平衡分压代替平衡浓度计算),
为平衡常数(用平衡分压代替平衡浓度计算), 为反应的速率常数。当恒压
为反应的速率常数。当恒压 ,只发生反应Ⅲ:COg+H2Og⇌CO2g+H2gΔH3=-akJ⋅mol-1K3且
,只发生反应Ⅲ:COg+H2Og⇌CO2g+H2gΔH3=-akJ⋅mol-1K3且 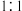 加料时,平衡转化率为 b,求反应物转化率为
加料时,平衡转化率为 b,求反应物转化率为 时的反应速率
时的反应速率
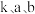 的计算式表示,不用化简)。
的计算式表示,不用化简)。(3)已知
 时,大气中的
时,大气中的  溶于水存在以下过程:
溶于水存在以下过程:①
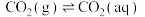
②

溶液中
 的浓度
的浓度 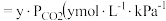 为比例系数,此题可看为常数)。当大气压强为
为比例系数,此题可看为常数)。当大气压强为 ,大气中
,大气中 的物质的量分数为
的物质的量分数为 时,溶液中
时,溶液中 的浓度为
的浓度为 (忽略
(忽略 和水的电离)。
和水的电离)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】氢能是一种极具发展潜力的清洁能源,目前有以下制取氢气的方法:
(1)水煤气变换制氢: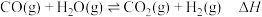
已知: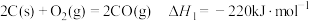
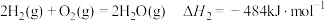
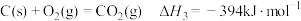
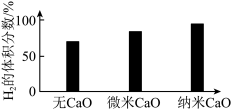
水煤气变换制氢体系中,一定时间内, 的添加情况与
的添加情况与 的体积分数关系如图。
的体积分数关系如图。
①水煤气变换制氢反应的
___________  。
。
②添加 后
后 的体积分数增大的原因是
的体积分数增大的原因是___________ (用化学方程式表达)。
③对比纳米 和微
和微 ,前者
,前者 的体积分数更大的原因是
的体积分数更大的原因是___________ 。
(2)甲醇水蒸气重整制氢: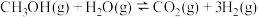 。控制原料气
。控制原料气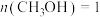 ,体系中甲醇的平衡转化率与温度和压强的关系如图。
,体系中甲醇的平衡转化率与温度和压强的关系如图。
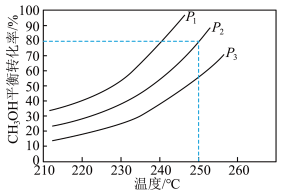
①甲醇水蒸气重整制氢反应在___________ 条件(填“高温”“低温”或“任意温度”)下能自发进行。
②图中的压强由小到大的顺序是___________ ,理由是___________ 。
③温度为250℃、压强为P2时,该反应的压力平衡常数Kp=___________ (列出算式)。
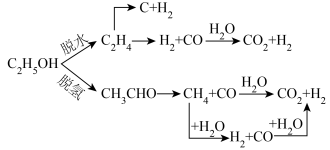
(3)乙醇重整制氢两条途径的机理如下图,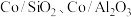 和
和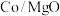 催化剂(酸性
催化剂(酸性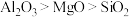 )在反应中表现出良好的催化活性和氢气选择性,但经长期反应后,催化剂表面均发现了积碳,积碳量
)在反应中表现出良好的催化活性和氢气选择性,但经长期反应后,催化剂表面均发现了积碳,积碳量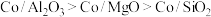 ,试分析
,试分析 表面的积碳量最大的原因
表面的积碳量最大的原因___________ 。
(1)水煤气变换制氢:
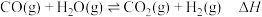
已知:
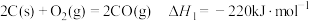
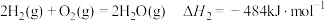
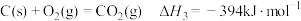
水煤气变换制氢体系中,一定时间内,
 的添加情况与
的添加情况与 的体积分数关系如图。
的体积分数关系如图。
①水煤气变换制氢反应的

 。
。②添加
 后
后 的体积分数增大的原因是
的体积分数增大的原因是③对比纳米
 和微
和微 ,前者
,前者 的体积分数更大的原因是
的体积分数更大的原因是(2)甲醇水蒸气重整制氢:
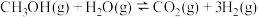 。控制原料气
。控制原料气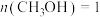 ,体系中甲醇的平衡转化率与温度和压强的关系如图。
,体系中甲醇的平衡转化率与温度和压强的关系如图。
①甲醇水蒸气重整制氢反应在
②图中的压强由小到大的顺序是
③温度为250℃、压强为P2时,该反应的压力平衡常数Kp=
(3)乙醇重整制氢两条途径的机理如下图,
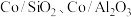 和
和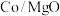 催化剂(酸性
催化剂(酸性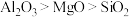 )在反应中表现出良好的催化活性和氢气选择性,但经长期反应后,催化剂表面均发现了积碳,积碳量
)在反应中表现出良好的催化活性和氢气选择性,但经长期反应后,催化剂表面均发现了积碳,积碳量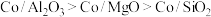 ,试分析
,试分析 表面的积碳量最大的原因
表面的积碳量最大的原因
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】宇宙中所有的一切都是能量的变化,研究化学反应中的能量变化意义重大。
(1)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热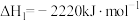 ,正丁烷的燃烧热
,正丁烷的燃烧热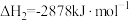 :异丁烷的燃烧热
:异丁烷的燃烧热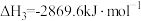 。下列有关说法正确的是
。下列有关说法正确的是_________ (填字母)。
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷的多
C.正丁烷比异丁烷稳定
(2)某实验小组用0.50 NaOH溶液和0.50
NaOH溶液和0.50
 溶液进行中和热的测定。
溶液进行中和热的测定。
①实验中用到的玻璃仪器有大、小烧杯、______________________ 。
②取50mL NaOH溶液和30mL 溶液进行实验,实验数据如表所示。
溶液进行实验,实验数据如表所示。
近似认为0.50 NaOH溶液和0.50
NaOH溶液和0.50
 溶液的密度都是1
溶液的密度都是1 ,中和后混合溶液的比热容
,中和后混合溶液的比热容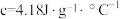 ,则△H≈
,则△H≈___________ (结果保留小数点后一位)。
(3)研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图:
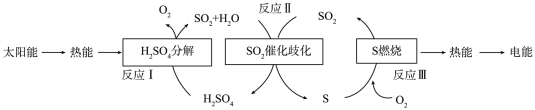
反应Ⅰ: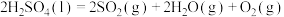

反应Ⅲ:
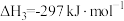
反应Ⅱ的热化学方程式:_____________________ 。
(4)热力学标准态(298K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H)。如图为第ⅥA族元素(包括O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。试完成下列问题。
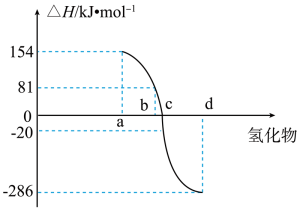
①图中a对应的氢化物是___________ (填化学式),结合元素周期律归纳非金属元素氢化物的稳定性与氢化物的生成热△H的关系:____________________________________________ 。
②硒化氢在上述条件下发生分解反应的热化学方程式为_____________________ 。(沸点:硒化氢-41.3℃;硒:6849℃)
(1)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热
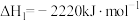 ,正丁烷的燃烧热
,正丁烷的燃烧热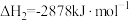 :异丁烷的燃烧热
:异丁烷的燃烧热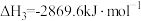 。下列有关说法正确的是
。下列有关说法正确的是A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷的多
C.正丁烷比异丁烷稳定
(2)某实验小组用0.50
 NaOH溶液和0.50
NaOH溶液和0.50
 溶液进行中和热的测定。
溶液进行中和热的测定。①实验中用到的玻璃仪器有大、小烧杯、
②取50mL NaOH溶液和30mL
 溶液进行实验,实验数据如表所示。
溶液进行实验,实验数据如表所示。温度 实验 次数 | 起始温度 | 终止温度 | ||
| NaOH溶液 | 平均值 | ||
1 | 26.2 | 26.0 | 26.4 | 30.4 |
2 | 27.0 | 27.4 | 27.2 | 33.3 |
3 | 25.9 | 25.9 | 25.9 | 29.8 |
4 | 26.4 | 26.2 | 26.3 | 30.4 |
 NaOH溶液和0.50
NaOH溶液和0.50
 溶液的密度都是1
溶液的密度都是1 ,中和后混合溶液的比热容
,中和后混合溶液的比热容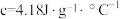 ,则△H≈
,则△H≈(3)研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图:

反应Ⅰ:
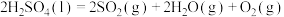

反应Ⅲ:

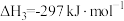
反应Ⅱ的热化学方程式:
(4)热力学标准态(298K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H)。如图为第ⅥA族元素(包括O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。试完成下列问题。

①图中a对应的氢化物是
②硒化氢在上述条件下发生分解反应的热化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】 捕集技术能有效解决温室效应及能源短缺问题。
捕集技术能有效解决温室效应及能源短缺问题。
已知:①
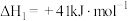
②
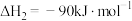
回答下列问题:
I. 催化加氢制
催化加氢制 的总反应:
的总反应:

(1)
_____  ,该反应在
,该反应在_____ (填“高温”或“低温”)下可自发进行。
(2)将 和
和 按物质的量比1:3混合,以固定流速通过盛放催化剂的反应器中,发生反应:
按物质的量比1:3混合,以固定流速通过盛放催化剂的反应器中,发生反应:
 ,在相同时间内,不同温度下的实验数据如图1所示。
,在相同时间内,不同温度下的实验数据如图1所示。 产率
产率 。则该反应的最佳温度为
。则该反应的最佳温度为_____ K,当温度由最佳温度继续升高到 时,
时, 的实验产率降低的原因是
的实验产率降低的原因是_____ 。
Ⅱ. 加氢制
加氢制 的一种催化机理如图2。
的一种催化机理如图2。
Ⅲ.工业上用 和
和 发生反应②合成甲醇。向某容器中充入
发生反应②合成甲醇。向某容器中充入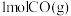 和
和 发生反应②,
发生反应②, 的平衡转化率与温度、压强的关系如图3所示。
的平衡转化率与温度、压强的关系如图3所示。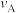
_____ (填“>”“<”或“=”)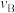 。
。
(5)若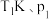 条件下,
条件下, 时反应达到平衡,且
时反应达到平衡,且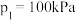 ,则
,则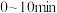 内,
内, 分压的平均变化率为
分压的平均变化率为_____  ,A点对应的
,A点对应的
_____ ( 表示分压平衡常数,分压=总压×物质的量分数)
表示分压平衡常数,分压=总压×物质的量分数)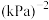 。
。
 捕集技术能有效解决温室效应及能源短缺问题。
捕集技术能有效解决温室效应及能源短缺问题。已知:①

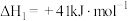
②

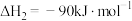
回答下列问题:
I.
 催化加氢制
催化加氢制 的总反应:
的总反应:

(1)

 ,该反应在
,该反应在(2)将
 和
和 按物质的量比1:3混合,以固定流速通过盛放催化剂的反应器中,发生反应:
按物质的量比1:3混合,以固定流速通过盛放催化剂的反应器中,发生反应:
 ,在相同时间内,不同温度下的实验数据如图1所示。
,在相同时间内,不同温度下的实验数据如图1所示。
 产率
产率 。则该反应的最佳温度为
。则该反应的最佳温度为 时,
时, 的实验产率降低的原因是
的实验产率降低的原因是Ⅱ.
 加氢制
加氢制 的一种催化机理如图2。
的一种催化机理如图2。
A.反应过程中的催化剂为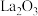 和 和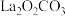 |
B.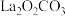 可以释放 可以释放 |
C.在 的作用下 的作用下 断键裂解产生 断键裂解产生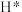 的过程为放热过程 的过程为放热过程 |
D.该机理中, 加氢制 加氢制 的过程需要 的过程需要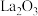 与 与 共同完成 共同完成 |
Ⅲ.工业上用
 和
和 发生反应②合成甲醇。向某容器中充入
发生反应②合成甲醇。向某容器中充入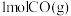 和
和 发生反应②,
发生反应②, 的平衡转化率与温度、压强的关系如图3所示。
的平衡转化率与温度、压强的关系如图3所示。
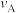
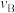 。
。(5)若
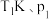 条件下,
条件下, 时反应达到平衡,且
时反应达到平衡,且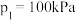 ,则
,则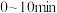 内,
内, 分压的平均变化率为
分压的平均变化率为 ,A点对应的
,A点对应的
 表示分压平衡常数,分压=总压×物质的量分数)
表示分压平衡常数,分压=总压×物质的量分数)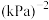 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】和硅同一主族的锗也是重要的半导体材料,锗应用于航空航天测控、光纤通讯等领域。一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如下:

已知:①“碱浸”过程中的反应为:GeO2+2NaOH=Na2GeO3+H2O、As2O3+2NaOH=2NaAsO2+H2O
② GeCl4的熔点为-49.5℃,AsCl3与GeCl4的沸点分别为130.2℃、84℃。
(1)砷的原子序数为33,砷在元素周期表中的位置为第______ 周期第________ 族。
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应的离子方程式为:___________________________________________________________________ 。
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是_________________ 。
(4)“蒸馏”过程中的反应的化学方程式为:________________________________ 。
(5)“水解”操作时保持较低温度有利于提高产率,其最可能的原因是_____________ (答一条即可)。
(6)若1吨二氧化锗粗品(含杂质30%)经提纯得0.745吨的较纯二氧化锗产品,则杂质脱除率为_________ 。
(7)和砷同一主族的锑也可以用于半导体中。一种突破传统电池设计理念的镁—锑液态金属二次电池工作原理如图所示:

该电池由于密度的不同,在重力作用下分为三层,工作时中间层熔融盐的组成不变。充电时,C1-向______ (填“上”或“下”)移动;放电时,正极的电极反应式为______ 。

已知:①“碱浸”过程中的反应为:GeO2+2NaOH=Na2GeO3+H2O、As2O3+2NaOH=2NaAsO2+H2O
② GeCl4的熔点为-49.5℃,AsCl3与GeCl4的沸点分别为130.2℃、84℃。
(1)砷的原子序数为33,砷在元素周期表中的位置为第
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应的离子方程式为:
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是
(4)“蒸馏”过程中的反应的化学方程式为:
(5)“水解”操作时保持较低温度有利于提高产率,其最可能的原因是
(6)若1吨二氧化锗粗品(含杂质30%)经提纯得0.745吨的较纯二氧化锗产品,则杂质脱除率为
(7)和砷同一主族的锑也可以用于半导体中。一种突破传统电池设计理念的镁—锑液态金属二次电池工作原理如图所示:

该电池由于密度的不同,在重力作用下分为三层,工作时中间层熔融盐的组成不变。充电时,C1-向
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】某小组以含镍废料(主要含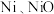 ,以及少量
,以及少量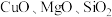 )为原料提取镍的流程如图所示:
)为原料提取镍的流程如图所示:
(1)固体2的主要成分为__________ (填化学式)。
(2)在“除镁”阶段,若溶液的 太小,会显著增加
太小,会显著增加 的用量,其原因为
的用量,其原因为____________________ (结合勒夏特列原理解释)。
(3) 可用于镍氢电池的正极材料。某镍氢电池的总反应为
可用于镍氢电池的正极材料。某镍氢电池的总反应为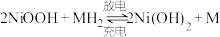 ,该电池充电时,阳极的电极反应式为
,该电池充电时,阳极的电极反应式为__________ 。
(4)可利用三室双膜法进行“电沉积”制镍,其原理如下:__________ 。
②可以通过电解法提纯粗镍,粗镍作______ (填“阳”或“阴”)极,阴极的电极反应式为_______________ 。
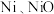 ,以及少量
,以及少量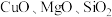 )为原料提取镍的流程如图所示:
)为原料提取镍的流程如图所示:
(1)固体2的主要成分为
(2)在“除镁”阶段,若溶液的
 太小,会显著增加
太小,会显著增加 的用量,其原因为
的用量,其原因为(3)
 可用于镍氢电池的正极材料。某镍氢电池的总反应为
可用于镍氢电池的正极材料。某镍氢电池的总反应为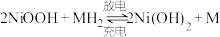 ,该电池充电时,阳极的电极反应式为
,该电池充电时,阳极的电极反应式为(4)可利用三室双膜法进行“电沉积”制镍,其原理如下:

②可以通过电解法提纯粗镍,粗镍作
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】SO2是空气污染物 ,含有SO2的尾气需处理后才能排放,有多种方法可除 去尾气中SO2。回答下列问题:
(1)氨水吸收法。利用氨水吸收烟气中的SO2, 其相关反应的主要热化学方程式如下:
SO2(g)+NH 3 • H2O(aq)=NH4HSO3(aq) △H1=akJ•mol-1;
NH 3 • H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(1)△H2= b kJ• mol-1;
2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq)△H3 =ckJ• mol-1;
则反应 2SO2(g)+4 NH 3 • H2O(aq)+ O2(g)=2(NH4)2SO4(aq)+2H2O(l)的△H=___________ kJ• mol-1(用含a、b、c的代数式表示)。
(2)热解气还原法。已知CO与SO2在加热和催化剂作用 下生成生成S(g)和CO2。
①该反应的化学方程式为__________ 。
②在T °C时,向lL恒容的密闭容器中入充1 mol CO、0.5molSO2发生上述反应(S为气态).5min时达到化学平衡,平衡时测得SO2的转化率为90 %,则 0 ~ 5 mi n 内 反应的平均速率v(SO2)=__________ 。此温度下该反应的平衡常数 K1=_______ 。下列选项中能够说明该反应已经达到平衡状态的是_____ (填字母)。
a.体系的压强保持不变
b.混合气体的密度保持不变
c.混合气体的平均摩尔质量保持不变
d.单位时间内CO消耗的物质的量与 SO2生成的物质的量之比为2:1
(3)氧化锌吸收法。配制ZnO悬浊液(含少量 MgO、CaO)在吸收塔中封闭循环脱硫。发生的主要反应为ZnO十SO2 = ZnSO3(s).吸收过程中,测得pH、吸收效率η随 时间t的变化如图a所示。溶液中含硫元素微粒各组分浓度之比如图b所示。

①已知纯ZnO的悬浮液 pH 约为6.8,判断在pH-t曲线cd 段发生的主要反应的离子方程式为____________ 。
②SO2的吸收效率η随 pH 降低而减小的原因是____________ 。
(1)氨水吸收法。利用氨水吸收烟气中的SO2, 其相关反应的主要热化学方程式如下:
SO2(g)+NH 3 • H2O(aq)=NH4HSO3(aq) △H1=akJ•mol-1;
NH 3 • H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(1)△H2= b kJ• mol-1;
2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq)△H3 =ckJ• mol-1;
则反应 2SO2(g)+4 NH 3 • H2O(aq)+ O2(g)=2(NH4)2SO4(aq)+2H2O(l)的△H=
(2)热解气还原法。已知CO与SO2在加热和催化剂作用 下生成生成S(g)和CO2。
①该反应的化学方程式为
②在T °C时,向lL恒容的密闭容器中入充1 mol CO、0.5molSO2发生上述反应(S为气态).5min时达到化学平衡,平衡时测得SO2的转化率为90 %,则 0 ~ 5 mi n 内 反应的平均速率v(SO2)=
a.体系的压强保持不变
b.混合气体的密度保持不变
c.混合气体的平均摩尔质量保持不变
d.单位时间内CO消耗的物质的量与 SO2生成的物质的量之比为2:1
(3)氧化锌吸收法。配制ZnO悬浊液(含少量 MgO、CaO)在吸收塔中封闭循环脱硫。发生的主要反应为ZnO十SO2 = ZnSO3(s).吸收过程中,测得pH、吸收效率η随 时间t的变化如图a所示。溶液中含硫元素微粒各组分浓度之比如图b所示。

①已知纯ZnO的悬浮液 pH 约为6.8,判断在pH-t曲线cd 段发生的主要反应的离子方程式为
②SO2的吸收效率η随 pH 降低而减小的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】 过度排放会引起气候、环境等问题。一定条件下可利用化学反应将其转化为燃料
过度排放会引起气候、环境等问题。一定条件下可利用化学反应将其转化为燃料 。以
。以 和
和 为原料合成
为原料合成 的主要反应如下:
的主要反应如下:
Ⅰ.
 ;
;
Ⅱ.
 ;
;
Ⅲ.

回答下列问题:
(1)
______  。
。
(2)在恒温条件下向恒容的密闭容器中通入 和
和 发生上述反应,若只考虑反应
发生上述反应,若只考虑反应 ,下列
,下列不能 说明反应达到平衡状态的是______ 。
A.
B.容器内的压强不再变化
C.容器内混合气体的密度不再变化
D.混合气体的平均摩尔质量不再变化
E.相同时间内 断裂与
断裂与 断裂比值为1:1
断裂比值为1:1
(3)将 和
和 按1:3通入体积为
按1:3通入体积为 的密闭容器中,假设只发生反应Ⅰ和反应Ⅱ,改变反应温度,分别测得
的密闭容器中,假设只发生反应Ⅰ和反应Ⅱ,改变反应温度,分别测得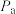 、
、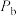 、
、 (单位
(单位 下
下 的平衡转化率(
的平衡转化率( )以及
)以及 时生成
时生成 、
、 选择性(
选择性( )的变化如图甲(选择性为目标产物在总产物中的比率,即
)的变化如图甲(选择性为目标产物在总产物中的比率,即 ;
; )。
)。


①图甲中 、
、 和
和 分别代表代表
分别代表代表 、
、 、
、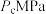 下
下 随温度变化趋势的是曲线,则
随温度变化趋势的是曲线,则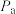 、
、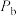 、
、 的从大到小的关系为
的从大到小的关系为______ 。
②随着温度升高, 、
、 和
和 条曲线接近重合的原因是
条曲线接近重合的原因是______ 。
③ 点对应的反应Ⅱ的平衡常数
点对应的反应Ⅱ的平衡常数
______ 。
④分子筛膜反应器可提高反应Ⅱ的平衡转化率,原理如图乙所示。同温同压下,将等物质的量的 和
和 通入无分子筛反应器,测得
通入无分子筛反应器,测得 的平衡转化率为
的平衡转化率为 ;若换成分子筛膜反应器,
;若换成分子筛膜反应器, 的平衡转化率为
的平衡转化率为 ,则相同时间内,上出口和下出口中
,则相同时间内,上出口和下出口中 的物质的量之比为
的物质的量之比为______ 。
(4)为同时提高 的平衡转化率和
的平衡转化率和 的平衡产率,应选择的反应条件为______。
的平衡产率,应选择的反应条件为______。
 过度排放会引起气候、环境等问题。一定条件下可利用化学反应将其转化为燃料
过度排放会引起气候、环境等问题。一定条件下可利用化学反应将其转化为燃料 。以
。以 和
和 为原料合成
为原料合成 的主要反应如下:
的主要反应如下:Ⅰ.

 ;
;Ⅱ.

 ;
;Ⅲ.


回答下列问题:
(1)

 。
。(2)在恒温条件下向恒容的密闭容器中通入
 和
和 发生上述反应,若只考虑反应
发生上述反应,若只考虑反应 ,下列
,下列A.

B.容器内的压强不再变化
C.容器内混合气体的密度不再变化
D.混合气体的平均摩尔质量不再变化
E.相同时间内
 断裂与
断裂与 断裂比值为1:1
断裂比值为1:1(3)将
 和
和 按1:3通入体积为
按1:3通入体积为 的密闭容器中,假设只发生反应Ⅰ和反应Ⅱ,改变反应温度,分别测得
的密闭容器中,假设只发生反应Ⅰ和反应Ⅱ,改变反应温度,分别测得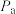 、
、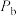 、
、 (单位
(单位 下
下 的平衡转化率(
的平衡转化率( )以及
)以及 时生成
时生成 、
、 选择性(
选择性( )的变化如图甲(选择性为目标产物在总产物中的比率,即
)的变化如图甲(选择性为目标产物在总产物中的比率,即 ;
; )。
)。

①图甲中
 、
、 和
和 分别代表代表
分别代表代表 、
、 、
、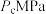 下
下 随温度变化趋势的是曲线,则
随温度变化趋势的是曲线,则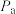 、
、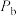 、
、 的从大到小的关系为
的从大到小的关系为②随着温度升高,
 、
、 和
和 条曲线接近重合的原因是
条曲线接近重合的原因是③
 点对应的反应Ⅱ的平衡常数
点对应的反应Ⅱ的平衡常数
④分子筛膜反应器可提高反应Ⅱ的平衡转化率,原理如图乙所示。同温同压下,将等物质的量的
 和
和 通入无分子筛反应器,测得
通入无分子筛反应器,测得 的平衡转化率为
的平衡转化率为 ;若换成分子筛膜反应器,
;若换成分子筛膜反应器, 的平衡转化率为
的平衡转化率为 ,则相同时间内,上出口和下出口中
,则相同时间内,上出口和下出口中 的物质的量之比为
的物质的量之比为(4)为同时提高
 的平衡转化率和
的平衡转化率和 的平衡产率,应选择的反应条件为______。
的平衡产率,应选择的反应条件为______。| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】硫及其化合物对人类的生产生活有着重要的作用,回答下列问题:
(1)一定温度下,将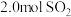 和
和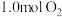 置于刚性容器中,发生反应
置于刚性容器中,发生反应

 。
。
①不能判断该反应达到平衡状态的标志是__________ (填标号)。
A.混合气体中 的浓度等于
的浓度等于 的浓度
的浓度
B.混合气体的平均相对分子质量保持不变
C. 的生成速率和
的生成速率和 的生成速率相等
的生成速率相等
D. 等于2:1:2
等于2:1:2
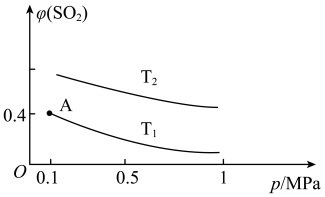
②平衡时 的体积分数随压强和温度变化的曲线如图所示。则温度关系:
的体积分数随压强和温度变化的曲线如图所示。则温度关系:
__________  (填“>”“<”或“=”),A点的化学平衡常数是
(填“>”“<”或“=”),A点的化学平衡常数是
__________  (
( 是以平衡分压代替平衡浓度的平衡常数,分压=总压
是以平衡分压代替平衡浓度的平衡常数,分压=总压 物质的量分数)。
物质的量分数)。
(2)一定温度下将 放入抽空的刚性容器中发生吸热反应:
放入抽空的刚性容器中发生吸热反应:
 。达到平衡后,压缩容器体积,一段时间后达到新平衡,与原平衡相对比,
。达到平衡后,压缩容器体积,一段时间后达到新平衡,与原平衡相对比,
__________ (填“增大”、“减小”或“不变”)。
若相同条件下,上述容器中发生副反应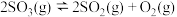 ,达到新平衡时,
,达到新平衡时, 的体积分数为
的体积分数为 ,则此时
,则此时 发生分解反应的平衡常数
发生分解反应的平衡常数
__________ (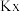 为以物质的量分数表示的平衡常数,计算结果保留两位有效数字,下同)。
为以物质的量分数表示的平衡常数,计算结果保留两位有效数字,下同)。
(3)亚硫酸 在水溶液中存在多种微粒形态。
在水溶液中存在多种微粒形态。 时,向
时,向 亚硫酸溶液中加入
亚硫酸溶液中加入 固体,含硫微粒(
固体,含硫微粒( 、
、 、
、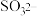 )的lgc和
)的lgc和 的关系如图所示。则曲线①代表的微粒是
的关系如图所示。则曲线①代表的微粒是__________ (填化学式),当 时,溶液中三种含硫微粒浓度大小顺序为
时,溶液中三种含硫微粒浓度大小顺序为__________ ,溶液中c点溶液的 值为
值为__________ 。

(1)一定温度下,将
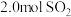 和
和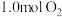 置于刚性容器中,发生反应
置于刚性容器中,发生反应

 。
。①不能判断该反应达到平衡状态的标志是
A.混合气体中
 的浓度等于
的浓度等于 的浓度
的浓度B.混合气体的平均相对分子质量保持不变
C.
 的生成速率和
的生成速率和 的生成速率相等
的生成速率相等D.
 等于2:1:2
等于2:1:2②平衡时
 的体积分数随压强和温度变化的曲线如图所示。则温度关系:
的体积分数随压强和温度变化的曲线如图所示。则温度关系:
 (填“>”“<”或“=”),A点的化学平衡常数是
(填“>”“<”或“=”),A点的化学平衡常数是
 (
( 是以平衡分压代替平衡浓度的平衡常数,分压=总压
是以平衡分压代替平衡浓度的平衡常数,分压=总压 物质的量分数)。
物质的量分数)。
(2)一定温度下将
 放入抽空的刚性容器中发生吸热反应:
放入抽空的刚性容器中发生吸热反应:
 。达到平衡后,压缩容器体积,一段时间后达到新平衡,与原平衡相对比,
。达到平衡后,压缩容器体积,一段时间后达到新平衡,与原平衡相对比,
若相同条件下,上述容器中发生副反应
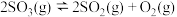 ,达到新平衡时,
,达到新平衡时, 的体积分数为
的体积分数为 ,则此时
,则此时 发生分解反应的平衡常数
发生分解反应的平衡常数
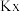 为以物质的量分数表示的平衡常数,计算结果保留两位有效数字,下同)。
为以物质的量分数表示的平衡常数,计算结果保留两位有效数字,下同)。(3)亚硫酸
 在水溶液中存在多种微粒形态。
在水溶液中存在多种微粒形态。 时,向
时,向 亚硫酸溶液中加入
亚硫酸溶液中加入 固体,含硫微粒(
固体,含硫微粒( 、
、 、
、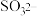 )的lgc和
)的lgc和 的关系如图所示。则曲线①代表的微粒是
的关系如图所示。则曲线①代表的微粒是 时,溶液中三种含硫微粒浓度大小顺序为
时,溶液中三种含硫微粒浓度大小顺序为 值为
值为
您最近一年使用:0次

 /℃
/℃ /℃
/℃

