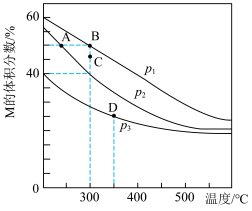
在密闭容器中充入1molX和1molY,发生反应: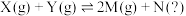 ,测得平衡混合物中M的体积分数在不同压强下随温度的变化情况如图所示。下列说法错误的是
,测得平衡混合物中M的体积分数在不同压强下随温度的变化情况如图所示。下列说法错误的是
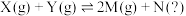 ,测得平衡混合物中M的体积分数在不同压强下随温度的变化情况如图所示。下列说法错误的是
,测得平衡混合物中M的体积分数在不同压强下随温度的变化情况如图所示。下列说法错误的是
| A.在该反应条件下N为气体 |
B.A、B、D三点平衡常数,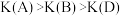 |
C.温度为300℃、压强为 条件下,X的平衡转化率为50% 条件下,X的平衡转化率为50% |
D.温度为300℃、压强为 条件下,C点v(正)>v(逆) 条件下,C点v(正)>v(逆) |
更新时间:2023-10-04 07:21:50
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】选择性催化还原法脱硝技术是目前国际上应用最为广泛的烟气脱硝技术,其反应如下:
主反应: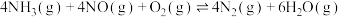
 ;
;
副反应:
 。
。
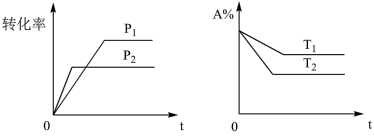
恒容密闭的容器中,分别在甲、乙催化剂作用下进行上述反应,10min时测得体系温度与NO转化率的关系如图所示。下列说法正确的是
主反应:
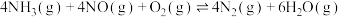
 ;
;副反应:

 。
。恒容密闭的容器中,分别在甲、乙催化剂作用下进行上述反应,10min时测得体系温度与NO转化率的关系如图所示。下列说法正确的是

A.若初始 ,则P点时NO的反应速率为 ,则P点时NO的反应速率为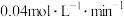 |
| B.图中M点对应的转化率是NO在该温度下的平衡转化率 |
| C.温度高于200℃时,温度升高,平衡逆向移动导致甲、乙作用下NO的转化率降低 |
| D.工业上选择催化剂乙的原因是其在较低温度下有很强的催化活性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】 还原
还原 制
制 的反应体系中,主要发生反应的热化学方程式为
的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ

反应Ⅱ

在恒容密闭容器中,起始投入一定物质的量的 和
和 发生反应,平衡时
发生反应,平衡时 的转化率、产物
的转化率、产物 或CO其中之一的选择性[
或CO其中之一的选择性[ ]随温度变化如下图所示。下列说法正确的是
]随温度变化如下图所示。下列说法正确的是

 还原
还原 制
制 的反应体系中,主要发生反应的热化学方程式为
的反应体系中,主要发生反应的热化学方程式为反应Ⅰ


反应Ⅱ


在恒容密闭容器中,起始投入一定物质的量的
 和
和 发生反应,平衡时
发生反应,平衡时 的转化率、产物
的转化率、产物 或CO其中之一的选择性[
或CO其中之一的选择性[ ]随温度变化如下图所示。下列说法正确的是
]随温度变化如下图所示。下列说法正确的是
| A.图中曲线a表示CO的选择性 |
B.200~600℃时,温度越高,平衡时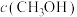 的浓度越小 的浓度越小 |
C.研究和使用在低温区高效的催化剂可提高制取 的产率 的产率 |
| D.高于600℃,反应Ⅱ的速率加快,反应Ⅰ的速率减慢 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v1=k1c2(M),反应②的速率可表示为v2=k2c2(M)(k1、k2为速率常数)。反应体系中组分M、Z的浓度(mol。L-1)随时间(分)变化情况如图,下列说法正确的是
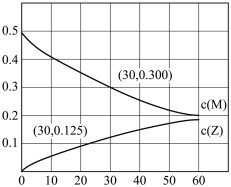
| A.0~30min时间段内,Y的平均反应速率为6.67×10-3mol·L-1·min-1 |
B.反应过程中体系Y和Z的浓度之比保持不变,30min时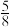 的M转化为Z 的M转化为Z |
| C.反应②的活化能比反应①的活化能大 |
| D.若该平行反应为可逆反应,正反应都为放热,升高温度,可提高Y的产率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】I2在水中溶解度很小,在KI溶液中溶解度显著增大,其原因是I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3-(aq)。某I2、KI混合溶液中,I3-的浓度c(I3-)与温度(T)的关系如图所示(曲线上的任一点都表示平衡状态)。下列说法正确的是
I3-(aq)。某I2、KI混合溶液中,I3-的浓度c(I3-)与温度(T)的关系如图所示(曲线上的任一点都表示平衡状态)。下列说法正确的是

 I3-(aq)。某I2、KI混合溶液中,I3-的浓度c(I3-)与温度(T)的关系如图所示(曲线上的任一点都表示平衡状态)。下列说法正确的是
I3-(aq)。某I2、KI混合溶液中,I3-的浓度c(I3-)与温度(T)的关系如图所示(曲线上的任一点都表示平衡状态)。下列说法正确的是
A.反应I2(aq)+I-(aq) I3-(aq) 的ΔH>0 I3-(aq) 的ΔH>0 |
| B.在上述平衡体系中加入CCl4,平衡不移动 |
| C.保持T1不变,若反应进行到d点时,一定有v正>v逆 |
| D.T2 ℃时,在上述平衡体系中加入少量KI固体后,平衡常数K增加 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】一定温度下,向三个容积不等的恒容密闭容器中分别投入2 mol NOCl,发生反应:2NOCl(g) 2NO(g)+Cl2(g)。t min后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
2NO(g)+Cl2(g)。t min后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是

 2NO(g)+Cl2(g)。t min后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
2NO(g)+Cl2(g)。t min后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
| A.A点延长反应时间,可以提高NOCl的转化率 |
| B.A、B两点的压强之比为25︰28 |
C.t min时,C点 正< 正< 逆 逆 |
| D.容积为a L的容器达到平衡后再投入1 mol NOCl、1 mol NO,平衡不移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】已知某化学反应的平衡常数表达式为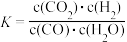 ,在不同的温度下该反应的平衡常数如表所示:
,在不同的温度下该反应的平衡常数如表所示:
下列有关叙述不正确的是
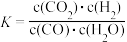 ,在不同的温度下该反应的平衡常数如表所示:
,在不同的温度下该反应的平衡常数如表所示:| t/°C | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
A.该反应的化学方程式是CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g) |
| B.上述反应的正反应是放热反应 |
C.若平衡浓度符合下列关系式: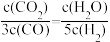 ,则此时的温度为1 000 °C ,则此时的温度为1 000 °C |
| D.在1L的密闭容器中通入CO2和H2各1mol,5 min后温度升高到830°C,此时测得CO为0.4 mol,则该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在密闭容器中的一定量混合气体发生反应xM (g)+yN(g) zP(g)。平衡时测得M的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0. 30 mol/L。下列有关判断正确的是
zP(g)。平衡时测得M的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0. 30 mol/L。下列有关判断正确的是
 zP(g)。平衡时测得M的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0. 30 mol/L。下列有关判断正确的是
zP(g)。平衡时测得M的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0. 30 mol/L。下列有关判断正确的是| A.x+y<z | B.平衡向正反应方向移动 |
| C.N的转化率降低 | D.混合气体的密度不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知:CO(g)+H2O(g) CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:
CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:
下列说法中,不正确的是( )
 CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:
CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系 能量的变化 | |||
n(CO) | n(H2O) | n(CO2) | n(H2) | ||
① | 1 | 4 | 0 | 0 | 放出热量:32.8 kJ |
② | 0 | 0 | 1 | 4 | 热量变化:Q1 |
③ | 1 | 1 | 2 | 1 | 热量变化:Q2 |
| A.若容器①中反应10min达到平衡,0至10min时间内,用CO表示的平均反应速率v(CO)= 4.0×10﹣2 mol/(L·min) |
| B.容器③中,开始时v(CO)生成>v(CO)消耗 |
| C.达平衡过程体系能量的变化:Q1= 4Q2 |
| D.平衡时,①与②容器中CO的体积分数相等 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】可逆反应①X(g)+2Y(g) ⇌ 2Z(g); ②2M(g) ⇌ N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可运动的密封圆板。反应开始和达到平衡状态时有关物理量的变化如图所示:

下列判断正确的是

下列判断正确的是
| A.反应①的正反应是吸热反应 |
| B.达平衡(I)时,X的转化率约为45% |
| C.在平衡(I)和平衡(Ⅱ)中,M的体积分数相等 |
| D.达平衡(I)时体系的压强与反应开始时体系的压强之比为11∶10 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】T℃时,含等浓度 与
与 的溶液中发生反应:
的溶液中发生反应: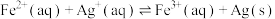
 ,
,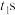 时刻,改变某一外界条件继续反应至
时刻,改变某一外界条件继续反应至 时刻,溶液中
时刻,溶液中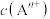 (
( 、
、 )随时间的变化关系如图所示(已知:T℃时,该反应的化学平衡常数
)随时间的变化关系如图所示(已知:T℃时,该反应的化学平衡常数 ,忽略水解)。下列说法正确的是
,忽略水解)。下列说法正确的是
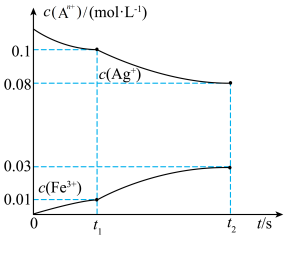
 与
与 的溶液中发生反应:
的溶液中发生反应: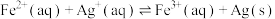
 ,
,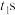 时刻,改变某一外界条件继续反应至
时刻,改变某一外界条件继续反应至 时刻,溶液中
时刻,溶液中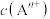 (
( 、
、 )随时间的变化关系如图所示(已知:T℃时,该反应的化学平衡常数
)随时间的变化关系如图所示(已知:T℃时,该反应的化学平衡常数 ,忽略水解)。下列说法正确的是
,忽略水解)。下列说法正确的是
A.若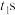 时未改变外界条件,则此时该反应未达到平衡状态 时未改变外界条件,则此时该反应未达到平衡状态 |
B.若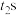 时反应达到平衡,则 时反应达到平衡,则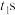 时改变的条件可能为升温 时改变的条件可能为升温 |
C.若始终保持温度不变,则逆反应速率: |
D. 内 内 的平均反应速率为 的平均反应速率为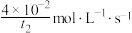 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
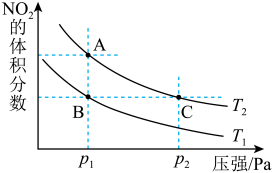
【推荐2】反应N2O4(g)  2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法不正确 的是
 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法
| A.A点的反应速率小于C点的反应速率 |
| B.A、C两点气体的颜色:A浅,C深 |
| C.由状态B到状态A,可以用降温的方法 |
| D.A、C两点气体的平均相对分子质量:A<C |
您最近一年使用:0次