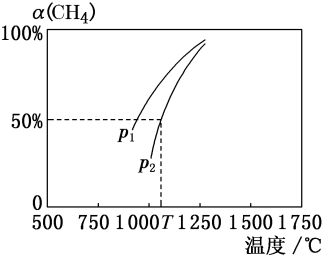
,工业合成
,工业合成 的K=0.5,回答问题。
的K=0.5,回答问题。(1)恒温恒容下,能说明该反应达到化学平衡状态的是______(填字母)。
| A.容器内的密度保持不变 | B.容器内压强保持不变 |
C.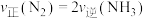 | D.混合气体的平均摩尔质量保持不变 |
(2)该温度下,容器为0.5L的密闭容器中模拟合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应
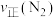
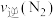 (填“>”、“<”、“=”或“不能确定”)。
(填“>”、“<”、“=”或“不能确定”)。(3)下列有关合成氨反应的图像一定正确的是(选填序号)______。
A. | B. |
C.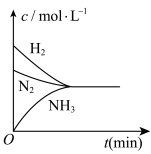 | D. |
更新时间:2023-10-31 15:29:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)某温度下在容积为2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
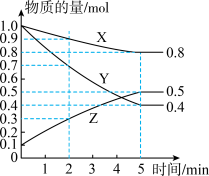
①该反应的化学方程式是___________ 。
②4min时,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③下列措施能增大该反应速率的是___________ (选填字母)
A.升高温度 B.恒容条件下充入Ar气
C.减小Z的浓度 D.将反应容器体积缩小
(2)反应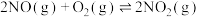 ,在一定温度下2L密闭容器内,能说明该反应已经达到化学平衡状态的是
,在一定温度下2L密闭容器内,能说明该反应已经达到化学平衡状态的是___________ 。
a.
b.容器内压强保持不变
c.
d.容器内的密度保持不变
e.容器内混合气体平均相对分子质量不变
f.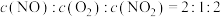
g.容器内气体颜色不变
(3)常见的烟道气中除去 的方法之一:
的方法之一: ,该反应的平衡常数表达式为
,该反应的平衡常数表达式为___________ 。若在2L的密闭容器中进行上述反应,经测定在5min内气体的质量减少了1.6g,则0~5min的平均反应速率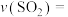
___________ 。
(1)某温度下在容积为2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②4min时,

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③下列措施能增大该反应速率的是
A.升高温度 B.恒容条件下充入Ar气
C.减小Z的浓度 D.将反应容器体积缩小
(2)反应
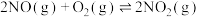 ,在一定温度下2L密闭容器内,能说明该反应已经达到化学平衡状态的是
,在一定温度下2L密闭容器内,能说明该反应已经达到化学平衡状态的是a.

b.容器内压强保持不变
c.

d.容器内的密度保持不变
e.容器内混合气体平均相对分子质量不变
f.
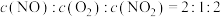
g.容器内气体颜色不变
(3)常见的烟道气中除去
 的方法之一:
的方法之一: ,该反应的平衡常数表达式为
,该反应的平衡常数表达式为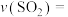
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮及其化合物在工农业生产、生活中有着重要作用,以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2L的密闭容器中加入0.2mol的 和0.6mol的
和0.6mol的 在一定条件下发生反应:
在一定条件下发生反应:
 ,若在5min时反应达到平衡,此时测得
,若在5min时反应达到平衡,此时测得 的物质的量为0.2mol,则前5min平均反应速率
的物质的量为0.2mol,则前5min平均反应速率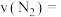
________ 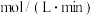 ,平衡时
,平衡时 的转化率为
的转化率为________ %。
(2)平衡后,若提高 的转化率,可以采取的措施有________(填字母序号)。
的转化率,可以采取的措施有________(填字母序号)。
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:
 ,其化学平衡常数K与温度T的关系如表所示:
,其化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较 、
、 的大小,
的大小,
________  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
②400℃时,反应 的化学平衡常数为
的化学平衡常数为________ 。当测得 、
、 和
和 物质的量分别为3mol、2mol和1mol时,则该反应的
物质的量分别为3mol、2mol和1mol时,则该反应的
________  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
③下列可用于判断 反应达到平衡状态的依据是
反应达到平衡状态的依据是________ (填字母序号)。
A.容器中气体压强不再变化 B.容器中气体的密度不再变化
C.容器中气体平均摩尔质量不再变化 D.
(1)若在一容积为2L的密闭容器中加入0.2mol的
 和0.6mol的
和0.6mol的 在一定条件下发生反应:
在一定条件下发生反应:
 ,若在5min时反应达到平衡,此时测得
,若在5min时反应达到平衡,此时测得 的物质的量为0.2mol,则前5min平均反应速率
的物质的量为0.2mol,则前5min平均反应速率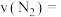
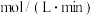 ,平衡时
,平衡时 的转化率为
的转化率为(2)平衡后,若提高
 的转化率,可以采取的措施有________(填字母序号)。
的转化率,可以采取的措施有________(填字母序号)。| A.加入催化剂 | B.增大容器体积 |
| C.降低反应体系的温度 | D.通入一定量He |

 ,其化学平衡常数K与温度T的关系如表所示:
,其化学平衡常数K与温度T的关系如表所示:T/℃ | 200 | 300 | 400 |
K |
|
| 0.5 |
①试比较
 、
、 的大小,
的大小,
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。②400℃时,反应
 的化学平衡常数为
的化学平衡常数为 、
、 和
和 物质的量分别为3mol、2mol和1mol时,则该反应的
物质的量分别为3mol、2mol和1mol时,则该反应的
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。③下列可用于判断
 反应达到平衡状态的依据是
反应达到平衡状态的依据是A.容器中气体压强不再变化 B.容器中气体的密度不再变化
C.容器中气体平均摩尔质量不再变化 D.

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】CrO 和Cr2O
和Cr2O 在溶液中可相互转化。室温下,初始浓度为1.0mol/L的K2CrO4溶液中,c(Cr2O
在溶液中可相互转化。室温下,初始浓度为1.0mol/L的K2CrO4溶液中,c(Cr2O )随c(H+)的变化如图所示。
)随c(H+)的变化如图所示。
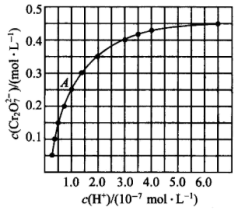
(1)向黄色的K2CrO4溶液中滴加稀硫酸,溶液变为橙色,用离子方程式表示该转化反应:_____ 。
(2)下列可判断转化反应达到平衡的是_____ (填标号)。
a.溶液的pH不再变化 b.v(H+)=2v(Cr2O )
)
c.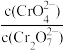 不再变化 d.c(CrO
不再变化 d.c(CrO )=0.45mol/L
)=0.45mol/L
(3)由图可知,溶液酸性增强,CrO 的平衡转化率
的平衡转化率_____ (填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为_____ 。
(4)升高温度,溶液中CrO 的平衡转化率减小,则该反应的△H
的平衡转化率减小,则该反应的△H____ 0(填“>”“<”或“=”)。
 和Cr2O
和Cr2O 在溶液中可相互转化。室温下,初始浓度为1.0mol/L的K2CrO4溶液中,c(Cr2O
在溶液中可相互转化。室温下,初始浓度为1.0mol/L的K2CrO4溶液中,c(Cr2O )随c(H+)的变化如图所示。
)随c(H+)的变化如图所示。
(1)向黄色的K2CrO4溶液中滴加稀硫酸,溶液变为橙色,用离子方程式表示该转化反应:
(2)下列可判断转化反应达到平衡的是
a.溶液的pH不再变化 b.v(H+)=2v(Cr2O
 )
)c.
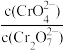 不再变化 d.c(CrO
不再变化 d.c(CrO )=0.45mol/L
)=0.45mol/L(3)由图可知,溶液酸性增强,CrO
 的平衡转化率
的平衡转化率(4)升高温度,溶液中CrO
 的平衡转化率减小,则该反应的△H
的平衡转化率减小,则该反应的△H
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】利用太阳能光解水,制备的H2用于还原CO2合成有机物,可实现资源的再利用。用H2还原CO2可以在一定条下合成CH3OH(不考虑副反应): ,某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为
,某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为_______ 。
 ,某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为
,某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)⇌2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的ΔH________ 0(填“大于”或“小于”);
(2)100 ℃时,体系中各物质浓度随时间变化如图所示。
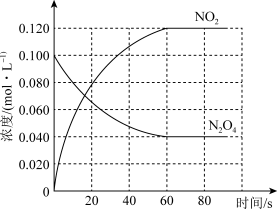
在0~60 s时段,反应速率v(N2O4)为___________________ mol·L-1·s-1;反应的平衡常数K的数值为_________________________ (保留两位小数)。
(3)100 ℃时,反应达平衡后,将反应容器的容积减少一半。平衡向________ (填“正反应”或“逆反应”)方向移动。
(4)100 ℃时达平衡后,改变反应温度为T,c(N2O4) 以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。T________ 100 ℃(填“大于”或“小于”)。
(1)反应的ΔH
(2)100 ℃时,体系中各物质浓度随时间变化如图所示。

在0~60 s时段,反应速率v(N2O4)为
(3)100 ℃时,反应达平衡后,将反应容器的容积减少一半。平衡向
(4)100 ℃时达平衡后,改变反应温度为T,c(N2O4) 以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。T
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】对于2X(g) Y(g)的体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。
Y(g)的体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。
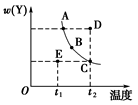
(1)该反应的正反应方向是一个________ 反应(“吸热”或“放热”)。
(2)A、B、C、D、E各状态中,v正<v逆的点是____________ 。
(3)维持t1不变,E→A所需时间为x,维持t2不变,D→C所需时间为y,则x______ y(填“<”、“>”或“=”)。
(4)欲使E状态从水平方向到C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的条件是____________ 。
 Y(g)的体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。
Y(g)的体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。
(1)该反应的正反应方向是一个
(2)A、B、C、D、E各状态中,v正<v逆的点是
(3)维持t1不变,E→A所需时间为x,维持t2不变,D→C所需时间为y,则x
(4)欲使E状态从水平方向到C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】甲醇燃料分为甲醇汽油和甲醇柴油。工业上合成甲醇的方法很多。
(1)一定条件下发生反应:
CO2(g) +3H2(g) =CH3OH(g)+H2O(g) △H1
2CO(g) +O2(g) =2CO2(g) △H2
2H2(g)+O2(g) =2H2O(g) △H3
则 CO(g) + 2H2(g) CH3OH(g) 的△H=
CH3OH(g) 的△H=________________ 。
(2)在容积为2L的密闭容器中进行反应:CO(g)+2H2(g) CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH) 与反应时间t的变化曲线如图所示。
CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH) 与反应时间t的变化曲线如图所示。
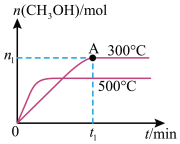
该反应的△H_____ 0 (填>、<或=)。
(3)若要提高甲醇的产率,可采取的措施有____________ (填字母)。
A.缩小容器体积 B.降低温度 C.升高温度 D.使用合适的催化剂 E.将甲醇从混合体系中分离出来
(1)一定条件下发生反应:
CO2(g) +3H2(g) =CH3OH(g)+H2O(g) △H1
2CO(g) +O2(g) =2CO2(g) △H2
2H2(g)+O2(g) =2H2O(g) △H3
则 CO(g) + 2H2(g)
 CH3OH(g) 的△H=
CH3OH(g) 的△H=(2)在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)
 CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH) 与反应时间t的变化曲线如图所示。
CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH) 与反应时间t的变化曲线如图所示。
该反应的△H
(3)若要提高甲醇的产率,可采取的措施有
A.缩小容器体积 B.降低温度 C.升高温度 D.使用合适的催化剂 E.将甲醇从混合体系中分离出来
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】T ℃下,向一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO浓度如下表:
(1)则c2合理的数值为________ (填字母)。
a.4.20 b.4.00 c.2.95 d.2.80
(2)将不同物质的量的H2O(g)和CO(g)分别通入体积为2 L的恒容密闭容器中,进行反应:H2O(g)+CO(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
若a=2,b=1,则c=______ ,达到平衡时实验组Ⅱ中H2O(g)和实验组Ⅲ中CO的转化率的关系为αⅡ(H2O)________ (填“<”“>”或“=”)αⅢ(CO)。
(3)二甲醚是清洁能源,用CO在催化剂存在下制备二甲醚的反应原理为2CO(g)+4H2(g) CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比
CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比 的变化曲线如图所示。
的变化曲线如图所示。
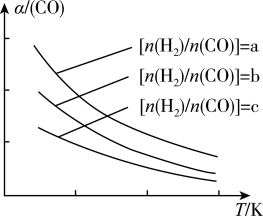
①a、b、c按从大到小的顺序排序为__________________________________________ 。
②根据图像可以判断该反应为放热反应,理由是_______________________________ 。
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/×10-4mol·L-1 | 10.0 | 4.50 | c1 | 1.50 | 1.00 | 1.00 |
| c(CO)/×10-3mol·L-1 | 3.60 | 3.05 | c2 | 2.75 | 2.70 | 2.70 |
(1)则c2合理的数值为
a.4.20 b.4.00 c.2.95 d.2.80
(2)将不同物质的量的H2O(g)和CO(g)分别通入体积为2 L的恒容密闭容器中,进行反应:H2O(g)+CO(g)
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:| 实验组 | 温度/℃ | 起始量/mol | 平衡量/ mol | 达到平衡所需时间/min | ||
| H2O | CO | CO | H2 | |||
| Ⅰ | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| Ⅱ | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| Ⅲ | 900 | a | b | c | d | t |
若a=2,b=1,则c=
(3)二甲醚是清洁能源,用CO在催化剂存在下制备二甲醚的反应原理为2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比
CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比 的变化曲线如图所示。
的变化曲线如图所示。
①a、b、c按从大到小的顺序排序为
②根据图像可以判断该反应为放热反应,理由是
您最近一年使用:0次