CO2固定是实现碳达峰、碳中和的有效途径。使用不同催化剂,CO2固定的产物也不同。在戊二酸锌催化下,CO2固定方式主要有:
nCO2+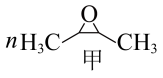
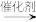
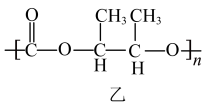
CO2+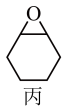
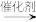
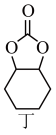
研究发现,利用氧化锌和戊二酸制备的戊二酸锌的催化效能良好。回答下列问题:
(1)一个基态氧原子的价层电子轨道表示式为______ ;基态碳原子核外有______ 个未成对电子。
(2)1mol丁含______ molσ键。
(3)乙中所含元素电负性由大到小的顺序为_____ (填元素符号),乙中碳原子的杂化类型是_____ 。
(4)戊二酸、丙二酸二甲酯的沸点分别为303℃、181℃,它们沸点差别较大的原因是_____ 。
(5)配离子[Zn(NH3)2(H2O)2]3+的空间结构只有1种,由此推知[Zn(NH3)4]2+的空间结构是______ 。
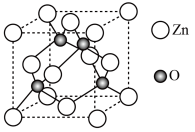
(6)ZnO晶胞结构如图所示。已知:ZnO晶体的密度为ρg/cm3,NA代表阿伏加德罗常数的值。氧离子的配位数为_____ 。氧和锌的最近距离为_____ nm。
nCO2+

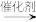

CO2+


研究发现,利用氧化锌和戊二酸制备的戊二酸锌的催化效能良好。回答下列问题:
(1)一个基态氧原子的价层电子轨道表示式为
(2)1mol丁含
(3)乙中所含元素电负性由大到小的顺序为
(4)戊二酸、丙二酸二甲酯的沸点分别为303℃、181℃,它们沸点差别较大的原因是
(5)配离子[Zn(NH3)2(H2O)2]3+的空间结构只有1种,由此推知[Zn(NH3)4]2+的空间结构是
(6)ZnO晶胞结构如图所示。已知:ZnO晶体的密度为ρg/cm3,NA代表阿伏加德罗常数的值。氧离子的配位数为

更新时间:2023-12-16 18:41:23
|
相似题推荐
【推荐1】根据元素在体内含量的不同,可将体内元素分为常量元素和微量元素。其中H、C、O、N、S、P等为常量元素,Fe、Zn等为微量元素。回答下列问题:
(1)基态Fe原子的核外电子排布式为[Ar]_______ ,有_______ 组相同能量的电子。
(2)数据表明,S元素的第一电离能小于P元素的第一电离能,其原因可能有两种:一种是S原子失去的是已经配对的电子,配对电子相互排斥,电离能较低,另一种是___________ 。
(3)原子的电子亲和能是指在0K下的气相中,原子获得电子变成负离子时所释放的能量。氧原子的第二电子亲和能(O-+e-→O2-释放的能量)不能直接在气相中测定,但可通过如图的Born-Haber循环计算得到。
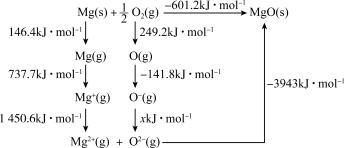
由图可知,Mg原子的第一电离能为___________ kJ·mol-1;O=O键键能为___________ kJ·mol-1;氧原子的第二电子亲和能为___________ kJ·mol-1。
(1)基态Fe原子的核外电子排布式为[Ar]
(2)数据表明,S元素的第一电离能小于P元素的第一电离能,其原因可能有两种:一种是S原子失去的是已经配对的电子,配对电子相互排斥,电离能较低,另一种是
(3)原子的电子亲和能是指在0K下的气相中,原子获得电子变成负离子时所释放的能量。氧原子的第二电子亲和能(O-+e-→O2-释放的能量)不能直接在气相中测定,但可通过如图的Born-Haber循环计算得到。
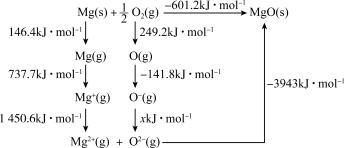
由图可知,Mg原子的第一电离能为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】周期表中前20种元素X、Y、Z、W原子序数依次增大,它们的结构性质等信息如下表所述:
请根据信息回答有关问题:
(1)元素X的原子核外共有_______ 种不同运动状态的电子,其基态原子中最高能级的电子云轮廓图形状是_______ 。
(2)Y的核外电子轨道表示式是_______ ,其价层电子的电子云在空间有_______ 种伸展方向。
(3)由X原子构成的共价晶体的名称是_______ ,晶体中X原子的杂化形式是_______ 。
(4)由Z和Y形成YZ3分子的电子式为_______ ,是_______ (填“极性”或“非极性”)分子。
| 元素 | 结构性质等信息 |
| X | 基态原子有三个能级,每个能级上的电子数都相等 |
| Y | 该元素原子价层电子排布式为nsnnpn+1 |
| Z | 常温常压下,该元素构成的单质是一种有毒的黄绿色气体 |
(1)元素X的原子核外共有
(2)Y的核外电子轨道表示式是
(3)由X原子构成的共价晶体的名称是
(4)由Z和Y形成YZ3分子的电子式为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】三氯甲烷为无色油状液体,不溶于水,密度比水大,是良好的有机溶剂。但对光敏感,遇光照会与空气中的氧作用,产生剧毒的光气:2CHCl3+O2 = 2HCl+2COCl2。
(1)氯的原子结构示意图为_______ , 氯所在周期的元素中,最高价氧化物所对应水化物碱性最强的是_______ (填化学式)。O、S等都是氧族元素,该族元素最外层电子的轨道表示式为_______ ;
(2)中子数为8的碳原子的符号可表示为_______ ;三氯甲烷的空间构型是_______ ;
(3)光气的结构式为 ,下列关于光气分子的说法正确的是_______;
,下列关于光气分子的说法正确的是_______;
(4)标准状况下,该反应每消耗11.2L空气(氧气的体积分数为21%),则发生转移的电子有_______ mol。
(5)若保管不当,三氯甲烷会被空气氧化而变质。实验室欲检验某试剂瓶内存放的三氯甲烷是否因氧化而变质,可用_______ (填试剂名称)进行检验。选用该试剂的理由是_______ 。
(1)氯的原子结构示意图为
(2)中子数为8的碳原子的符号可表示为
(3)光气的结构式为
 ,下列关于光气分子的说法正确的是_______;
,下列关于光气分子的说法正确的是_______;A.比例模型为 |
B.电子式是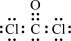 |
| C.具有极性键和非极性键 |
| D.所有原子都达到了最外层8电子稳定结构 |
(5)若保管不当,三氯甲烷会被空气氧化而变质。实验室欲检验某试剂瓶内存放的三氯甲烷是否因氧化而变质,可用
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】 、
、 、
、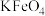 、NaClO和
、NaClO和 都是重要的氧化剂。
都是重要的氧化剂。
(1)Mn位于元素周期表第___________ 周期___________ 族,基态Mn原子未成对的电子数为___________ 。
(2)基态Cr原子的核外电子排布式为___________ ,第四周期ds区元素中,与基态Cr原子最外层电子数目相同的元素的元素符号为___________ 。
(3) 中,电负性最低的元素是
中,电负性最低的元素是___________ (填元素符号);硝酸根中N的___________ 杂化轨道与O的2p轨道形成___________ 键(填“ ”或“
”或“ ”)。
”)。
(4)NaClO的电子式为___________ ,NaClO在水溶液中会水解产生HClO分子,该分子的立体构型为___________ 。
(5)铁的各级电离能数据为:第一电离能 、第二电离能
、第二电离能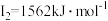 、第三电离能
、第三电离能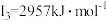 、第四电离能
、第四电离能 、第五电离能
、第五电离能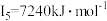 …,
…, 明显大于
明显大于 的原因是
的原因是___________ 。
 、
、 、
、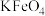 、NaClO和
、NaClO和 都是重要的氧化剂。
都是重要的氧化剂。(1)Mn位于元素周期表第
(2)基态Cr原子的核外电子排布式为
(3)
 中,电负性最低的元素是
中,电负性最低的元素是 ”或“
”或“ ”)。
”)。(4)NaClO的电子式为
(5)铁的各级电离能数据为:第一电离能
 、第二电离能
、第二电离能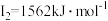 、第三电离能
、第三电离能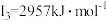 、第四电离能
、第四电离能 、第五电离能
、第五电离能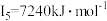 …,
…, 明显大于
明显大于 的原因是
的原因是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】根据物质结构有关性质和特点,回答下列问题:
(1)基态As原子的价层电子的电子云轮廓图形状为_____________ 。
(2)Na3AsO3可用于碘的微量分析。Na3AsO3中所含阴离子的立体构型为_____________ ,写出一种与其互为等电子体的分子:_____________ (填化学式)。
(3)丙烯腈(CH2=CH-CN)分子中碳原子轨道杂化类型是____________ 。
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为___________ 。区分晶体Ni和非晶体Ni的最可靠的科学方法为___________ 。
(5)钛存在两种同素异形体,α—Ti采纳六方最密堆积,β—Ti采纳体心立方堆积,由α—Ti转变为β—Ti晶体体积____________ (填“膨胀”或“收缩”)。
(6)某镍白铜合金的立方晶胞结构如图所示。若合金的密度为d g·cm-3,晶胞参数a=______ nm。
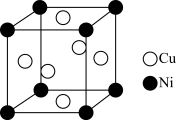
(1)基态As原子的价层电子的电子云轮廓图形状为
(2)Na3AsO3可用于碘的微量分析。Na3AsO3中所含阴离子的立体构型为
(3)丙烯腈(CH2=CH-CN)分子中碳原子轨道杂化类型是
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为
(5)钛存在两种同素异形体,α—Ti采纳六方最密堆积,β—Ti采纳体心立方堆积,由α—Ti转变为β—Ti晶体体积
(6)某镍白铜合金的立方晶胞结构如图所示。若合金的密度为d g·cm-3,晶胞参数a=

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】硫是一种重要的非金属元素,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是_______ 。
(2)①硫单质的一种结构为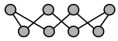 ,杂化方式为
,杂化方式为_______ ;CS2中C的杂化方式为_______ 。
② 、CS2、
、CS2、 键角由大到小的顺序是
键角由大到小的顺序是_______ 。
(3)ZnS晶胞如图所示:_______ 空隙中。
A.正四面体 B.正六面体 C.正八面体
②已知晶胞密度为ρg/cm3,阿伏加德罗常数为NA,则晶胞边长为_______ pm。
(1)基态硫原子的价层电子排布图是
(2)①硫单质的一种结构为
 ,杂化方式为
,杂化方式为②
 、CS2、
、CS2、 键角由大到小的顺序是
键角由大到小的顺序是(3)ZnS晶胞如图所示:
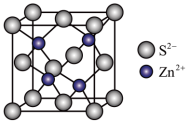
A.正四面体 B.正六面体 C.正八面体
②已知晶胞密度为ρg/cm3,阿伏加德罗常数为NA,则晶胞边长为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(1)硫及其化合物有许多用途,相关物质的物理常数如下表所示:
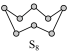
如图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为______________________________________ 。
(2)关于化合物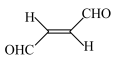 ,下列叙述正确的是
,下列叙述正确的是________ 。
A.分子间可形成氢键
B.分子中既有极性键又有非极性键
C.分子中有7个σ键和1个π键
D.该分子在水中的溶解度大于2丁烯
(3)已知苯酚(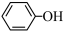 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子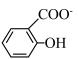 能形成分子内氢键,据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键,据此判断,相同温度下电离平衡常数Ka2(水杨酸)__________ Ka(苯酚)(填“>”或“<”),其原因是____________________ 。
(4)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为_________________________ 。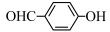 的沸点比
的沸点比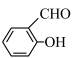 高,原因是
高,原因是__________ 。
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
如图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(2)关于化合物
 ,下列叙述正确的是
,下列叙述正确的是A.分子间可形成氢键
B.分子中既有极性键又有非极性键
C.分子中有7个σ键和1个π键
D.该分子在水中的溶解度大于2丁烯
(3)已知苯酚(
 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键,据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键,据此判断,相同温度下电离平衡常数Ka2(水杨酸)(4)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为
 的沸点比
的沸点比 高,原因是
高,原因是
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
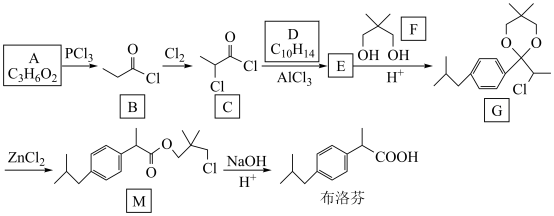
【推荐2】布洛芬可以缓解新冠病毒感染的症状,对新冠病毒感染有一定的治疗作用,其中一种合成路线如图所示。
已知:①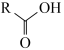
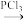
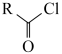
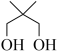
②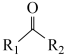 +
+

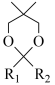 +H2O
+H2O
回答下列问题:
(1)A具有的官能团名称为_____ 。
(2)布洛芬的分子式为_____ ,最多有____ 个原子共平面。
(3)F的化学名称为______ ,其易溶于水的原因为_____ 。
(4)B→C的反应类型为_____ 。
(5)E+F→G的化学方程式为_____ 。
(6)D的同分异构体中,苯环上的一氯取代物有两种的化合物共有_____ 种(不含立体异构)。

已知:①

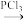

②
 +
+

 +H2O
+H2O回答下列问题:
(1)A具有的官能团名称为
(2)布洛芬的分子式为
(3)F的化学名称为
(4)B→C的反应类型为
(5)E+F→G的化学方程式为
(6)D的同分异构体中,苯环上的一氯取代物有两种的化合物共有
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态镍原子价电子排布式为___________ 。
(2)丁二酮肟( )是检验Ni2+的灵敏试剂,常与Ni2+形成图I所示的配合物,图II是硫代氧的结果:
)是检验Ni2+的灵敏试剂,常与Ni2+形成图I所示的配合物,图II是硫代氧的结果:
①下列说法正确的有___________ (填字母)。
A.在I中N元素的电负性最大 B.在I中C-C-C键角是180°
C.在II中-SH 上的S原子采取sp3杂化 D.在II中存在σ键、Π键与配位键
②化合物I的熔、沸点高于化合物II的原因是___________ 。
(3)工业上选用硫酸和硝酸的混酸与Ni反应制备NiSO4。写出与SO 互为等电子体的一种分子
互为等电子体的一种分子___________ 。Fe、Co、Ni三种元素二价离子的硫酸盐晶体的晶胞类型相同,其熔点由高到低的顺序为___________ 。
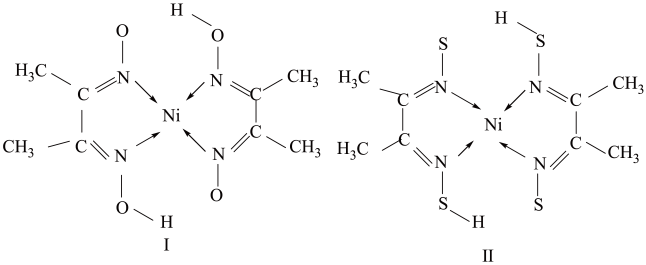
(4)Ni和La的合金是目前使用广泛的储氢材料。该合金的晶胞结构如图所示。
①设该合金的密度为dg/cm3,则该晶胞的体积为___________ cm3(用含 d的代数式表示,NA表示阿伏加德罗常数的值)
②该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知:a=500pm,c=400pm;标准状况下氢气的密度为9.00×10-5g/cm3; 储氢能力= 。若忽略储氢前后晶胞的体积变化,则该合金的储氢能力为
。若忽略储氢前后晶胞的体积变化,则该合金的储氢能力为___________ (列出最简计算式,计算式不使用小数。NA表示阿伏加德罗常数的值)。
(1)基态镍原子价电子排布式为
(2)丁二酮肟(
 )是检验Ni2+的灵敏试剂,常与Ni2+形成图I所示的配合物,图II是硫代氧的结果:
)是检验Ni2+的灵敏试剂,常与Ni2+形成图I所示的配合物,图II是硫代氧的结果:
①下列说法正确的有
A.在I中N元素的电负性最大 B.在I中C-C-C键角是180°
C.在II中-SH 上的S原子采取sp3杂化 D.在II中存在σ键、Π键与配位键
②化合物I的熔、沸点高于化合物II的原因是
(3)工业上选用硫酸和硝酸的混酸与Ni反应制备NiSO4。写出与SO
 互为等电子体的一种分子
互为等电子体的一种分子(4)Ni和La的合金是目前使用广泛的储氢材料。该合金的晶胞结构如图所示。

①设该合金的密度为dg/cm3,则该晶胞的体积为
②该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知:a=500pm,c=400pm;标准状况下氢气的密度为9.00×10-5g/cm3; 储氢能力=
 。若忽略储氢前后晶胞的体积变化,则该合金的储氢能力为
。若忽略储氢前后晶胞的体积变化,则该合金的储氢能力为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】H、N、O、S、Ni、As为元素周期表中1~4周期元素。请回答下列问题:
(1)上述元素中第一电离能最大的元素符号是___________ ,电负性最大的元素的原子其价电子轨道表示式为___________ 。
(2)CH3NO2中C和N的原子轨道杂化方式分别为___________ 、___________ 。
(3)SO32-其空间构型为___________ 。写出一种与该酸根等电子体的微粒___________ 。
(4)NH3极易溶于水其原因除二者都为极性分子外,另一个重要原因是___________ 。
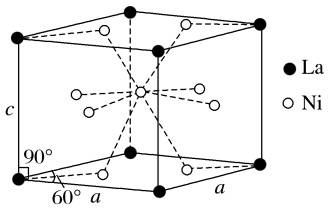
(5)Ni与As形成的一种化合物,其晶体如图所示,属六方晶系。
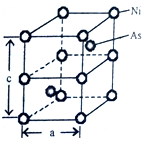
①该晶体的化学式为___________ ,As原子的配位数为___________ 。
②已知晶胞参数a=360.2pm,c=500.9pm,此晶体的密度为___________ g·cm-3。(写出计算式,NA为阿伏伽德罗常数的值)
(1)上述元素中第一电离能最大的元素符号是
(2)CH3NO2中C和N的原子轨道杂化方式分别为
(3)SO32-其空间构型为
(4)NH3极易溶于水其原因除二者都为极性分子外,另一个重要原因是
(5)Ni与As形成的一种化合物,其晶体如图所示,属六方晶系。

①该晶体的化学式为
②已知晶胞参数a=360.2pm,c=500.9pm,此晶体的密度为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】2011年,谢赫德曼因发现“准晶体”独享诺贝尔化学奖。2009年,科学家们在俄罗斯东部的河流中发现了十分耐磨的天然准晶体矿物Al63Cu24Fe13,有力地证明了准晶体理论。回答下列问题。
(1)可通过_____ 方法区分晶体、准晶体和非晶体。
(2)基态Fe原子的电子排布式是_____ 。铝和铁的第一电离能的大小次序是_____ 。
(3)五羰基合铁[Fe(CO)5]是一种浅黄色难溶于水的液体,其熔点-20℃,沸点103℃。依据以上信息可推断五羰基合铁属于______ (“准晶体”、“离子晶体”、“分子晶体”或“原子晶体”)。
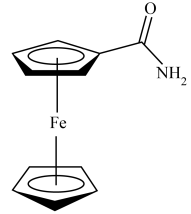
(4)二茂铁甲酰胺的结构如下图所示。其中N原子的杂化方式为______ 。
(5)工业用沉淀法制备磁性材料铁氧体,一般在制备的时候使用NH3和N2H4等弱碱。比较表格中的熔沸点数据,发现N2H4的熔沸点高于NH3的熔沸点,其原因是_____ 。
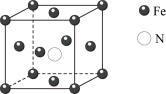
(6)氮和铁也能形成一种磁性材料,其晶胞如下图所示,该磁性材料的化学式为_____ 。晶胞参数为anm,则该晶胞密度的计算式为ρ=____ g/cm3(用NA表示阿伏加 德罗常数的值)。
(1)可通过
(2)基态Fe原子的电子排布式是
(3)五羰基合铁[Fe(CO)5]是一种浅黄色难溶于水的液体,其熔点-20℃,沸点103℃。依据以上信息可推断五羰基合铁属于
(4)二茂铁甲酰胺的结构如下图所示。其中N原子的杂化方式为

(5)工业用沉淀法制备磁性材料铁氧体,一般在制备的时候使用NH3和N2H4等弱碱。比较表格中的熔沸点数据,发现N2H4的熔沸点高于NH3的熔沸点,其原因是
NH3 | N2H4 | |
熔点/℃ | -78 | 2 |
沸点/℃ | -34 | 113 |
(6)氮和铁也能形成一种磁性材料,其晶胞如下图所示,该磁性材料的化学式为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ. 、
、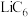 是重要的电极材料,回答下列问题:
是重要的电极材料,回答下列问题:
(1)基态Co原子的价电子排布式为__________ 。
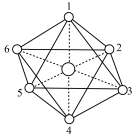
(2)Co(Ⅲ)可形成多种配合物,如图所示是 结构,
结构, 位于正八面体中心,若其中两个
位于正八面体中心,若其中两个 被
被 取代,则
取代,则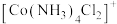 的空间结构有
的空间结构有__________ 种。
(3) 、
、 在合成化学上应用广泛。
在合成化学上应用广泛。 的空间结构为
的空间结构为__________ ; 、
、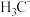 、
、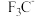 的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是
的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是__________ 。
Ⅱ.钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
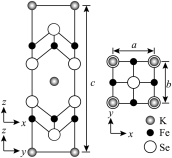
(4)该超导材料的最简化学式为__________ ;
(5)该晶胞参数a=b=0.4nm、c=1.4nm。阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为__________  (列出计算式)。
(列出计算式)。
 、
、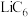 是重要的电极材料,回答下列问题:
是重要的电极材料,回答下列问题:(1)基态Co原子的价电子排布式为
(2)Co(Ⅲ)可形成多种配合物,如图所示是
 结构,
结构, 位于正八面体中心,若其中两个
位于正八面体中心,若其中两个 被
被 取代,则
取代,则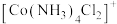 的空间结构有
的空间结构有
(3)
 、
、 在合成化学上应用广泛。
在合成化学上应用广泛。 的空间结构为
的空间结构为 、
、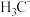 、
、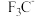 的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是
的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是Ⅱ.钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:

(4)该超导材料的最简化学式为
(5)该晶胞参数a=b=0.4nm、c=1.4nm。阿伏加德罗常数的值为
 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近半年使用:0次



