已知 属于难溶于水、可溶于酸的盐。常温下,用
属于难溶于水、可溶于酸的盐。常温下,用 调节
调节 浊液的
浊液的 ,测得在不同
,测得在不同 条件下,体系中
条件下,体系中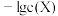 (
( 为
为 或
或 )与
)与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 属于难溶于水、可溶于酸的盐。常温下,用
属于难溶于水、可溶于酸的盐。常温下,用 调节
调节 浊液的
浊液的 ,测得在不同
,测得在不同 条件下,体系中
条件下,体系中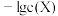 (
( 为
为 或
或 )与
)与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
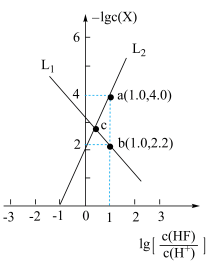
A. 代表 代表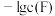 与 与 的变化曲线 的变化曲线 |
B.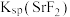 的数量级为 的数量级为 |
C.a点的溶液中存在 |
D. 点的溶液中存在 点的溶液中存在 |
2024·四川自贡·一模 查看更多[3]
(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)四川省泸州市泸县第一中学2023-2024学年高二上学期1月期末化学试题2024届四川省自贡市普高高三上学期第一次诊断性考试理综试题
更新时间:2023-12-19 12:48:31
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】电解质溶液导电能力越强,电导率越大。常温下用0.1000 mol/L盐酸分别滴定10.00 mL浓度均为0.1000 mol/L的NaOH溶液和二甲胺[(CH3)2NH]溶液{二甲胺在水中电离与氨相似,已知在常温下Kb[(CH3)2NH·H2O]=1.6×10-4},利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
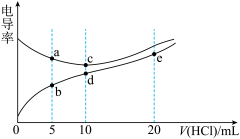

| A.盐酸滴定二甲胺实验中选择酚酞作指示剂比选甲基橙误差更小 |
| B.d点溶液中:c(H+)>c(OH-)+c[(CH3)2NH2+] |
| C.b、c、d、e四点的溶液中,水的电离程度最大的是d点 |
| D.a点溶液与d点的溶液混合后的溶液中: c(OH-) < c(H+) < c[(CH3)2 NH2+] <c(Na+)< c(Cl-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】亚氯酸钠(NaClO2)在溶液中对生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都是具有漂白作用。已知pOH=﹣lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析正确的是


| A.HClO2的电离平衡常数的数值Ka=10-8 |
| B.pOH=11时,ClO2-部分转化成ClO2和Cl-离子的方程式为:5ClO2-+2H2O=4ClO2+ Cl-+4OH- |
| C.pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-) |
| D.同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知:25℃, 的电离平衡常数
的电离平衡常数 ,25℃,向1L
,25℃,向1L 某一元酸里
某一元酸里 溶液中逐渐通入氨,若溶液温度和体积保持不变,所得混合溶液的
溶液中逐渐通入氨,若溶液温度和体积保持不变,所得混合溶液的 与
与 变化的关系如图所示。下列叙述不正确的是
变化的关系如图所示。下列叙述不正确的是

 的电离平衡常数
的电离平衡常数 ,25℃,向1L
,25℃,向1L 某一元酸里
某一元酸里 溶液中逐渐通入氨,若溶液温度和体积保持不变,所得混合溶液的
溶液中逐渐通入氨,若溶液温度和体积保持不变,所得混合溶液的 与
与 变化的关系如图所示。下列叙述不正确的是
变化的关系如图所示。下列叙述不正确的是
A.由图可推知,25℃时  溶液的 溶液的 约为10 约为10 |
B.当通入  时,所得溶液中: 时,所得溶液中: |
C. 时,所得溶液中: 时,所得溶液中: |
D. 时,所得溶液中: 时,所得溶液中: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,已知某三元弱酸H3A的三级电离平衡常数分别为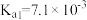 、
、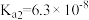 、
、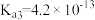 ,下列说法
,下列说法错误 的是
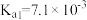 、
、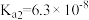 、
、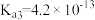 ,下列说法
,下列说法| A.Na3A的第一级水解平衡常数Kh1的数量级为10-2 |
B.在NaH2A溶液中: |
| C.0.1mol/L的Na3A和0.1mol/L的Na2HA溶液中水电离程度,前者大于后者 |
| D.向H3A溶液中加入NaOH溶液至中性时:c(Na+)=3c(A3-)+2c(HA2-)+c(H2A-) |
您最近一年使用:0次
【推荐1】常温下几种阳离子浓度与溶液pH的关系如图所示。据图判断下列说法正确的是


| A.Ksp[Cu(OH)2]=1.0×10-15 |
| B.Mg(OH)2饱和溶液中c(Mg2+)=1.0×10-4 mol/L |
| C.a点可表示Fe(OH)3的不饱和溶液,Cu(OH)2的饱和溶液 |
| D.Fe3+、Cu2+、Fe2+浓度均为0.01 mol/L的混合溶液中加入足量H2O2溶液后,调节pH=3.2时可将Fe3+、Fe2+全部除去,而Cu2+不会产生沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 用乙酸浸泡水壶中的水垢,可将其清除 | 乙酸的酸性小于碳酸 |
| B | 将MgCl2溶液加热蒸干,得到白色固体 | 固体为MgCl2 |
| C | 向某溶液中滴加K3[Fe(CN)6]溶液,产生蓝色沉淀 | 原溶液中有Fe2+ |
| D | 向盛有1 mL 2 mol/L NaOH溶液的试管中滴入几滴0.1 mol/L MgCl2溶液,有白色沉淀生成;再加入几滴0.1 mol/L FeCl3溶液,有红褐色沉淀生成 | Ksp[Mg(OH)2] >Ksp[Fe(OH)3] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 ,溶液中
,溶液中 、
、 、
、 和
和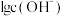 随pH变化的关系如图所示。下列说法错误的是
随pH变化的关系如图所示。下列说法错误的是

 的数量级为
的数量级为

 的水解程度始终增大
的水解程度始终增大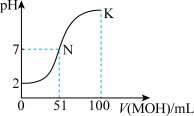
 减小
减小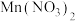 、
、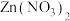 、HNO2溶液中滴加NaOH溶液,溶液pX[
、HNO2溶液中滴加NaOH溶液,溶液pX[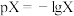 ,X代表
,X代表 、
、 、
、 ]与pH的关系如图所示。已知:
]与pH的关系如图所示。已知: 。下列说法错误的是
。下列说法错误的是

 的数量级为
的数量级为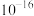
 比
比 更易溶于HNO2
更易溶于HNO2


