甲烷重整时涉及以下两个反应:
①CH4(g)+H2O(g) CO(g)+3H2(g) K1②CO(g)+H2O(g)
CO(g)+3H2(g) K1②CO(g)+H2O(g) CO2(g)+H2(g) K2
CO2(g)+H2(g) K2
它们的平衡常数随温度的变化如图所示,下列说法正确的是

①CH4(g)+H2O(g)
 CO(g)+3H2(g) K1②CO(g)+H2O(g)
CO(g)+3H2(g) K1②CO(g)+H2O(g) CO2(g)+H2(g) K2
CO2(g)+H2(g) K2它们的平衡常数随温度的变化如图所示,下列说法正确的是

| A.反应①、②都是放热反应 |
| B.两曲线交点表示此时①、②两反应速率相等 |
C.相同温度下,CH4(g)+2H2O(g) CO2(g)+4H2(g)的平衡常数为K1+K2 CO2(g)+4H2(g)的平衡常数为K1+K2 |
| D.相同条件下,增大反应①中水蒸气的浓度,CH4的转化率增大 |
更新时间:2023-12-28 11:51:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】反应
 可用于消除汽车尾气中的有害气体。在密闭容器中充入
可用于消除汽车尾气中的有害气体。在密闭容器中充入
 和
和
 ,平衡时
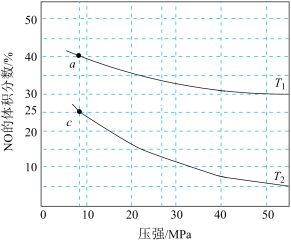
,平衡时 的体积分数随温度、压强的变化关系如下图所示。下列说法不正确的是
的体积分数随温度、压强的变化关系如下图所示。下列说法不正确的是

 可用于消除汽车尾气中的有害气体。在密闭容器中充入
可用于消除汽车尾气中的有害气体。在密闭容器中充入
 和
和
 ,平衡时
,平衡时 的体积分数随温度、压强的变化关系如下图所示。下列说法不正确的是
的体积分数随温度、压强的变化关系如下图所示。下列说法不正确的是
A.若a、c两点的正反应速率分别为 、 、 ,则 ,则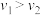 |
B.c点处 的体积分数为12.5% 的体积分数为12.5% |
C.a点处 的平衡转化率为12.5% 的平衡转化率为12.5% |
D.当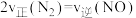 时,反应 时,反应 达到平衡 达到平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
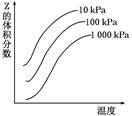
【推荐2】如图是温度和压强对反应X+Y 2Z影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
2Z影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
 2Z影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
2Z影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
| A.恒容时,混合气体的密度可作为此反应是否达到化学平衡状态的判断依据 |
| B.X、Y、Z均为气态 |
| C.上述反应的逆反应的△H>0 |
| D.使用催化剂Z的产率提高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
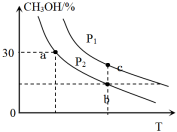
【推荐3】以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。向2L容器中充入lmolCO2和3molH2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得反应在不同温度和压强下,平衡混合物中CH3OH体积分数如图所示。下列说法错误的是
CH3OH(g)+H2O(g),测得反应在不同温度和压强下,平衡混合物中CH3OH体积分数如图所示。下列说法错误的是
 CH3OH(g)+H2O(g),测得反应在不同温度和压强下,平衡混合物中CH3OH体积分数如图所示。下列说法错误的是
CH3OH(g)+H2O(g),测得反应在不同温度和压强下,平衡混合物中CH3OH体积分数如图所示。下列说法错误的是
| A.P1>P2 |
| B.a点CO2的转化率为75% |
| C.a、b、c三点对应的化学反应速率v(a)<v(c)<v(b) |
| D.b→a过程,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】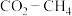 重整可获得
重整可获得 。
。 重整反应的热化学方程式为
重整反应的热化学方程式为
反应I: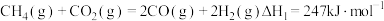
反应Ⅱ: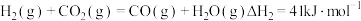
反应Ⅲ:
 下,将
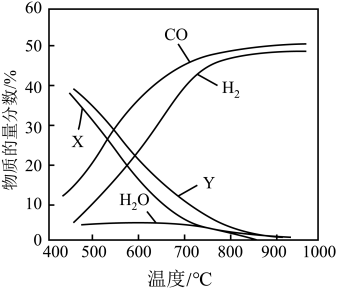
下,将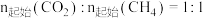 的混合气体置于密闭容器中,不同温度下重整体系中,平衡时各气体组分的物质的量分数如图所示。下列说法
的混合气体置于密闭容器中,不同温度下重整体系中,平衡时各气体组分的物质的量分数如图所示。下列说法不正确 的是
 重整可获得
重整可获得 。
。 重整反应的热化学方程式为
重整反应的热化学方程式为反应I:
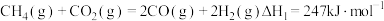
反应Ⅱ:
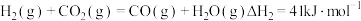
反应Ⅲ:

 下,将
下,将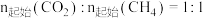 的混合气体置于密闭容器中,不同温度下重整体系中,平衡时各气体组分的物质的量分数如图所示。下列说法
的混合气体置于密闭容器中,不同温度下重整体系中,平衡时各气体组分的物质的量分数如图所示。下列说法
A.曲线X表示 |
B.反应 进行的程度很小 进行的程度很小 |
C.500℃, 时,向平衡体系中再充入一定量的 时,向平衡体系中再充入一定量的 ,达新平衡后, ,达新平衡后,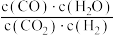 保持不变 保持不变 |
D.随着温度升高,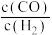 变小。原因是反应Ⅲ增大的程度小于反应Ⅱ增大的程度 变小。原因是反应Ⅲ增大的程度小于反应Ⅱ增大的程度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】学习小组对可逆反应
 进行探究。常温下,向盛有2mL0.01
进行探究。常温下,向盛有2mL0.01
 溶液的试管中滴加2滴0.01
溶液的试管中滴加2滴0.01 KSCN溶液,改变下列条件,试管中溶液颜色不会加深的是
KSCN溶液,改变下列条件,试管中溶液颜色不会加深的是

 进行探究。常温下,向盛有2mL0.01
进行探究。常温下,向盛有2mL0.01
 溶液的试管中滴加2滴0.01
溶液的试管中滴加2滴0.01 KSCN溶液,改变下列条件,试管中溶液颜色不会加深的是
KSCN溶液,改变下列条件,试管中溶液颜色不会加深的是| A.将试管放入冰水浴中 | B.加水稀释 |
C.加入1 KSCN溶液 KSCN溶液 | D.加入少量 固体 固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于化学平衡常数的说法正确的是
| A.在任何条件下,化学平衡常数都不变 |
| B.当改变反应物的浓度时,化学平衡常数会发生改变 |
| C.由化学平衡常数K可以推断一个可逆反应进行的程度 |
| D.化学平衡常数K与温度、反应物浓度以及体系的压强有关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用合成气(主要成分为CO、CO2和H2)通过下列反应合成甲醇。下列说法正确的是
反应①:CO2(g)+H2(g) CO(g)+H2O(g) △H1=41kJ·mol–1
CO(g)+H2O(g) △H1=41kJ·mol–1
反应②:CO(g)+2H2(g) CH3OH(g) △H2=–99kJ·mol–1
CH3OH(g) △H2=–99kJ·mol–1
反应③:CO2(g)+3H2(g) CH3OH(g) + H2O(l) △H3
CH3OH(g) + H2O(l) △H3
反应①:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=41kJ·mol–1
CO(g)+H2O(g) △H1=41kJ·mol–1反应②:CO(g)+2H2(g)
 CH3OH(g) △H2=–99kJ·mol–1
CH3OH(g) △H2=–99kJ·mol–1反应③:CO2(g)+3H2(g)
 CH3OH(g) + H2O(l) △H3
CH3OH(g) + H2O(l) △H3| A.反应①为放热反应 | B.增大反应①的压强,H2转化率提高 |
| C.△H3=-58kJ·mol–1 | D.反应②使用催化剂,△H2不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 催化加氢是碳中和的重要手段之一,以下是
催化加氢是碳中和的重要手段之一,以下是 加氢时发生的两个主要反应:
加氢时发生的两个主要反应:
反应Ⅰ:

反应Ⅱ:

在体积为1L的两个恒容密闭容器中分别按表中所示充入一定量的 和
和 ,平衡体系中碳化物的物质的量分数X(CO)和
,平衡体系中碳化物的物质的量分数X(CO)和 随温度变化关系如图所示。
随温度变化关系如图所示。
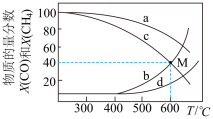
下列有关说法错误的是
 催化加氢是碳中和的重要手段之一,以下是
催化加氢是碳中和的重要手段之一,以下是 加氢时发生的两个主要反应:
加氢时发生的两个主要反应:反应Ⅰ:


反应Ⅱ:


在体积为1L的两个恒容密闭容器中分别按表中所示充入一定量的
 和
和 ,平衡体系中碳化物的物质的量分数X(CO)和
,平衡体系中碳化物的物质的量分数X(CO)和 随温度变化关系如图所示。
随温度变化关系如图所示。
| 容器 | 起始物质的量/mol | |
 |  | |
| 甲 | 1 | 3 |
| 乙 | 2 | 6 |
| A.曲线d表示乙容器中X(CO)随温度的变化 |
| B.600℃达到平衡时,甲容器中反应Ⅱ的平衡常数为2.4 |
C.M点对应 的转化率为80% 的转化率为80% |
| D.使用选择性催化剂,M点位置保持不变 |
您最近一年使用:0次
【推荐2】一定温度下,在三个体积均为1.0L的恒容密闭容器中,反应2H2(g)+CO(g) CH3OH(g)达到平衡。下列说法
CH3OH(g)达到平衡。下列说法错误 的是
 CH3OH(g)达到平衡。下列说法
CH3OH(g)达到平衡。下列说法| 容器 | 温度/K | 起始浓度/mol·L-1 | 平衡浓度mol·L-1 | ||
| H2 | CO | CH3OH | CH3OH | ||
| ① | 400 | 0.20 | 0.10 | 0 | 0.08 |
| ② | 400 | 0.40 | 0.20 | 0 | X |
| ③ | 500 | 0 | 0 | 0.10 | 0.025 |
| A.该反应的正反应是放热反应 | B.平衡时的反应速率:③>① |
| C.X=0.16 | D.400K时该反应平衡常数的值为2500 |
您最近一年使用:0次

 2Z(g) △H<0,若反应开始经t1后达到平衡,又经t2后由于反应条件的改变使平衡破坏,到t3时又达平衡(如图所示),t2~t3曲线变化的原因是
2Z(g) △H<0,若反应开始经t1后达到平衡,又经t2后由于反应条件的改变使平衡破坏,到t3时又达平衡(如图所示),t2~t3曲线变化的原因是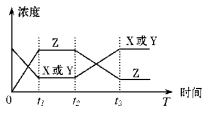
 2CO(g)下列能表明该反应已达到平衡状态的是(
2CO(g)下列能表明该反应已达到平衡状态的是(