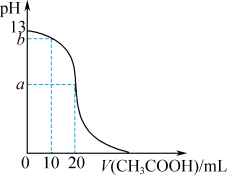
常温下,量取10.00mL 溶液置于锥形瓶中,加入指示剂,用
溶液置于锥形瓶中,加入指示剂,用 溶液滴定,所得溶液的
溶液滴定,所得溶液的 随
随 溶液体积的变化如图所示,达到滴定终点时,消耗
溶液体积的变化如图所示,达到滴定终点时,消耗 溶液20.00mL。下列说法正确的是
溶液20.00mL。下列说法正确的是
 溶液置于锥形瓶中,加入指示剂,用
溶液置于锥形瓶中,加入指示剂,用 溶液滴定,所得溶液的
溶液滴定,所得溶液的 随
随 溶液体积的变化如图所示,达到滴定终点时,消耗
溶液体积的变化如图所示,达到滴定终点时,消耗 溶液20.00mL。下列说法正确的是
溶液20.00mL。下列说法正确的是
A. 溶液的浓度为 溶液的浓度为 |
B. |
C.当 时,溶液中存在 时,溶液中存在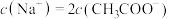 |
D. 、 、 两点对应溶液中,由水电离出的 两点对应溶液中,由水电离出的 a>b a>b |
更新时间:2024-02-10 15:22:59
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】甲、乙两人用同一瓶盐酸滴定同一瓶NaOH溶液。甲将锥形瓶用NaOH待测液润洗后,使用水洗过的碱式滴定管取碱液于锥形瓶中;乙则用甲用过的滴定管取碱液于刚用蒸馏水洗过且存有蒸馏水的锥形瓶中,其他操作及读数均正确,你的判断是
| A.甲操作有错 | B.乙操作有错 |
| C.甲测定数值一定比乙小 | D.乙实际测得值较不准确 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关关仪器的使用方法或实验操作正确的是
| A.配制一定物质的量浓度溶液中,洗净的容量瓶要放进烘箱中烘干,以防溶液被稀释 |
| B.测量Zn与稀硫酸反应速率的实验中,应在标准状况下测量H2的体积,以方便计算 |
| C.酸碱滴定实验中,用待测溶液润洗锥形瓶,以减少实验误差 |
| D.中和热的测定实验中,要用环形玻璃搅拌棒搅拌,使反应更充分 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】化学上常用AG表示溶液中的lg 。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的一元酸HA溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是
。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的一元酸HA溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是

 。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的一元酸HA溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是
。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的一元酸HA溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是
A.随着NaOH溶液的加入, 减小 减小 |
| B.25℃时,HA的电离常数Ka≈1.0×10-4.5 |
| C.b点溶液中存在c(H+)+c(HA)=c(OH-)+c(A-) |
| D.a、b、c、d、e五点的溶液中,水的电离程度最大的点是e |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下图三条曲线表示不同温度下水的离子积常数,下列说法不正确的是


A.图中温度: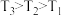 | B.图中 的关系: 的关系: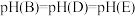 |
| C.C点物质可能是盐酸 | D.图中五点 间的关系: 间的关系: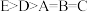 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,向20m1某稀Ba(OH)2溶液中滴入浓度为0.1mol/L的醋酸。溶液中由水电离出的氢氧根离子浓度随滴入醋酸的体积变化如图,下列分析正确的是
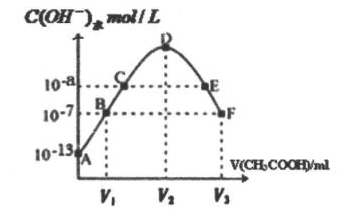

| A.稀Ba(OH)2溶液的浓度为0.1mol・L-1 |
| B.C点溶液的PH=a |
| C.D点溶液中c(OH-)<c(H+)+c(CH3COOH) |
| D.E点溶液中存在c(CH3COO-)>c(Ba2+)>C(OH-)>C(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】25℃时,将1
 的二元酸
的二元酸 与
与 分别加水稀释至100倍和200倍,所得溶液
分别加水稀释至100倍和200倍,所得溶液 均为4.下列说法中不正确的是
均为4.下列说法中不正确的是

 的二元酸
的二元酸 与
与 分别加水稀释至100倍和200倍,所得溶液
分别加水稀释至100倍和200倍,所得溶液 均为4.下列说法中不正确的是
均为4.下列说法中不正确的是A. 为强酸, 为强酸, 为弱酸 为弱酸 |
B.等体积0.1 的 的 与 与 溶液中分别加入等质量铁粉,后者产生气泡较快 溶液中分别加入等质量铁粉,后者产生气泡较快 |
C.0.1 的 的 、 、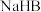 溶液等体积混合后,溶液中存在 溶液等体积混合后,溶液中存在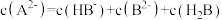 |
D. 的 的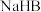 溶液中: 溶液中: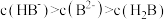 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某二元酸(化学式用H2X表示)在水中的电离方程式是:H2X=H++HX-,HX-⇌H++X2-。25 ℃时,向20.00 mL 0.1 mol·L-1 H2X溶液中滴入0.1 mol·L-1 NaOH溶液,溶液中由水电离出的c水(OH-)的负对数[-lgc水(OH-)]即pOH水与所加NaOH溶液体积的关系如图所示。下列说法中正确的是
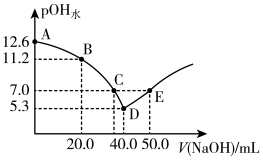

| A.D点溶液中c(OH-)=c(H+)+c(HX-) |
| B.B点c(X2-)>c(H+)-c(OH-) |
| C.水的电离程度:A>B>C>D |
D.图中C点至D点对应溶液中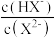 逐渐增大 逐渐增大 |
您最近一年使用:0次