下列与实验相关的叙述正确的是
| A.取一定体积浓硫酸配制稀硫酸,从量筒中倒出浓硫酸后未冲洗量筒,所配溶液浓度偏低 |
B.将 溶液从20℃升温至30℃,溶液中 溶液从20℃升温至30℃,溶液中 减小 减小 |
| C.酸碱滴定时,若加入待测液前用待测液润洗锥形瓶,将导致测定结果偏低 |
D.将 沉淀转入表面皿中,加入足量稀盐酸,加热蒸干得无水 沉淀转入表面皿中,加入足量稀盐酸,加热蒸干得无水 固体 固体 |
更新时间:2024-01-16 21:02:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。若要配制1 mol·L-1的稀硫酸标准溶液,用其滴定某未知浓度的NaOH溶液。下列有关说法错误的是( )
| A.实验中用到的滴定管和容量瓶使用前都需要检漏 |
| B.如果实验需用85 mL的稀硫酸标准溶液,配制时可选用100 mL容量瓶 |
| C.用甲基橙作指示剂,滴定终点时,溶液颜色从红色变为橙色 |
| D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸滴定,会导致测定的NaOH溶液浓度偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
A.若用醋酸溶液和NaOH溶液进行中和反应反应热的测定,则得到的 偏大 偏大 |
| B.酸碱中和滴定实验结束后,俯视滴定管液面读数将导致所测溶液的浓度偏大 |
C.用 计测得等浓度的 计测得等浓度的 溶液的 溶液的 小于 小于 溶液的 溶液的 ,说明酸性: ,说明酸性: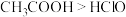 |
D.在一定条件下将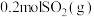 和 和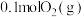 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 ,放出 ,放出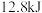 热量,则其热化学方程式为 热量,则其热化学方程式为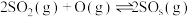  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】草酸晶体(H2C2O4⋅2H2O)用途广泛,易溶于水,其制备及纯度测定实验如下。
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温至60℃左右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝酸与98%硫酸),主要反应为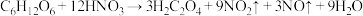 。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体
。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体 。
。
Ⅱ.纯度测定
称取制得的草酸晶体 ,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。根据上述实验,下列说法正确的是
,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。根据上述实验,下列说法正确的是
I.制备
步骤1:将mg淀粉溶于水与少量硫酸加入反应器中,保持85~90℃约30min,然后逐渐降温至60℃左右。
步骤2:控制反应温度在55~60℃条件下,边搅拌边缓慢滴加含有适量催化剂的混酸(65%硝酸与98%硫酸),主要反应为
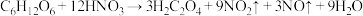 。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体
。严格控制混酸的滴加速度,防止发生副反应。3h左右,冷却,减压过滤得粗品,精制得草酸晶体 。
。Ⅱ.纯度测定
称取制得的草酸晶体
 ,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。根据上述实验,下列说法正确的是
,配成100.00mL溶液。取出20.00mL,用cmol·L-1酸性KMnO4标准溶液滴定,重复2~3次,滴定终点时,平均消耗标准溶液VmL。根据上述实验,下列说法正确的是| A.配制溶液时容量瓶底部残留少量水,会导致所配溶液浓度偏低 |
| B.滴加“混酸”速度过快,不影响草酸晶体的产率 |
| C.锥形瓶用草酸溶液润洗,所测产品纯度会偏低 |
| D.滴定终点读数时仰视,所测产品纯度偏高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,通过下列实验探究FeCl3水解反应[FeCl3(黄色)+3H2O⇌Fe(OH)3(红褐色)+3HCl]的条件。
下列有关说法正确的是
实验序号 | 实验操作 | 实验现象 |
1 | 将FeCl3溶液加热片刻 | 溶液颜色变深 |
2 | 向FeCl3 溶液中通入少量HCl气体 | 溶液颜色变浅 |
3 | 向FeCl3溶液中加入少量(NH4)2SO4固体 | 溶液颜色变浅 |
4 | 向FeCl3溶液中加入少量NaHCO3固体 | 产生红褐色沉淀,溶液中出现大量气泡 |
| A.实验1得到的溶液中有c(Cl-)>c(Fe3+)>c(OH-)>c(H+) |
| B.实验2中FeCl3水解反应的化学平衡常数变小 |
| C.实验3得到的溶液中有3c(Fe3+)+c(H+)=c(NH3·H2O)+c(Cl-)+c(OH-) |
D.实验4中反应的离子方程式为Fe3++ +H2O=Fe(OH)3↓+CO2↑ +H2O=Fe(OH)3↓+CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于物质用途的说法不合理的是
| A.碳酸钠的溶液显碱性,可用作食用碱 |
| B.光洁无锈的铁丝可用于焰色反应实验 |
| C.漂白粉可漂白棉麻等衣物 |
| D.单质钠着火,可以用泡沫灭火器灭火 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验操作或装置能达到目的的是
| A | B | C | D |
 |  |  |  |
| 制NH3 | 收集NO2气体 | ①中有气泡,②中无气泡,说明酸性:醋酸>碳酸>硼酸 | 由CuCl2溶液得到CuCl2固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,实验测得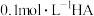 溶液的
溶液的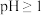 ,下列推理错误的是
,下列推理错误的是
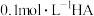 溶液的
溶液的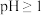 ,下列推理错误的是
,下列推理错误的是| A.NaA可能呈酸性 |
B.HA溶液中 |
C.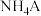 可能呈中性 可能呈中性 |
| D.若稀释HA溶液10倍,pH的数值增大1,则HA是强酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】由下列实验操作及现象所得结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向某溶液中加入70%硫酸后加热,并将气体产物依次通过品红溶液和澄清石灰水,品红溶液褪色,澄清石灰水变浑浊 | 该溶液中含亚硫酸盐 |
| B | 向蛋白质溶液中加入饱和氯化铵溶液,有固体析出 | 蛋白质发生了变性 |
| C | 将变黑的银器浸入盛有NaCl溶液的铝制容器中,银器由黑变白 | 生成了Ag |
| D | 用pH计测CH3COONa溶液和NaNO2溶液的pH,前者大于后者 | Ka(HNO2)>Ka(CH3COOH) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】1mL浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释(溶液体积为V),溶液pH随lgV的变化情况如图所示,则下列说法正确的是( )


| A.XOH是弱碱 |
| B.pH=10的溶液中c(X+):XOH大于X2CO3 |
| C.CO32-的水解常数Kh1约为1.0×10-3.8 |
D.当lgV=2时,升高X2CO3溶液温度,溶液碱性增强且 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在一定条件下,Na2CO3溶液存在水解平衡:CO32- + H2O HCO3-+ OH- ,下列说法正确的是
HCO3-+ OH- ,下列说法正确的是
 HCO3-+ OH- ,下列说法正确的是
HCO3-+ OH- ,下列说法正确的是| A.通入CO2,平衡朝正反应方向移动 |
| B.稀释溶液,水解平衡常数增大 |
C.升高温度,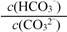 减小 减小 |
| D.加入NaOH固体,溶液pH减小 |
您最近一年使用:0次

 )由大到小的顺序是:①>②>③
)由大到小的顺序是:①>②>③

