碳酸钠溶液显碱性,含 的溶液与碳酸钠溶液反应,产物可能是
的溶液与碳酸钠溶液反应,产物可能是 或
或 。已知:
。已知:
①图1中曲线表示 体系中各含碳粒子的物质的量分数与溶液
体系中各含碳粒子的物质的量分数与溶液 的关系
的关系
②图2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓关系符合
;曲线Ⅱ的离子浓关系符合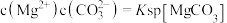 。注:起始
。注:起始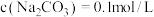 ,不同
,不同 下
下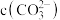 由图1得到。下列说法正确的是
由图1得到。下列说法正确的是
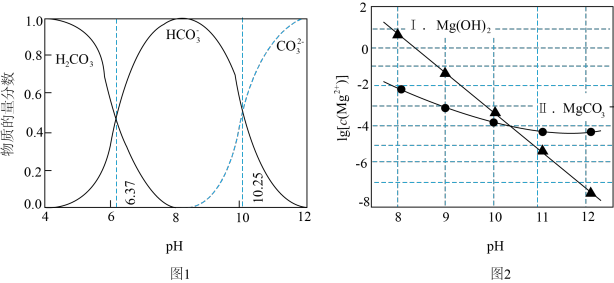
 的溶液与碳酸钠溶液反应,产物可能是
的溶液与碳酸钠溶液反应,产物可能是 或
或 。已知:
。已知:①图1中曲线表示
 体系中各含碳粒子的物质的量分数与溶液
体系中各含碳粒子的物质的量分数与溶液 的关系
的关系②图2中曲线Ⅰ的离子浓度关系符合
 ;曲线Ⅱ的离子浓关系符合
;曲线Ⅱ的离子浓关系符合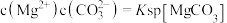 。注:起始
。注:起始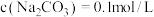 ,不同
,不同 下
下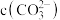 由图1得到。下列说法正确的是
由图1得到。下列说法正确的是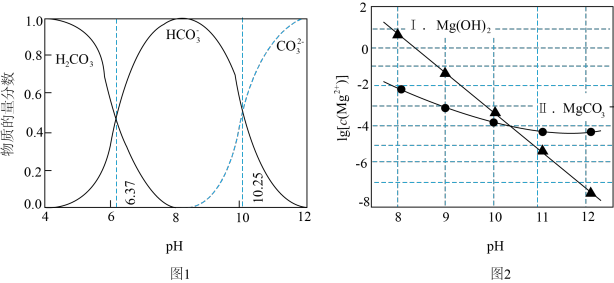
A.常温下, 的第一步水解平衡常数数量级为 的第一步水解平衡常数数量级为 |
B.由图2,初始状态 , ,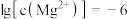 ,有沉淀生成 ,有沉淀生成 |
C.由图2,初始状态 , ,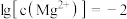 ,平衡后溶液存在 ,平衡后溶液存在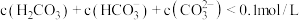 |
D.由图1和图2,初始状态 , ,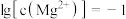 时,发生反应: 时,发生反应: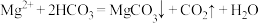 |
2024·江西上饶·一模 查看更多[2]
更新时间:2024-03-14 09:56:32
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】室温下,向柠檬酸(C6H8O7)溶液中滴入NaOH溶液,随着NaOH溶液的加入,所得溶液中C6H8O7、 、
、  和
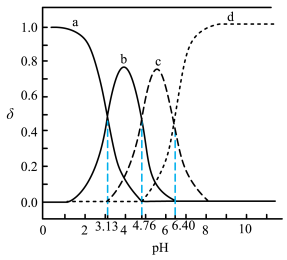
和 的分布系数δ (x)随pH变化曲线如图所示。已知δ(x)=
的分布系数δ (x)随pH变化曲线如图所示。已知δ(x)=  ,下列叙述错误的是
,下列叙述错误的是
 、
、  和
和 的分布系数δ (x)随pH变化曲线如图所示。已知δ(x)=
的分布系数δ (x)随pH变化曲线如图所示。已知δ(x)=  ,下列叙述错误的是
,下列叙述错误的是
| A.C6H8O7的Ka1为10−3.13 |
B.曲线b表示δ( )随pH的变化 )随pH的变化 |
C.在C6H6Na2O7溶液中, ( )>( )>( )>( )>( ) ) |
D.pH大于6时,发生的反应主要为 +OH- = +OH- = +H2O +H2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列有关说法中正确的是
| A.已知25ºC时NH4CN溶液显碱性,则25ºC时的电离常数K(NH3∙H2O) > K(HCN) |
| B.室温时,相同体积、相同pH的盐酸和醋酸溶液中由水电离出的c(H+):盐酸小于醋酸溶液 |
| C.已知Ksp(AgCl)= 1.56×10-10,Ksp(Ag2SO4)= 9.0×10-12,含有Cl-、CrO42-且浓度均为0.010mol∙L-1溶液中逐滴加入0.010mol∙L-1的AgNO3溶液时,CrO42-先产生沉淀 |
| D.常温下pH = 7的CH3COOH 和NaOH混合溶液中,c(Na+) > c(CH3COO-) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是( )
| A.一般情况下,盐类越稀越易水解,所以稀释盐溶液,Kh越大 |
| B.一般情况下,一元弱碱的Kb值越大碱性越弱 |
| C.Kw随着溶液中c(H+)和c(OH-)的改变而改变 |
| D.加热氯化钠溶液,pH值将变小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】常温下,用浓度为 的
的 标准溶液滴定
标准溶液滴定 的
的 溶液,滴定过程中溶液的
溶液,滴定过程中溶液的 随
随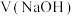 ,
, (含A粒子的物质的量分数)的变化曲线如图所示(忽略溶液体积变化)。已知:
(含A粒子的物质的量分数)的变化曲线如图所示(忽略溶液体积变化)。已知: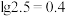 。下列说法错误的是
。下列说法错误的是
 的
的 标准溶液滴定
标准溶液滴定 的
的 溶液,滴定过程中溶液的
溶液,滴定过程中溶液的 随
随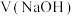 ,
, (含A粒子的物质的量分数)的变化曲线如图所示(忽略溶液体积变化)。已知:
(含A粒子的物质的量分数)的变化曲线如图所示(忽略溶液体积变化)。已知: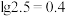 。下列说法错误的是
。下列说法错误的是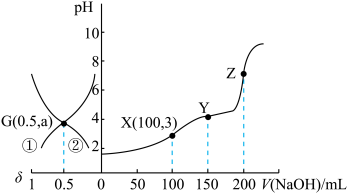
A.曲线①代表 的物质的量分数变化 的物质的量分数变化 |
B.X点: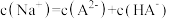 |
C.Y点: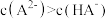 |
| D.a=3.6 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法中,正确的是
| A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH会增大 |
B.AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq) ,往其中加入少量NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小 Ag+(aq)+Cl-(aq) ,往其中加入少量NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小 |
| C.向等浓度KCl、KI的混合溶液中,滴加AgNO3溶液,先产生黄色沉淀,证明此条件下Ksp(AgCl)>Ksp(AgI) |
D.硬水含有较多Ca2+、Mg2+、 、 、 加热煮沸可以完全除去其中的Ca2+、Mg2+ 加热煮沸可以完全除去其中的Ca2+、Mg2+ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】已知:ZnS呈白色,CuS呈黑色;常温下,Ksp(ZnS)=3.0×10-25,Ksp(CuS)=1.0×10-36;pM=-lgc(M2+)。常温下,向10.0mL0.20mol•L-1ZnCl2溶液中逐滴滴加0.10mol•L-1Na2S溶液,溶液中pM与加入Na2S溶液的体积(V)的关系如图所示。下列说法不正确的是( )
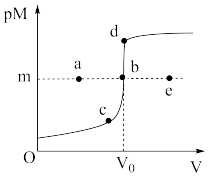

A.V0=20.0mL,m=12.5- lg3 lg3 |
| B.相同实验条件下,若用10.0mL0.20mol•L-1CuCl2溶液代替上述ZnCl2溶液,则反应终点b向d方向移动 |
| C.若c(ZnCl2)=0.10mol•L-1,则反应终点可能为e点 |
| D.向b点浊液中加入0.002molCuCl2固体,白色沉淀变黑色 |
您最近一年使用:0次

 的
的 溶液,下列判断中正确的是
溶液,下列判断中正确的是 增大
增大
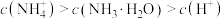
 ,则
,则 的水解百分率为10%
的水解百分率为10%

