常温下,用浓度为 的
的 标准溶液滴定
标准溶液滴定 的
的 溶液,滴定过程中溶液的
溶液,滴定过程中溶液的 随
随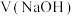 ,
, (含A粒子的物质的量分数)的变化曲线如图所示(忽略溶液体积变化)。已知:
(含A粒子的物质的量分数)的变化曲线如图所示(忽略溶液体积变化)。已知: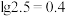 。下列说法错误的是
。下列说法错误的是
 的
的 标准溶液滴定
标准溶液滴定 的
的 溶液,滴定过程中溶液的
溶液,滴定过程中溶液的 随
随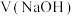 ,
, (含A粒子的物质的量分数)的变化曲线如图所示(忽略溶液体积变化)。已知:
(含A粒子的物质的量分数)的变化曲线如图所示(忽略溶液体积变化)。已知: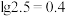 。下列说法错误的是
。下列说法错误的是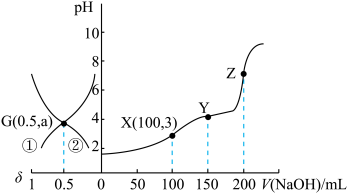
A.曲线①代表 的物质的量分数变化 的物质的量分数变化 |
B.X点: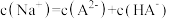 |
C.Y点: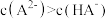 |
| D.a=3.6 |
更新时间:2024-05-21 14:33:52
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列说法不正确的是
| A.将纯水加热,pH减小,仍呈中性 |
| B.中和物质的量相同的氢氧化钠,消耗盐酸和醋酸的物质的量相同 |
| C.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D.在相同温度下,pH相等的盐酸、CH3COOH溶液,c(Cl―)=c(CH3COO―) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在不同温度下,水溶液中 与
与 有如图所示关系。下列说法正确的是
有如图所示关系。下列说法正确的是
 与
与 有如图所示关系。下列说法正确的是
有如图所示关系。下列说法正确的是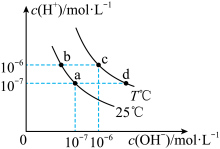
A.c点对应的溶液 ,溶液呈弱酸性 ,溶液呈弱酸性 |
B.b点对应的溶液中可以大量共存: 、 、 、 、 、 、 |
C.若a点表示 和 和 的混合溶液,则该溶液中的离子浓度大小为: 的混合溶液,则该溶液中的离子浓度大小为: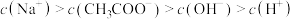 |
D.若d点表示某等浓度、等体积的 和 和 混合溶液,则溶液中的离子浓度存在如下关系: 混合溶液,则溶液中的离子浓度存在如下关系: |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】关于小苏打水溶液的表述正确的是
A.存在的电离平衡为HCO +H2O +H2O H2CO3+OH- H2CO3+OH- |
B.c(Na+)+c(H+)=c(HCO )+c(CO )+c(CO )+c(OH-) )+c(OH-) |
C.c(Na+)=c(HCO )+c(CO )+c(CO )+c(H2CO3) )+c(H2CO3) |
D.HCO 的电离程度大于HCO 的电离程度大于HCO 的水解程度 的水解程度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
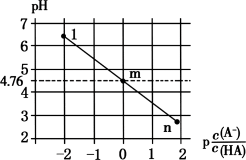
【推荐2】常温下,将NaOH溶液滴加到20mL等浓度的某一元酸(HA)溶液中,测得混合溶液的pH与微粒浓度变化关系如图所示[已知:p =−lg
=−lg ]。下列说法错误的是
]。下列说法错误的是
 =−lg
=−lg ]。下列说法错误的是
]。下列说法错误的是
| A.m点对应的NaOH溶液体积小于10mL |
| B.Ka(HA)的数量级为10−5 |
| C.I点所示溶液中:c(Na+)<c(A-)+c(HA) |
| D.n、m、I三点,n点水的电离程度最大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】亚砷酸(H3AsO3)可用于白血病的治疗。室温下,配制一组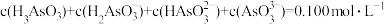 的H3AsO3和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化关系曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是
的H3AsO3和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化关系曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是
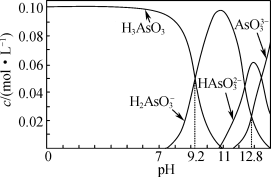
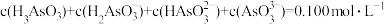 的H3AsO3和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化关系曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是
的H3AsO3和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化关系曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是
| A.H3AsO3的电离常数Ka1的数量级为10-9 |
B.c(Na+)=0.100 mol·L-1的溶液中: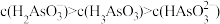 |
C.通常情况下,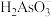 电离程度大于水解程度 电离程度大于水解程度 |
D.pH=12.8的溶液中: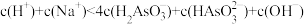 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列叙述中不正确的是
| A.在0.1 mol/L CH3COOH溶液中,c(H+)=c(CH3COO-)+c(OH-) |
| B.常温下将10 mL 0.02 mol/L NaOH溶液与l0 mL0.02 mol/L H2SO4溶液充分混合,若混合后溶液的体积为20 mL,则混合后溶液的pH=2 |
| C.在0.1 mol/L NH4Cl溶液中,c(H+)=c(NH3·H2O)+c(OH-) |
D.在0.1 mol/L Na2CO3溶液中,2c(Na+)=c(H2CO3)+c(CO )+c(HCO )+c(HCO ) ) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列有关电解质溶液的说法正确的是
| A.在蒸馏水中滴加浓H2S04,Kw不变 |
| B.CaC03不易溶于稀硫酸,也不易溶于醋酸 |
| C.NaCI溶液和CH3 COONH4溶液均显中性,两溶液中水的电离程度相同 |
| D.在Na2S稀溶液中,c(H+) ="c(" OH-)-2c(H2S) -c(HS-) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列化学用语正确的是
A.NaHCO3水解的离子方程式:HCO3-+ H2O CO32-+H3O+ CO32-+H3O+ |
B.NH4Cl溶于D2O中:NH4++D2O NH3·HDO+D+ NH3·HDO+D+ |
C.Na2S显碱性原因:S2-+2H2O H2S+2OH- H2S+2OH- |
| D.向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-=A2-+H2O |
您最近一年使用:0次

 数目为0.1 NA
数目为0.1 NA


