Ⅰ.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图1所示。根据图中数据,填写下列空白。

(1)该反应的化学方程式为________________________________________ 。
(2)反应开始至2 min,气体Z的平均反应速率v(Z)=________ 。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________ 倍。
②若此时将容器的体积缩小为原来的 ,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________ (填“放热”或“吸热”)反应。
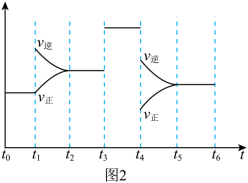
(4)上述反应在t1~t6内反应速率与时间图象如图2所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是 (填字母)。
Ⅱ.已知水溶液中c(H+)和c(OH-)的关系如图所示:
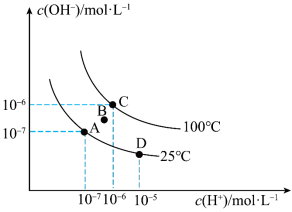
(5)图中B点水的离子积常数___________ 10-12(填“>”、“=”或“<”)。
(6)从A点到D点,可采取的措施是___________ 。
a.升温 b.加入少量盐酸 c.降温 d.加入少量NaOH
(7)100℃时,pH=2的盐酸中水电离产生的H+浓度为___________ mol/L。
(8)25℃时,将pH=12的NaOH溶液与pH=3的H2SO4溶液混合,若所得混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为___________ 。

(1)该反应的化学方程式为
(2)反应开始至2 min,气体Z的平均反应速率v(Z)=
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的
②若此时将容器的体积缩小为原来的
 ,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为(4)上述反应在t1~t6内反应速率与时间图象如图2所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是 (填字母)。

| A.在t1时增大了压强 | B.B.在t3时加入催化剂 |
| C.在t4时降低了温度 | D.t2~t3时X的转化率最高 |
Ⅱ.已知水溶液中c(H+)和c(OH-)的关系如图所示:

(5)图中B点水的离子积常数
(6)从A点到D点,可采取的措施是
a.升温 b.加入少量盐酸 c.降温 d.加入少量NaOH
(7)100℃时,pH=2的盐酸中水电离产生的H+浓度为
(8)25℃时,将pH=12的NaOH溶液与pH=3的H2SO4溶液混合,若所得混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为
更新时间:2024-03-18 15:28:53
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】373K时,某 1L密闭容器中加入1molPCl5发生如下可逆反应: 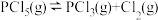 ,其中物质PCl3的物质的量变化如右图所示。
,其中物质PCl3的物质的量变化如右图所示。

(1)前20s内PCl5(g)的平均反应速率为______
(2)373K时该反应的平衡常数的值为_______
(3)若在此平衡体系中再加入1mol的 PCl5,与原平衡比较,新平衡时PCl5的转化率___ (填“增大”或“减小”,下同)。PCl5的平衡浓度_____________ 。
(4)将原平衡升温至473K,重新达平衡时(其他条件不变),PCl3的平衡浓度为 PCl5的3倍,该反应的正反应为(填“放热反应”或 “吸热反应”)________ ,为增大平衡体系中Cl2的物质的量,下列措施正确的是(其它条件相同)_____
a.升高温度 b.扩大容器的体积
c.加入合适的催化剂 d.再充入 PCl3
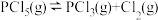 ,其中物质PCl3的物质的量变化如右图所示。
,其中物质PCl3的物质的量变化如右图所示。
(1)前20s内PCl5(g)的平均反应速率为
(2)373K时该反应的平衡常数的值为
(3)若在此平衡体系中再加入1mol的 PCl5,与原平衡比较,新平衡时PCl5的转化率
(4)将原平衡升温至473K,重新达平衡时(其他条件不变),PCl3的平衡浓度为 PCl5的3倍,该反应的正反应为(填“放热反应”或 “吸热反应”)
a.升高温度 b.扩大容器的体积
c.加入合适的催化剂 d.再充入 PCl3
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15 mL 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出上述实验中发生反应的化学方程式:_______________________________ 。
(2)实验结果表明,催化剂的催化效果与________ 有关。
(3)某同学在10 mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是______ 。
Ⅱ.某反应在体积为5 L的恒容密闭容器中进行, 在0~3分钟内各物质的量的变化情况如下图所示(A,B,C均为气体,且A气体有颜色)。
(4)该反应的的化学方程式为________________ 。
(5)反应开始至2分钟时,B的平均反应速率为____ 。
(6)下列措施能使该反应加快的是__ (仅改变一个条件)。
a.降低温度 b.缩小容积 c.使用效率更高更合适的催化剂
(7)能说明该反应已达到平衡状态的是___________ (填序号)。
①单位时间内生成n mol B的同时生成2n mol C
②单位时间内生成n mol B的同时生成2n mol A
③容器内压强不再随时间而发生变化的状态
④用C、A、B的物质的量浓度变化表示的反应速率的比为2:2:1的状态
⑤混合气体的颜色不再改变的状态
⑥混合气体的密度不再改变的状态
⑦v逆(A)=v正(C)
(8)由图求得平衡时A的转化率为__________ 。
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5 min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30 min |
(1)写出上述实验中发生反应的化学方程式:
(2)实验结果表明,催化剂的催化效果与
(3)某同学在10 mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是
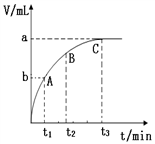
Ⅱ.某反应在体积为5 L的恒容密闭容器中进行, 在0~3分钟内各物质的量的变化情况如下图所示(A,B,C均为气体,且A气体有颜色)。

(4)该反应的的化学方程式为
(5)反应开始至2分钟时,B的平均反应速率为
(6)下列措施能使该反应加快的是
a.降低温度 b.缩小容积 c.使用效率更高更合适的催化剂
(7)能说明该反应已达到平衡状态的是
①单位时间内生成n mol B的同时生成2n mol C
②单位时间内生成n mol B的同时生成2n mol A
③容器内压强不再随时间而发生变化的状态
④用C、A、B的物质的量浓度变化表示的反应速率的比为2:2:1的状态
⑤混合气体的颜色不再改变的状态
⑥混合气体的密度不再改变的状态
⑦v逆(A)=v正(C)
(8)由图求得平衡时A的转化率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】室温下,将 、
、 、KI、
、KI、 溶液及淀粉混合,一段时间后溶液先变为蓝色,后蓝色褪去,且两种现象交替出现。反应分两步进行:反应A:
溶液及淀粉混合,一段时间后溶液先变为蓝色,后蓝色褪去,且两种现象交替出现。反应分两步进行:反应A: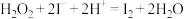 ;反应B:……;总反应为:
;反应B:……;总反应为: 。
。
回答下列问题:
(1)反应B的离子方程式是______ 。 的作用为
的作用为______ 。
(2)小组同学探究溶液颜色第一次变蓝快慢的影响因素,进行下列反应。
①实验Ⅰ中,若2s时 的浓度变为
的浓度变为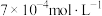 ,则0~2s时
,则0~2s时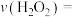
______ 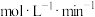
②为探究不同pH对溶液颜色第一次变蓝快慢的影响因素,进行实验Ⅰ和Ⅱ,则
______ ;实验Ⅲ和实验Ⅳ对照实验的目的为______ ;若探究温度对溶液颜色第一次变蓝快慢的影响因素,可选择实验______ 和实验______ (填写“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)。
 、
、 、KI、
、KI、 溶液及淀粉混合,一段时间后溶液先变为蓝色,后蓝色褪去,且两种现象交替出现。反应分两步进行:反应A:
溶液及淀粉混合,一段时间后溶液先变为蓝色,后蓝色褪去,且两种现象交替出现。反应分两步进行:反应A: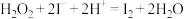 ;反应B:……;总反应为:
;反应B:……;总反应为: 。
。回答下列问题:
(1)反应B的离子方程式是
 的作用为
的作用为(2)小组同学探究溶液颜色第一次变蓝快慢的影响因素,进行下列反应。
试剂用量(mL) 序号 | 温度 | 0.01 | 0.01 | 0.01 | 0.01 |
|
Ⅰ | 25℃ | 5 | 4 | 8 | 3 | 0 |
Ⅱ | 25℃ | 5 | 2 | x | y | z |
Ⅲ | 35℃ | 5 | 4 | 8 | 3 | 0 |
Ⅳ | 35℃ | 3 | 4 | 8 | 3 | 2 |
 的浓度变为
的浓度变为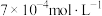 ,则0~2s时
,则0~2s时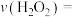
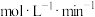
②为探究不同pH对溶液颜色第一次变蓝快慢的影响因素,进行实验Ⅰ和Ⅱ,则

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】十九大报告提出“打赢蓝天保卫战”,对大气污染的防治提出了更高的要求,氮的氧化物(主要是NO和NO2)会形成酸雨、光化学烟雾等,是大气的主要污染物之一。
I.(1)利用NH3还原氮氧化物是目前应用广泛的氮氧化物脱除技术 ,除NO的主要反应是4NH3(g) +6NO(g)⇌5N2(g) +6H2O(l)。脱氮率在不同的催化剂Mn和Cr下与温度的关系如图所示。工业选取的最佳催化剂是_________ (填序号),理由是______ 。

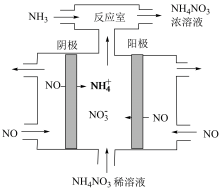
(2)用电解的方法可将NO转化为NH4NO3,变污染气体为氮肥,装置如图所示,阳极的电极反应式是______ 。当阳极消耗11.2 L(标准状况下)气体,阴极消耗相同状况下NO的体积是_____ L。
Ⅱ.研究氮氧化物与悬浮在大气中海盐粒子相互作用时,可发生如下反应:
2NO(g) +Cl2(g) ⇌ 2ClNO(g) ①化学平衡常数为 K1
2NO2(g) + NaCl(s)⇌NaNO3(s) +ClNO(g)②化学平衡常数为 K2
(3)4NO2(g) +2NaCl(s)⇌2NaNO3(s) +2NO(g) +Cl2(g)的平衡常数K=_______ (用K1、K2表示)
(4)在一定条件下恒温恒容的密闭容器中,按一定比例充入NO2和Cl2气体,平衡时ClNO的体积分数φ随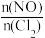 的变化如图所示,当
的变化如图所示,当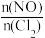 =3时,达到平衡状态时 ClNO的体积分数φ可能是A、B 、C三点中的
=3时,达到平衡状态时 ClNO的体积分数φ可能是A、B 、C三点中的_______ 点。

(5)进一步研究发现,在温度T℃时,反应①的正反应速率v正= kcn(ClNO),测得速率和浓度的关系如表,则n=______ , k=______ ( 只填数值)。
I.(1)利用NH3还原氮氧化物是目前应用广泛的氮氧化物脱除技术 ,除NO的主要反应是4NH3(g) +6NO(g)⇌5N2(g) +6H2O(l)。脱氮率在不同的催化剂Mn和Cr下与温度的关系如图所示。工业选取的最佳催化剂是

(2)用电解的方法可将NO转化为NH4NO3,变污染气体为氮肥,装置如图所示,阳极的电极反应式是

Ⅱ.研究氮氧化物与悬浮在大气中海盐粒子相互作用时,可发生如下反应:
2NO(g) +Cl2(g) ⇌ 2ClNO(g) ①化学平衡常数为 K1
2NO2(g) + NaCl(s)⇌NaNO3(s) +ClNO(g)②化学平衡常数为 K2
(3)4NO2(g) +2NaCl(s)⇌2NaNO3(s) +2NO(g) +Cl2(g)的平衡常数K=
(4)在一定条件下恒温恒容的密闭容器中,按一定比例充入NO2和Cl2气体,平衡时ClNO的体积分数φ随
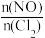 的变化如图所示,当
的变化如图所示,当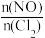 =3时,达到平衡状态时 ClNO的体积分数φ可能是A、B 、C三点中的
=3时,达到平衡状态时 ClNO的体积分数φ可能是A、B 、C三点中的
(5)进一步研究发现,在温度T℃时,反应①的正反应速率v正= kcn(ClNO),测得速率和浓度的关系如表,则n=
| 序号 | c(ClNO)/mol·L-1 | v正/mol·L-1· min-1 |
| ① | 0.20 | 1.8 × 10-8 |
| ② | 0.40 | 7.2× 10-8 |
| ③ | 0.60 | 1.62× 10-7 |
您最近一年使用:0次
【推荐2】造成大气污染的NOx、SO2主要来自于汽车尾气及工厂废气的排放,对其进行处理是我们研究的重要课题。
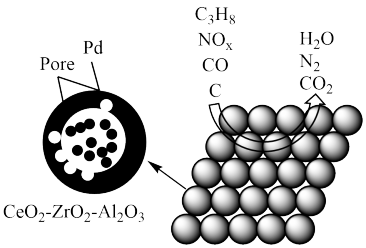
(1)某汽车安装的尾气净化装置工作原理如图所示。下列叙述错误的是_______(填字母)。
(2)已知:2C(s)+O2(g) 2CO(g) ΔH1=-221.0kJ·mol-1
2CO(g) ΔH1=-221.0kJ·mol-1
N2(g)+O2(g) 2NO(g) ΔH2=+180.5kJ·mol-1
2NO(g) ΔH2=+180.5kJ·mol-1
2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH3=-746.0kJ·mol-1
2CO2(g)+N2(g) ΔH3=-746.0kJ·mol-1
则用焦炭还原NO生成无污染气体的热化学方程式为_______ 。
(3)我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S↓。
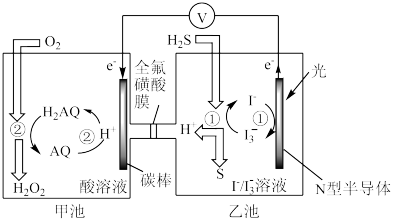
①装置中H+向_______ 池迁移。
②写出乙池溶液中发生反应的离子方程式_______ 。
(4)铈元素(Ce)常见有+3、+4两种价态。NO可以被含Ce4+的溶液吸收,生成含有Ce3+和 的吸收液,反应的离子方程式为
的吸收液,反应的离子方程式为_______ ;现采用电解法将上述吸收液中的 转化为无毒物质,同时再生Ce4+,其原理如图所示。
转化为无毒物质,同时再生Ce4+,其原理如图所示。

①Ce4+从电解槽的_______ (填字母代号)口流出。
②写出阴极的电极反应式:_______ 。
(1)某汽车安装的尾气净化装置工作原理如图所示。下列叙述错误的是_______(填字母)。

| A.Pd-Pore催化剂可提高尾气净化反应的平衡转化率 |
| B.NOx的生成主要是与汽油燃烧不充分有关 |
| C.在此变化过程中,NOx被还原 |
| D.在催化剂的作用下,CO、NOx、C3H8都转化为无毒的物质 |
 2CO(g) ΔH1=-221.0kJ·mol-1
2CO(g) ΔH1=-221.0kJ·mol-1N2(g)+O2(g)
 2NO(g) ΔH2=+180.5kJ·mol-1
2NO(g) ΔH2=+180.5kJ·mol-12NO(g)+2CO(g)
 2CO2(g)+N2(g) ΔH3=-746.0kJ·mol-1
2CO2(g)+N2(g) ΔH3=-746.0kJ·mol-1则用焦炭还原NO生成无污染气体的热化学方程式为
(3)我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S↓。

①装置中H+向
②写出乙池溶液中发生反应的离子方程式
(4)铈元素(Ce)常见有+3、+4两种价态。NO可以被含Ce4+的溶液吸收,生成含有Ce3+和
 的吸收液,反应的离子方程式为
的吸收液,反应的离子方程式为 转化为无毒物质,同时再生Ce4+,其原理如图所示。
转化为无毒物质,同时再生Ce4+,其原理如图所示。
①Ce4+从电解槽的
②写出阴极的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】CO2作为未来的重要碳源,其选择性加氢合成CH3OH一直是研究热点。在CO2加氢合成CH3OH的体系中,同时发生以下反应:
反应iCO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H1<0
CH3OH(g)+H2O(g) ∆H1<0
反应iiCO2(g)+H2(g) CO(g)+H2O(g) ∆H2>0
CO(g)+H2O(g) ∆H2>0
(1)已知化学键键能如表所示
上述反应i的ΔH1=_______ 。
(2)在T°C时,若某容器中只发生反应i,向体积为2L的恒容该容器中充入物质的量之和为4mol的H2和CO2,达到平衡时CO2的转化率与起始时 的关系如图所示:
的关系如图所示:

①当起始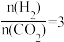 时,反应经过10min达到平衡,若此时CO2的转化率为0.6,则0~10min内平均反应速率v(H2)=
时,反应经过10min达到平衡,若此时CO2的转化率为0.6,则0~10min内平均反应速率v(H2)= _______ 。若此时再向容器中充入CO2(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将_______ (填“增大”“减小”或“不变”)。
②A、B、C、D四点中CH3OH的体积分数最大的点是_______ (填“A”、“B”“C”或“D”点)。
(3)如图所示,向甲乙两个密闭容器分别充入lmolCO2和3molH2,发生反应i,起始温度体积相同(T1℃、2L密闭容器)。达到平衡时,乙的容器容积为1.5L,则该温度下的平衡常数为_______ ,平衡时甲容器中CO2的物质的量_______ 0.5(填“大于、小于、等于、无法确定”),若将甲改为绝热恒容,其它条件不变,平衡时CH3OH的浓度将_______ (增大、减小、不变)。

(4)当起始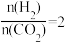 时,维持压强不变,将CO2和H2按一定流速通过反应器,催化剂活性受温度影响变化不大,结合反应i和反应ii,分析温度大于235℃后甲醇的选择性随温度升高而下降的原因是
时,维持压强不变,将CO2和H2按一定流速通过反应器,催化剂活性受温度影响变化不大,结合反应i和反应ii,分析温度大于235℃后甲醇的选择性随温度升高而下降的原因是_______ 。

反应iCO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H1<0
CH3OH(g)+H2O(g) ∆H1<0反应iiCO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2>0
CO(g)+H2O(g) ∆H2>0(1)已知化学键键能如表所示
| 化学键 | C=O | C-O | H-H | C-H | C-C | H-O |
| 键能/kJ·mol-1 | a | b | c | d | e | f |
上述反应i的ΔH1=
(2)在T°C时,若某容器中只发生反应i,向体积为2L的恒容该容器中充入物质的量之和为4mol的H2和CO2,达到平衡时CO2的转化率与起始时
 的关系如图所示:
的关系如图所示:
①当起始
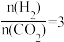 时,反应经过10min达到平衡,若此时CO2的转化率为0.6,则0~10min内平均反应速率v(H2)=
时,反应经过10min达到平衡,若此时CO2的转化率为0.6,则0~10min内平均反应速率v(H2)= ②A、B、C、D四点中CH3OH的体积分数最大的点是
(3)如图所示,向甲乙两个密闭容器分别充入lmolCO2和3molH2,发生反应i,起始温度体积相同(T1℃、2L密闭容器)。达到平衡时,乙的容器容积为1.5L,则该温度下的平衡常数为

(4)当起始
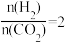 时,维持压强不变,将CO2和H2按一定流速通过反应器,催化剂活性受温度影响变化不大,结合反应i和反应ii,分析温度大于235℃后甲醇的选择性随温度升高而下降的原因是
时,维持压强不变,将CO2和H2按一定流速通过反应器,催化剂活性受温度影响变化不大,结合反应i和反应ii,分析温度大于235℃后甲醇的选择性随温度升高而下降的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)某温度(t℃)时,水的Kw=1×10-12,则该温度_______ (填“>”“<”或“=”)25℃,其理由是_______ 。
(2)该温度下,c(H+)=1×10-7 mol·L-1的溶液呈_______ (填“酸性”“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=_______ mol·L-1。
(3)25 ℃时,0.1 mol·L-1下列物质的溶液:①HCl、②H2SO4、③NaCl、④NaOH 、⑤Ba(OH)2,水电离出的c(H+)由大到小的关系是_______ (填序号)。
(4)25 ℃时,pH=4的盐酸中水的电离程度_______ (填“>”、“<”或“=”)pH=10的Ba(OH)2溶液中水的电离程度。
(1)某温度(t℃)时,水的Kw=1×10-12,则该温度
(2)该温度下,c(H+)=1×10-7 mol·L-1的溶液呈
(3)25 ℃时,0.1 mol·L-1下列物质的溶液:①HCl、②H2SO4、③NaCl、④NaOH 、⑤Ba(OH)2,水电离出的c(H+)由大到小的关系是
(4)25 ℃时,pH=4的盐酸中水的电离程度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】I.A、B、C、D、E 为短周期元素且它们的原子序数依次增大,A 的核外电子总数与其周期数相同;其中D原子的 L电子层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的 L 电子层中未成对电子数与D相同,但有空轨道;D与E同族,请回答下列问题:
(1)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的电子式为____________ ,A分别与 B、C、D形成的共价化合物中既含有极性共价键,又含有非极性共价键的化合物是____________________ (填化学式,任意写出两种)。
(2)B的一种氢化物的相对分子质量是 26,其分子中σ键和π键的数目之比为____________ 。
(3)常温下,相同c(H+)的H2E溶液和硫酸溶液,稀释相同的倍数后的c(H+)前者与后者的关系_________ 。(“大于”、“小于”、“相等”)
Ⅱ.(1)在某温度(T ℃)的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x 与y 关系如图所示。

该温度下,水的离子积为_____ ,T ℃_______ 25℃(填“大于”“小于”或“等于”)。
(2)某温度下,纯水的c(H+)=2.0×10-7mol·L-1。在此温度下,某溶液中由水电离出的c(H+)=4.0×10-13 mol·L-1,则该溶液的pH可能是___________ 。(lg4≈0.6)
(1)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的电子式为
(2)B的一种氢化物的相对分子质量是 26,其分子中σ键和π键的数目之比为
(3)常温下,相同c(H+)的H2E溶液和硫酸溶液,稀释相同的倍数后的c(H+)前者与后者的关系
Ⅱ.(1)在某温度(T ℃)的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x 与y 关系如图所示。

该温度下,水的离子积为
(2)某温度下,纯水的c(H+)=2.0×10-7mol·L-1。在此温度下,某溶液中由水电离出的c(H+)=4.0×10-13 mol·L-1,则该溶液的pH可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)某温度(t℃)时,水的离子积KW=1×10-12mol2•L-2,则该温度_______ 。(填“>”、“<”或“=”)25℃,其理由是_______ 。
(2)该温度下,c水(H+)=1×10﹣7mol•L﹣1的溶液中只存在NaOH溶质,则由H2O电离出来的c水(OH—)=_______ mol•L﹣1。
(3)实验室用Zn和稀硫酸反应制取H2,反应时溶液中水的电离平衡_______ (填“向左”、“向右”或“不”,下同)移动;在新制氯水中加入少量NaCl固体,水的电离平衡_______ 移动。
(4)25℃时,0.1mol•L﹣1的下列4种溶液,水电离出的c水(H+)由大到小的关系是_______ 。(填序号)
①盐酸 ②H2SO4 ③NaOH ④Ba(OH)2
(5)25℃时,pH=4的盐酸中水的电离程度_______ pH=10的Ba(OH)2溶液中水的电离程度(填“大于”、“等于”或 “小于”)。
(1)某温度(t℃)时,水的离子积KW=1×10-12mol2•L-2,则该温度
(2)该温度下,c水(H+)=1×10﹣7mol•L﹣1的溶液中只存在NaOH溶质,则由H2O电离出来的c水(OH—)=
(3)实验室用Zn和稀硫酸反应制取H2,反应时溶液中水的电离平衡
(4)25℃时,0.1mol•L﹣1的下列4种溶液,水电离出的c水(H+)由大到小的关系是
①盐酸 ②H2SO4 ③NaOH ④Ba(OH)2
(5)25℃时,pH=4的盐酸中水的电离程度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】常温下,向100mL0.01mol·L-1的HA溶液中逐滴加入0.02mol·L-1的MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:

(1)由图中信息可知HA为___ 酸(填“强”或“弱”)。
(2)常温下一定浓度的MA稀溶液的pH=a,则a___ 7(填“>”、“<”或“=”),用离子方程式表示其原因为___ ,此时溶液中由水电离出的c(OH-)=___ 。
(3)请写出K点所对应的溶液中离子浓度的大小关系:___ 。
(4)①K点对应的溶液中下列选项正确的是___ 。
A.c(M+)+c(MOH)=2c(A-)
B.2c(H+)+c(M+)=2c(OH-)+c(MOH)
C.c(H+)+c(A-)=c(M+)+c(OH-)
D.c(MOH)>c(M+)
②若K点溶液pH=10,c(MOH)+c(OH-)=___ mol·L-1(列出准确的计算式)。

(1)由图中信息可知HA为
(2)常温下一定浓度的MA稀溶液的pH=a,则a
(3)请写出K点所对应的溶液中离子浓度的大小关系:
(4)①K点对应的溶液中下列选项正确的是
A.c(M+)+c(MOH)=2c(A-)
B.2c(H+)+c(M+)=2c(OH-)+c(MOH)
C.c(H+)+c(A-)=c(M+)+c(OH-)
D.c(MOH)>c(M+)
②若K点溶液pH=10,c(MOH)+c(OH-)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.CH3COOH为常见的弱酸,在工业生产和生活中有广泛应用。
(1)中和100 mL pH=3的CH3COOH溶液和1 L pH=4的CH3COOH溶液,需要等物质的量浓度的NaOH溶液的体积分别为V1和V2,则V1____ (填“>”、“=”或“<”)V2。
(2)常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL某未知浓度的CH3COOH溶液,滴定曲线如图所示。其中A点所示溶液中c(CH3COO-)=2c(CH3COOH),C点所示溶液中存在:c(CH3COO-)+c(CH3COOH)=c(Na+)。则CH3COOH的电离常数Ka=____ ,CH3COOH的实际浓度为_____ 。

Ⅱ.将0.23 mol二氧化硫气体和0.11 mol氧气混合放入容积为1 L的恒容密闭容器中,发生反应生成三氧化硫气体,反应达到平衡时,得到0.12 mol三氧化硫气体。若温度保持不变,向其中再加入0.50 mol氧气后重新达到平衡,则氧气的转化率____ (填“增大”、“不变”或“减小”,下同),混合气体的密度____ ,该温度下反应的平衡常数K____ ;若温度保持不变,向其中再加入0.12 mol氦气后重新达到平衡,则二氧化硫的转化率___ 。
Ⅲ.向BaCl2溶液中先后滴加AgNO3溶液和KBr溶液,当两种沉淀共存时, =
=______ 。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=1.8×10-10]
(1)中和100 mL pH=3的CH3COOH溶液和1 L pH=4的CH3COOH溶液,需要等物质的量浓度的NaOH溶液的体积分别为V1和V2,则V1
(2)常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL某未知浓度的CH3COOH溶液,滴定曲线如图所示。其中A点所示溶液中c(CH3COO-)=2c(CH3COOH),C点所示溶液中存在:c(CH3COO-)+c(CH3COOH)=c(Na+)。则CH3COOH的电离常数Ka=

Ⅱ.将0.23 mol二氧化硫气体和0.11 mol氧气混合放入容积为1 L的恒容密闭容器中,发生反应生成三氧化硫气体,反应达到平衡时,得到0.12 mol三氧化硫气体。若温度保持不变,向其中再加入0.50 mol氧气后重新达到平衡,则氧气的转化率
Ⅲ.向BaCl2溶液中先后滴加AgNO3溶液和KBr溶液,当两种沉淀共存时,
 =
=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)①常温下,pH=3的盐酸和pH=11的氢氧化钡等体积混合,溶液的pH=____ 。
②常温下pH=3的盐酸和pH=6的盐酸等体积混合(不考虑混合时溶液的体积变化),溶液的pH=____ 。(lg2=0.3)
(2)在某温度下,H2O的离子积常数为1×10-13,则该温度下:
①某溶液中的H+浓度为1×10-7mol/L,则该溶液呈___ 性。
②99mLpH=1的H2SO4溶液与101mLpH=12的KOH溶液混合后(不考虑混合时溶液的体积变化),溶液的pH=___ 。
(3)今有①CH3COOH、②HCl、③H2SO4三种溶液,用序号回答下列问题:
a.当它们pH相同时,其物质的量浓度由大到小排列是___ 。
b.当它们的物质的量浓度相同时,其pH由大到小排列是___ 。
c.中和同一烧碱溶液,需同浓度的三种酸溶液的体积关系为___ 。(用等式表示)
d.体积和浓度均相同的①、②、③三溶液,分别与同浓度的烧碱溶液恰好完全反应,反应需烧碱溶液的体积关系为___ 。(用等式表示)
②常温下pH=3的盐酸和pH=6的盐酸等体积混合(不考虑混合时溶液的体积变化),溶液的pH=
(2)在某温度下,H2O的离子积常数为1×10-13,则该温度下:
①某溶液中的H+浓度为1×10-7mol/L,则该溶液呈
②99mLpH=1的H2SO4溶液与101mLpH=12的KOH溶液混合后(不考虑混合时溶液的体积变化),溶液的pH=
(3)今有①CH3COOH、②HCl、③H2SO4三种溶液,用序号回答下列问题:
a.当它们pH相同时,其物质的量浓度由大到小排列是
b.当它们的物质的量浓度相同时,其pH由大到小排列是
c.中和同一烧碱溶液,需同浓度的三种酸溶液的体积关系为
d.体积和浓度均相同的①、②、③三溶液,分别与同浓度的烧碱溶液恰好完全反应,反应需烧碱溶液的体积关系为
您最近一年使用:0次





