(1)①常温下,pH=3的盐酸和pH=11的氢氧化钡等体积混合,溶液的pH=____ 。
②常温下pH=3的盐酸和pH=6的盐酸等体积混合(不考虑混合时溶液的体积变化),溶液的pH=____ 。(lg2=0.3)
(2)在某温度下,H2O的离子积常数为1×10-13,则该温度下:
①某溶液中的H+浓度为1×10-7mol/L,则该溶液呈___ 性。
②99mLpH=1的H2SO4溶液与101mLpH=12的KOH溶液混合后(不考虑混合时溶液的体积变化),溶液的pH=___ 。
(3)今有①CH3COOH、②HCl、③H2SO4三种溶液,用序号回答下列问题:
a.当它们pH相同时,其物质的量浓度由大到小排列是___ 。
b.当它们的物质的量浓度相同时,其pH由大到小排列是___ 。
c.中和同一烧碱溶液,需同浓度的三种酸溶液的体积关系为___ 。(用等式表示)
d.体积和浓度均相同的①、②、③三溶液,分别与同浓度的烧碱溶液恰好完全反应,反应需烧碱溶液的体积关系为___ 。(用等式表示)
②常温下pH=3的盐酸和pH=6的盐酸等体积混合(不考虑混合时溶液的体积变化),溶液的pH=
(2)在某温度下,H2O的离子积常数为1×10-13,则该温度下:
①某溶液中的H+浓度为1×10-7mol/L,则该溶液呈
②99mLpH=1的H2SO4溶液与101mLpH=12的KOH溶液混合后(不考虑混合时溶液的体积变化),溶液的pH=
(3)今有①CH3COOH、②HCl、③H2SO4三种溶液,用序号回答下列问题:
a.当它们pH相同时,其物质的量浓度由大到小排列是
b.当它们的物质的量浓度相同时,其pH由大到小排列是
c.中和同一烧碱溶液,需同浓度的三种酸溶液的体积关系为
d.体积和浓度均相同的①、②、③三溶液,分别与同浓度的烧碱溶液恰好完全反应,反应需烧碱溶液的体积关系为
更新时间:2019-11-14 08:17:53
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。回答下列各小题。
I.已知在25℃时,次氯酸、碳酸和亚硫酸的电离平衡常数分别为:
HClO Ka=4.7×10-8
H2CO3 Ka1=4.3×10-7 Ka2=5.6×10-11
H2SO3 Ka1=1.5×10-2 Ka2=1.0×10-7
(1)相同浓度的ClO-、 、
、 、
、 结合H+的能力最强的为
结合H+的能力最强的为_______ 。(填离子符号)
II.水在25℃和95℃时电离平衡曲线如图。
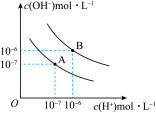
(2)已知在25℃时,将pH=12的NaOH溶液与pH=2的H2SO4溶液均升温至35℃,两溶液pH变化分别为_______(填字母)。
(3)在曲线B所对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=6,则NaOH溶液与H2SO4溶液的体积比为_______ 。
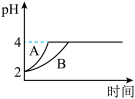
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量Zn粒,反应过程中两溶液pH变化如图。图中表示醋酸溶液中pH变化曲线_______ (填“A”或“B”);设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1_______ m2。 (选填“<”、“=”、“>”)
(5)25 C时,在体积为2 L的密闭容器中,气态物质A、B、C的物质的量n随时间t的变化如图所示。
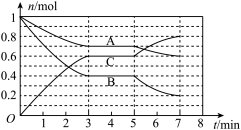
根据图1数据。写出该反应的化学方程式:_______ ;在5~7min内,若K值不变,则此处曲线变化的原因是_______ 。
I.已知在25℃时,次氯酸、碳酸和亚硫酸的电离平衡常数分别为:
HClO Ka=4.7×10-8
H2CO3 Ka1=4.3×10-7 Ka2=5.6×10-11
H2SO3 Ka1=1.5×10-2 Ka2=1.0×10-7
(1)相同浓度的ClO-、
 、
、 、
、 结合H+的能力最强的为
结合H+的能力最强的为II.水在25℃和95℃时电离平衡曲线如图。

(2)已知在25℃时,将pH=12的NaOH溶液与pH=2的H2SO4溶液均升温至35℃,两溶液pH变化分别为_______(填字母)。
| A.增加、减小 | B.增加、增加 | C.减小、不变 | D.不变、减小 |
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量Zn粒,反应过程中两溶液pH变化如图。图中表示醋酸溶液中pH变化曲线

(5)25 C时,在体积为2 L的密闭容器中,气态物质A、B、C的物质的量n随时间t的变化如图所示。

根据图1数据。写出该反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】25℃时, 的电离常数
的电离常数 。常温下,往25mL氢氧化钠标准溶液中逐滴加入
。常温下,往25mL氢氧化钠标准溶液中逐滴加入 的
的 溶液,pH变化曲线如图所示:
溶液,pH变化曲线如图所示:
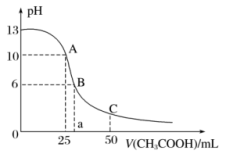
(1)该氢氧化钠溶液的物质的量浓度为_______ 。
(2)A点对应的横坐标为25mL,请用离子方程式解释A点所示的溶液显碱性的原因:_______ 。
(3)A点所示的溶液中各离子浓度由大到小的排列顺序是:_______ 。
(4)电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
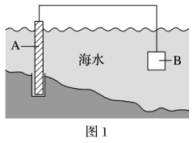
图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_______ (填字母)
a.碳棒 b.锌板 c.铜板
(5)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
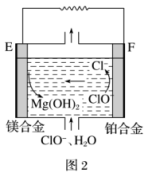
E为该燃料电池的_______ (填“正”或“负”)极。F电极上的电极反应式为_______ 。
 的电离常数
的电离常数 。常温下,往25mL氢氧化钠标准溶液中逐滴加入
。常温下,往25mL氢氧化钠标准溶液中逐滴加入 的
的 溶液,pH变化曲线如图所示:
溶液,pH变化曲线如图所示:
(1)该氢氧化钠溶液的物质的量浓度为
(2)A点对应的横坐标为25mL,请用离子方程式解释A点所示的溶液显碱性的原因:
(3)A点所示的溶液中各离子浓度由大到小的排列顺序是:
(4)电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择
a.碳棒 b.锌板 c.铜板
(5)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。

E为该燃料电池的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】(1)汽车尾气是城市空气污染的一个重要因素,一种CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,在高温熔融状态下能传导O2-(过程中无气体产生),则负极的反应式为___ 。
(2)以上述电池为电源,通过导线连接成图一电解池。
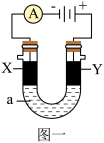
①若X、Y为石墨,a为2L0.1mol/LKCl溶液,写出电解总反应的离子方程式___ 。
②若X、Y分别为铜、银,a为1L0.2mol/LAgNO3溶液,写出Y电极反应式___ 。
(3)室温时,按上述(2)①电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图二(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。
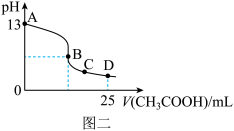
①结合图二计算,上述电解过程中消耗一氧化碳的质量为___ g。
②若图二的B点pH=7,则滴定终点在___ 区间(填“AB”、“BC”或“CD”)。
(2)以上述电池为电源,通过导线连接成图一电解池。

①若X、Y为石墨,a为2L0.1mol/LKCl溶液,写出电解总反应的离子方程式
②若X、Y分别为铜、银,a为1L0.2mol/LAgNO3溶液,写出Y电极反应式
(3)室温时,按上述(2)①电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图二(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。

①结合图二计算,上述电解过程中消耗一氧化碳的质量为
②若图二的B点pH=7,则滴定终点在
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】水溶液中的行为是中学化学的重要内容。
(1)在某温度(T℃)的水溶液中,c(H+)=10xmol•L-1,c(OH-)=10ymol•L-1,x与y关系如图所示。
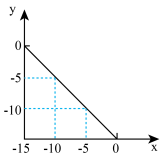
将此温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为______ (已知lg5=0.7)
(2)已知部分弱酸的电离常数如表:
①0.1mol•L-1NaCN溶液和0.1mol•L-1NaHCO3溶液中,c(CN-)______ c(HCO )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
②常温下,pH相同的三种溶液:a.CH3COONa、b.NaCN、c.Na2CO3,其物质的量浓度由大到小的顺序是______ 。(填序号)
(3)三氯化铁是一种重要的化合物,可以用来腐蚀电路板。
①25℃时,FeCl3溶液显酸性,原因是(用离子方程式表示)______ ,把FeCl3溶液蒸干灼烧得到的主要产物是______ ;
②某腐蚀废液中含有0.5mol•L-1Fe3+和0.26mol•L-1Cu2+,欲使Fe3+完全沉淀【c(Fe3+)≤4×10-5mol•L-1】而Cu2+不沉淀,则需控制溶液pH的范围为______ 。【KspCu(OH)2=2.6×10-19;KspFe(OH)3=4×10-38】
(1)在某温度(T℃)的水溶液中,c(H+)=10xmol•L-1,c(OH-)=10ymol•L-1,x与y关系如图所示。

将此温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为
(2)已知部分弱酸的电离常数如表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka=1.8×10-5 | Ka=4.3×10-10 | Ka1=5.0×10-7 Ka2=5.6×10-11 |
 )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。②常温下,pH相同的三种溶液:a.CH3COONa、b.NaCN、c.Na2CO3,其物质的量浓度由大到小的顺序是
(3)三氯化铁是一种重要的化合物,可以用来腐蚀电路板。
①25℃时,FeCl3溶液显酸性,原因是(用离子方程式表示)
②某腐蚀废液中含有0.5mol•L-1Fe3+和0.26mol•L-1Cu2+,欲使Fe3+完全沉淀【c(Fe3+)≤4×10-5mol•L-1】而Cu2+不沉淀,则需控制溶液pH的范围为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】在水的电离平衡中,c(H+)和c(OH-)的关系如下图所示:

(1)A点水的离子积为1×10-14,B点水的离子积为__________ 。造成水的离子积变化的原因是__________________________________________________ 。
(2)25℃时,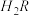 在水溶液中的电离方程式为:
在水溶液中的电离方程式为:
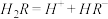 ,
,

 。
。
① 0.1 mol/L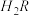 溶液的pH
溶液的pH________ 1(填“>”、“<”或“=”)。
②在0.1 mol/L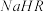 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是:______________ 。
(3)100℃时,0.01 mol/L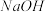 溶液的pH =
溶液的pH =____________ 。
(4)100℃时,将pH =8的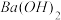 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则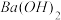 溶液与盐酸的体积比为
溶液与盐酸的体积比为___________ 。

(1)A点水的离子积为1×10-14,B点水的离子积为
(2)25℃时,
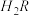 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: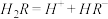 ,
,

 。
。① 0.1 mol/L
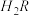 溶液的pH
溶液的pH②在0.1 mol/L
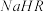 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是:(3)100℃时,0.01 mol/L
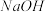 溶液的pH =
溶液的pH =(4)100℃时,将pH =8的
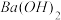 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则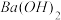 溶液与盐酸的体积比为
溶液与盐酸的体积比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】Ⅰ:现有以下几种物质①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸钠、⑥亚硫酸氢钠、⑦氨水。请回答下列问题:
(1)以上物质属于弱电解质的是______ (填序号);
(2)常温下④的溶液pH______ 7(填>“<”或“=”),原因______ (用离子方程式表示);
(3)⑥的水溶液中呈酸性,原因是______ 。
(4)常温下,将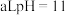 的
的 溶液与
溶液与 的
的 溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的
溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的 ,则
,则
______ 。
(5)已知:
a.常温下,醋酸和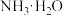 的电离平衡常数均为
的电离平衡常数均为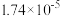 ;
;
b.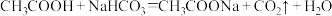
则 溶液呈
溶液呈______ 性(填“酸”、“碱”或“中”,下同), 溶液呈
溶液呈______ 性。
(6)对于醋酸溶液和醋酸钠溶液的下列说法正确的是______;
(1)以上物质属于弱电解质的是
(2)常温下④的溶液pH
(3)⑥的水溶液中呈酸性,原因是
(4)常温下,将
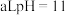 的
的 溶液与
溶液与 的
的 溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的
溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的 ,则
,则
(5)已知:
a.常温下,醋酸和
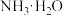 的电离平衡常数均为
的电离平衡常数均为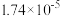 ;
;b.
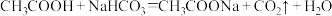
则
 溶液呈
溶液呈 溶液呈
溶液呈(6)对于醋酸溶液和醋酸钠溶液的下列说法正确的是______;
| A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小。 |
| B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解。 |
| C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离。 |
| D.常温下,醋酸和醋酸钠等体积等浓度混合,溶液呈碱性。 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】盐碱地是土壤表层集聚过多盐碱成分,对农作物有害的土地。回答下列问题:
(1)盐碱地(含较多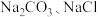 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为___________ (用离子方程式说明);已知 时,
时, 的
的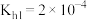 ,则当
,则当 溶液中
溶液中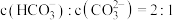 时,溶液的
时,溶液的
___________ 。
(2) 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液___________ (填“喷在叶片上”或“随水灌入土壤中”),主要理由是___________ 。
(3)已知:常温下,碳酸的电离平衡常数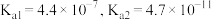 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加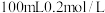 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
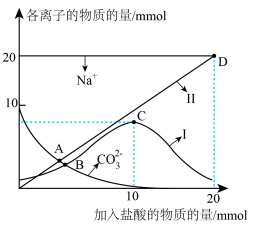
①曲线Ⅰ代表的离子是_______ 。
②A、B两点水的电离程度大小为A_______ B。
③根据上图,下列有关说法不正确的是_______ 。
a.滴加至 点时,
点时,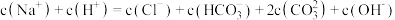
b.滴加至 点时,
点时,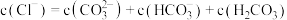
c.滴加至 点时,溶液
点时,溶液
④已知 电离平衡常数约为
电离平衡常数约为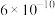 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱_______ 。
⑤证明 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是_______ 。
(1)盐碱地(含较多
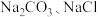 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为 时,
时, 的
的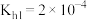 ,则当
,则当 溶液中
溶液中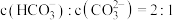 时,溶液的
时,溶液的
(2)
 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液(3)已知:常温下,碳酸的电离平衡常数
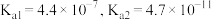 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加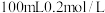 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
①曲线Ⅰ代表的离子是
②A、B两点水的电离程度大小为A
③根据上图,下列有关说法不正确的是
a.滴加至
 点时,
点时,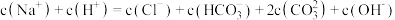
b.滴加至
 点时,
点时,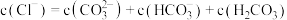
c.滴加至
 点时,溶液
点时,溶液
④已知
 电离平衡常数约为
电离平衡常数约为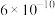 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱⑤证明
 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】亚磷酸(H3PO3)是重要的化工原料,可作尼龙增白剂、农药中间体等。
(1)亚磷酸溶液与硝酸银溶液混合生成黑色的银和一氧化氮气体,反应的化学方程式为________ 。
(2)亚磷酸为二元弱酸。
已知:
① H3PO3(aq)+NaOH(aq) NaH2PO3(aq)+H2O(l)△H=-akJ/mol
NaH2PO3(aq)+H2O(l)△H=-akJ/mol
②HCl(aq)+NaOH(aq) NaCl(aq)H2O(l)△H=-bkJ/mol
NaCl(aq)H2O(l)△H=-bkJ/mol
求H3PO3(aq) H+(aq)+H2PO3-(aq) △H=
H+(aq)+H2PO3-(aq) △H= ______
(3)25℃时,H3PO3电离常数Ka1=8.4×10-3,则NaH2PO3水解常数Kh=_____ (结果保留两位有效数字);Na2HPO3为________ (填“正盐”或“酸式盐”),其溶液显_____ (填“酸性”、“中性”、“碱性”或“无法判断”);浓度均为0.1mol/L的Na2HPO3和NaOH的混合液,加水稀释10倍后的溶液中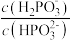 将
将_______ (填“增大”、“不变”或“减小”)。
(4)亚磷酸可用电解Na2HPO3溶液来制得,装置如图所示:
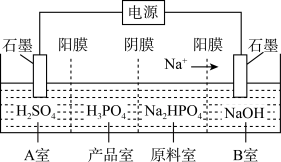
①A室的电极反应式为_________________ ;
②产品室中反应的离子方程式为____________ 。
(1)亚磷酸溶液与硝酸银溶液混合生成黑色的银和一氧化氮气体,反应的化学方程式为
(2)亚磷酸为二元弱酸。
已知:
① H3PO3(aq)+NaOH(aq)
 NaH2PO3(aq)+H2O(l)△H=-akJ/mol
NaH2PO3(aq)+H2O(l)△H=-akJ/mol②HCl(aq)+NaOH(aq)
 NaCl(aq)H2O(l)△H=-bkJ/mol
NaCl(aq)H2O(l)△H=-bkJ/mol求H3PO3(aq)
 H+(aq)+H2PO3-(aq) △H=
H+(aq)+H2PO3-(aq) △H= (3)25℃时,H3PO3电离常数Ka1=8.4×10-3,则NaH2PO3水解常数Kh=
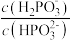 将
将(4)亚磷酸可用电解Na2HPO3溶液来制得,装置如图所示:

①A室的电极反应式为
②产品室中反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】已知 25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)表中三种酸酸性最强的是__________ 。
(2)常温下,0.1 mol L1 CH3COOH 溶液加水稀释过程中,下列表达式的数据变大的是__________ (填字母)。
A.c(H+) B.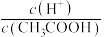 C.
C. D.
D.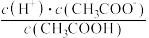
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:__________ 。
(4)25℃时,将a mol L1 醋酸与b mol L1 氢氧化钠等体积混合,反应后溶液恰好显中性,这时钠离子浓度与醋酸根离子浓度相等,用 a、b 表示醋酸的电离平衡常数为__________ 。
化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7、Ka2=5.6×10-11 | Ka=3.0×10-8 |
(2)常温下,0.1 mol L1 CH3COOH 溶液加水稀释过程中,下列表达式的数据变大的是
A.c(H+) B.
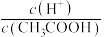 C.
C. D.
D.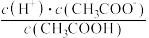
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将a mol L1 醋酸与b mol L1 氢氧化钠等体积混合,反应后溶液恰好显中性,这时钠离子浓度与醋酸根离子浓度相等,用 a、b 表示醋酸的电离平衡常数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某小组为证明同温同压下,同浓度,同体积的酸性不同的两种二元酸与足量镁带反应时生成H2量相同而反应速率不同,装置如图。主要步骤如下:

①配制浓度为0.5mol/L的硫酸和草酸溶液;
②用____量取10.00mL0.5mol/L的硫酸和草酸溶液分别加入两锥形瓶中;
③分别取去表面氧化膜的镁带系于铜丝末端;
④检查装置气密性,乙中装满水,按图连接好装置;
⑤将铜丝下移,使足量镁带浸如酸中(铜丝不与酸接触)至完全反应,同时需要记录反应时间;
⑥反应结束时,读取量筒内水体积ymL。
将以上步骤补充完整并回答下列问题
(1)②中仪器是______ 。
(2)用草酸晶体(H2C2O4∙2H2O)配制80mL,c(H2C2O4)=0.5mol/L的草酸溶液,需要草酸晶体的质量为_____ g。主要仪器有________ 、_______ 、烧杯、玻璃棒、托盘天平等
(3)读取量筒内水体积时,若丙中的液面高于乙中液面,使乙、丙中液面相平的操作方法是_______ 。
(4)若铜丝与酸接触将会使测得的反应速率_____ (填“偏大”“偏小”);原因是________ 。
(5)简述速率不等的原因_________ 。

①配制浓度为0.5mol/L的硫酸和草酸溶液;
②用____量取10.00mL0.5mol/L的硫酸和草酸溶液分别加入两锥形瓶中;
③分别取去表面氧化膜的镁带系于铜丝末端;
④检查装置气密性,乙中装满水,按图连接好装置;
⑤将铜丝下移,使足量镁带浸如酸中(铜丝不与酸接触)至完全反应,同时需要记录反应时间;
⑥反应结束时,读取量筒内水体积ymL。
将以上步骤补充完整并回答下列问题
(1)②中仪器是
(2)用草酸晶体(H2C2O4∙2H2O)配制80mL,c(H2C2O4)=0.5mol/L的草酸溶液,需要草酸晶体的质量为
(3)读取量筒内水体积时,若丙中的液面高于乙中液面,使乙、丙中液面相平的操作方法是
(4)若铜丝与酸接触将会使测得的反应速率
(5)简述速率不等的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】为了证明醋酸是弱电解质,甲、乙、丙、丁四人分别选用下列试剂进行实验:0.1 mol·L-1醋酸溶液、0.1 mol·L-1盐酸、pH=3的盐酸、pH=3的醋酸、CH3COONa晶体、NaCl晶体、CH3COONH4晶体、蒸馏水、锌粒、pH试纸、酚酞、NaOH溶液等。
(1)甲取出10 mL 0.1 mol·L-1的醋酸溶液,用pH试纸测出其pH=a,确定醋酸是弱电解质,则a应该满足的关系是________ ,理由是________ 。
(2)乙分别取pH=3的醋酸和盐酸各1 mL,分别用蒸馏水稀释到100 mL,然后用pH试纸分别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是___________ 。
(3)丙分别取pH=3的盐酸和醋酸各10 mL,然后加入质量相同的锌粒,醋酸放出H2的平均速率快,则认定醋酸是弱电解质,你认为这一方法正确吗?_______ ,请说明理由:_________ 。
(1)甲取出10 mL 0.1 mol·L-1的醋酸溶液,用pH试纸测出其pH=a,确定醋酸是弱电解质,则a应该满足的关系是
(2)乙分别取pH=3的醋酸和盐酸各1 mL,分别用蒸馏水稀释到100 mL,然后用pH试纸分别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是
(3)丙分别取pH=3的盐酸和醋酸各10 mL,然后加入质量相同的锌粒,醋酸放出H2的平均速率快,则认定醋酸是弱电解质,你认为这一方法正确吗?
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为______________________ 。
(2)常温下0.1 mol·L-1的CH3COOH溶液,若升高温度,上述4种表达式的数据增大的是______ 。
A.c(H+) B.c(H+)/c(CH3COOH) C. c(H+)·c(OH-) D.c(CH3COO-)·c(H+)/c(CH3COOH)
(3)取0.10mol CH3COOH (冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示:比较a、b点的相关性质(填“>”“<”或“=”):
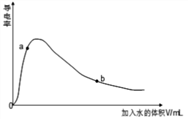
n(H+)∶a_____ b;c(CH3COO-)∶a_____ b;完全中和时消耗NaOH的物质的量∶a_____ b;
(4)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是__________ (填写序号)
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④A中有锌剩余
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为
(2)常温下0.1 mol·L-1的CH3COOH溶液,若升高温度,上述4种表达式的数据增大的是
A.c(H+) B.c(H+)/c(CH3COOH) C. c(H+)·c(OH-) D.c(CH3COO-)·c(H+)/c(CH3COOH)
(3)取0.10mol CH3COOH (冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示:比较a、b点的相关性质(填“>”“<”或“=”):

n(H+)∶a
(4)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④A中有锌剩余
您最近一年使用:0次



