室温下 溶液中各含碳粒子的物质的量分数与pH的关系如图1所示。向
溶液中各含碳粒子的物质的量分数与pH的关系如图1所示。向 、
、 混合溶液X中滴加
混合溶液X中滴加 溶液,所得溶液中
溶液,所得溶液中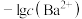 与
与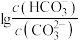 的关系如图2所示。下列说法不正确的是
的关系如图2所示。下列说法不正确的是
 溶液中各含碳粒子的物质的量分数与pH的关系如图1所示。向
溶液中各含碳粒子的物质的量分数与pH的关系如图1所示。向 、
、 混合溶液X中滴加
混合溶液X中滴加 溶液,所得溶液中
溶液,所得溶液中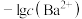 与
与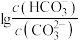 的关系如图2所示。下列说法不正确的是
的关系如图2所示。下列说法不正确的是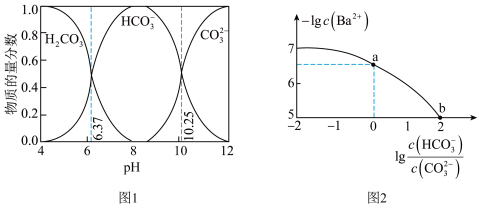
| A.b点对应溶液的pH为8.25 |
B.混合溶液X中一定存在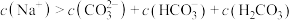 |
C.a对应的溶液中存在: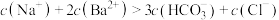 |
D.a→b的过程中,溶液中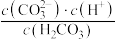 一直增大 一直增大 |
更新时间:2024-04-01 09:10:52
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】常温时,下列溶液中微粒的物质的量浓度关系正确的是
A.0.1mol/L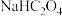 与0.1mol/L HCl等体积混合: 与0.1mol/L HCl等体积混合: |
B.0.1mol/L的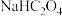 溶液,其pH=4,则 溶液,其pH=4,则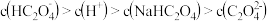 |
C.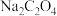 溶液: 溶液: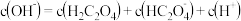 |
D.将0.1mol/L的 溶液和0.1mol/L 溶液和0.1mol/L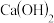 溶液等体积混合后,则: 溶液等体积混合后,则: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】工业生产中常通过生成氟化物沉淀除去Ca2+、Mg2+,为探究溶液酸碱性对沉淀的影响,用盐酸分别调节CaF2和MgF2浊液的pH,在不同pH条件下,测得体系中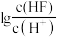 与
与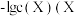 为
为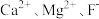 )的变化关系如图所示。已知
)的变化关系如图所示。已知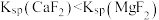 ,下列说法正确的是
,下列说法正确的是
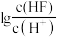 与
与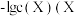 为
为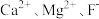 )的变化关系如图所示。已知
)的变化关系如图所示。已知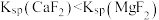 ,下列说法正确的是
,下列说法正确的是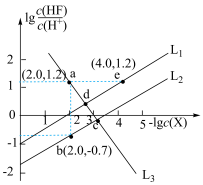
A. 表示 表示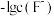 与 与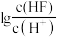 的变化曲线 的变化曲线 |
B.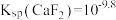 |
C.c点溶液中: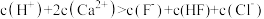 (不考虑水的电离因素) (不考虑水的电离因素) |
D.e点浊液中加入 固体,阳离子 固体,阳离子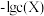 沿 沿 向d点移 向d点移 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】以酚酞为指示剂,用0.1000mol·L-1的NaOH溶液滴定20mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积V(NaOH)的变化关系如下图所示,[比如
随滴加NaOH溶液体积V(NaOH)的变化关系如下图所示,[比如 的分布系数:
的分布系数: ],下列叙述错误的是
],下列叙述错误的是
 随滴加NaOH溶液体积V(NaOH)的变化关系如下图所示,[比如
随滴加NaOH溶液体积V(NaOH)的变化关系如下图所示,[比如 的分布系数:
的分布系数: ],下列叙述错误的是
],下列叙述错误的是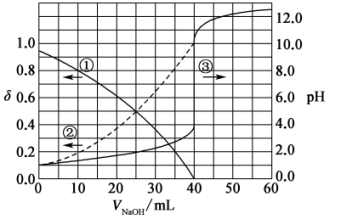
A. 的电离常数 的电离常数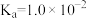 |
B. 溶液的浓度为 溶液的浓度为 |
C.曲线①代表 ,曲线②代表 ,曲线②代表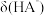 |
D.由图可知 的第一步电离方程式为 的第一步电离方程式为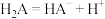 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
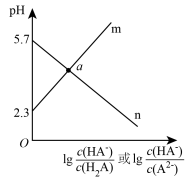
【推荐2】常温下,向二元弱酸 溶液中滴加
溶液中滴加 溶液,测得混合溶液的pH与离子浓度变化的关系如图所示,下列说法错误的是
溶液,测得混合溶液的pH与离子浓度变化的关系如图所示,下列说法错误的是
 溶液中滴加
溶液中滴加 溶液,测得混合溶液的pH与离子浓度变化的关系如图所示,下列说法错误的是
溶液,测得混合溶液的pH与离子浓度变化的关系如图所示,下列说法错误的是
A.曲线m表示pH与 变化的曲线 变化的曲线 |
B.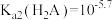 |
C. 溶液中: 溶液中: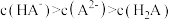 |
D.交点a的溶液中: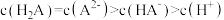 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】下列关于NaHCO3溶液(不考虑空气溶解)的相关事实,能够证明H2CO3为弱酸的是
A.溶液中存在 | B.溶液中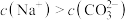 |
| C.溶液中存在两种分子 | D.溶液中pH>7 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】 为二元酸,其电离过程为:
为二元酸,其电离过程为: ,
, 。常温时,向
。常温时,向 水溶液中逐滴滴加
水溶液中逐滴滴加 溶液,混合溶液中
溶液,混合溶液中 、
、 和
和 的物质的量分数
的物质的量分数 随pH变化的关系如图所示。下列说法正确的是
随pH变化的关系如图所示。下列说法正确的是
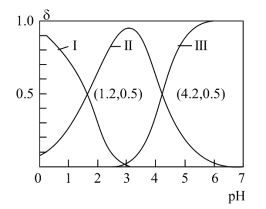
 为二元酸,其电离过程为:
为二元酸,其电离过程为: ,
, 。常温时,向
。常温时,向 水溶液中逐滴滴加
水溶液中逐滴滴加 溶液,混合溶液中
溶液,混合溶液中 、
、 和
和 的物质的量分数
的物质的量分数 随pH变化的关系如图所示。下列说法正确的是
随pH变化的关系如图所示。下列说法正确的是
A. 的 的 的数量级为 的数量级为 |
B.当溶液中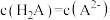 时, 时, |
C.当溶液中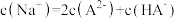 时,加入V( 时,加入V( 溶液) 溶液)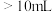 |
D.向 的溶液中继续滴加 的溶液中继续滴加 溶液,水的电离程度减小 溶液,水的电离程度减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
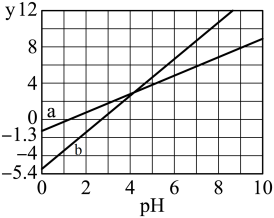
【推荐2】常温下,某二元弱酸H2A溶液中离子浓度与pH的关系如图所示{y为lg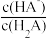 或lg
或lg }。下列说法错误的是
}。下列说法错误的是
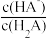 或lg
或lg }。下列说法错误的是
}。下列说法错误的是
A.曲线a为lg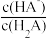 与pH的变化关系 与pH的变化关系 |
| B.该温度下,H2A的Ka1为10-1.3 |
| C.升高温度,则图中曲线a、b下移 |
| D.曲线a、b的交点处,溶液中c(A2—)=c(HA—) |
您最近一年使用:0次

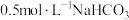 溶液滴定
溶液滴定 溶液,加入的
溶液,加入的 时溶液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的
时溶液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的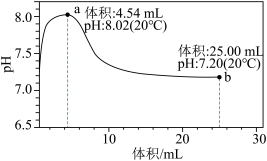
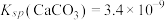 ,
, ,
,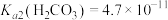 。
。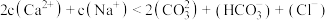
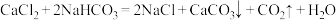
 的数量级为
的数量级为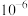
 ]。下列叙述错误的是
]。下列叙述错误的是


