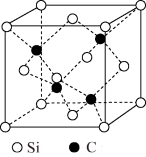按要求完成下列问题:
Ⅰ.氧化锆(化学式为 )晶胞结构如图所示:
)晶胞结构如图所示:
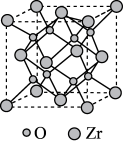
(1) 在晶胞中的配位数是
在晶胞中的配位数是______ ,若该晶胞的密度为 ,用
,用 表示
表示 伏伽德罗常数的值,则该晶胞的体积是
伏伽德罗常数的值,则该晶胞的体积是______  (列出计算式)。(氧化锆的摩尔质量
(列出计算式)。(氧化锆的摩尔质量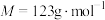 )
)
Ⅱ.Ce、Zr、Mn和Fe都是过渡金属元素,Mn与Fe两元素的部分电离能如下表所示。
(2)铁元素位于元素周期表______ 族,属于______ 区。
(3)比较两元素的 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子更难,请从原子结构分析原因
再失去1个电子更难,请从原子结构分析原因______ 。
Ⅰ.氧化锆(化学式为
 )晶胞结构如图所示:
)晶胞结构如图所示:
(1)
 在晶胞中的配位数是
在晶胞中的配位数是 ,用
,用 表示
表示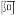 伏伽德罗常数的值,则该晶胞的体积是
伏伽德罗常数的值,则该晶胞的体积是 (列出计算式)。(氧化锆的摩尔质量
(列出计算式)。(氧化锆的摩尔质量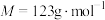 )
)Ⅱ.Ce、Zr、Mn和Fe都是过渡金属元素,Mn与Fe两元素的部分电离能如下表所示。
| 元素 | 电离能( ) ) | ||
 |  |  | |
| Mn | 717 | 1509 | 3248 |
| Fe | 759 | 1561 | 2957 |
(2)铁元素位于元素周期表
(3)比较两元素的
 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子更难,请从原子结构分析原因
再失去1个电子更难,请从原子结构分析原因
更新时间:2024-04-10 09:49:56
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,用化学用语回答下列问题:
(1)原子半径最小的元素是___________ (填元素名称);非金属性最强的是___________ (填元素符号)。
(2)②与④形成的原子个数比为1∶2的化合物的结构式为___________ 。
(3)①、⑥、⑨与④按照1∶1∶1∶4形成的化合物,在熔化过程中克服的作用力为___________
A.离子键 B.共价键 C.分子间作用力 D.离子键和共价键
(4)③、④、⑥的离子半径由大到小的顺序为___________ (用离子符号表示)。
(5)②、③、⑤分别与氢气化合,形成简单气态氢化物的稳定性由强到弱的顺序为___________ (用分子式表示)。
(6)请设计实验证明⑥与⑦的金属性强弱___________ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)②与④形成的原子个数比为1∶2的化合物的结构式为
(3)①、⑥、⑨与④按照1∶1∶1∶4形成的化合物,在熔化过程中克服的作用力为
A.离子键 B.共价键 C.分子间作用力 D.离子键和共价键
(4)③、④、⑥的离子半径由大到小的顺序为
(5)②、③、⑤分别与氢气化合,形成简单气态氢化物的稳定性由强到弱的顺序为
(6)请设计实验证明⑥与⑦的金属性强弱
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,Q的核电荷数是X与Z的核电荷数之和, E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为___________ 、____________ ;
(2)XZ2与YZ2分子的立体结构分别是___________ 和___________ ,在水中溶解度较大的是________ (填化学式);
(3)Q元素的价电子排布图为___________ ,在形成化合物时它的最高化合价为_____ ;
(4)Z与E形成的化合物中,各原子最外层都达到8电子结构,该化合物中心原子采用的轨道杂化方式是____________ 。
(1)X、Y的元素符号依次为
(2)XZ2与YZ2分子的立体结构分别是
(3)Q元素的价电子排布图为
(4)Z与E形成的化合物中,各原子最外层都达到8电子结构,该化合物中心原子采用的轨道杂化方式是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】砷的一些化合物常用作半导体、除草剂、杀鼠药等。回答下列问题:
(1)基态As原子的核外电子排布式为[Ar]__________ ,有___________ 个未成对电子。
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是_____________ 。
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为____________ ,1mol 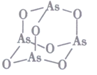 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为________ mol。
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0, );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为_____________ 。
②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为____________ g·cm-3(列出计算式即可)。
(1)基态As原子的核外电子排布式为[Ar]
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为
 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0,
 );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】已知X、Y、Z、W、R是元素周期表前四周期中原子序数依次增大的常见元素,相关信息如下表:
(1)X基态原子中能量最高的电子,其电子云在空间有___________ 个方向,原子轨道呈___________ 形。
(2) 是动物和人体所必需的微量元素之一,也是重要的工业原料,与Y同族。Se的原子结构示意图为
是动物和人体所必需的微量元素之一,也是重要的工业原料,与Y同族。Se的原子结构示意图为___________ 。
(3)Z的基态原子的电子排布式为___________ 。
(4)H2Y的中心原子采取___________ 杂化,VSEPR模型为___________ ,分子构型为___________ 。
| 元素 | 相关信息 |
| X | 元素原子的核外p电子数比s电子数少1 |
| Y | 地壳中含量最多的元素 |
| Z | 第一电离能至第四电离能分别是: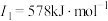 , , , ,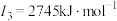 , ,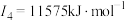 |
| W | 前四周期中电负性最小的元素 |
| R | 在周期表的第十一列 |
(2)
 是动物和人体所必需的微量元素之一,也是重要的工业原料,与Y同族。Se的原子结构示意图为
是动物和人体所必需的微量元素之一,也是重要的工业原料,与Y同族。Se的原子结构示意图为(3)Z的基态原子的电子排布式为
(4)H2Y的中心原子采取
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】钙和铜合金可用作电解制钙的阴极电极材料,回答下列问题:
(1)Cu在元素周期表中的位置是_______ ,基态Cu2+核外电子填充的最高能级符号为_____ 。
(2)CaCO3高温分解可制得CaO。CaO与C在一定条件下可生成CaC2,CaC2与水反应生成Ca(OH)2和一种4原子气体分子。
①该气体分子的电子式______ ,该气体分子中σ键与π键的数目之比为______ 。
②C原子未成对电子的数目为______ 。
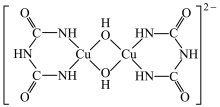
(3)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如下图所示,该反应原理可用于检验蛋白质或其他含肽键的化合物。______ 、_______ 。
(1)Cu在元素周期表中的位置是
(2)CaCO3高温分解可制得CaO。CaO与C在一定条件下可生成CaC2,CaC2与水反应生成Ca(OH)2和一种4原子气体分子。
①该气体分子的电子式
②C原子未成对电子的数目为
(3)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如下图所示,该反应原理可用于检验蛋白质或其他含肽键的化合物。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】已知A、B、C、D、E、F都是元素周期表中前36号元素,它们的原子序数依次增大。A原子基态时最外层电子数是其内层电子总数的2倍,C原子基态时s电子数与p电子数相等,D在元素周期表的各元素中电负性最大,E的基态原子核外有6个能级且全部充满电子,F原子基态时未成对电子数是同周期元素中最多的。
(1)F元素的名称是________ ,基态F原子的价电子轨道表示式_________ 画出AC2的电子式_______________ E元素常见离子的电子排布式______________ 。
(2)A、B、C的电负性大小顺序(填元素符号,下同)______________ ,第一电离能大小顺序为_________________ 。
(1)F元素的名称是
(2)A、B、C的电负性大小顺序(填元素符号,下同)
您最近一年使用:0次
【推荐1】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大,A元素的价层电子排布式为 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)D、C两种元素形成的化合物的电子式为___________ 。
(2)A、B、C三种元素的电负性由小到大的顺序为___________ (用元素符号表示)。
(3)C元素的电子排布图为___________ 。
(4)E元素位于元素周期表的第___________ 族,形成的离子中较稳定的离子的价层电子排布式是___________ 。
(5)F元素位于元素周期表的___________ 区,B元素原子核外占据最高能级的电子云轮廓图是___________ 形。
(6)G可能的性质有___________(填字母)。
 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)D、C两种元素形成的化合物的电子式为
(2)A、B、C三种元素的电负性由小到大的顺序为
(3)C元素的电子排布图为
(4)E元素位于元素周期表的第
(5)F元素位于元素周期表的
(6)G可能的性质有___________(填字母)。
| A.其最高价氧化物对应水化物是弱酸 | B.其第一电离能小于磷小于硒 |
| C.其原子半径大于锗 | D.氢化物的稳定性G大于A |
您最近一年使用:0次
【推荐2】C、N、O、Al、Si、Cu是常见的六种元素。
①Si位于元素周期表第________ 周期第________ 族。
②N的基态原子核外电子排布式为________ ;Cu的基态原子最外层有________ 个电子。
③用“>”或“<”填空:
(2)O、Na、P、Cl四种元素中电负性最大的是________ (填元素符号),其中P原子的核外电子排布式为___________________ 。
(3)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是_________ (填元素符号),e的价层电子轨道示意图为____________ 。
(4)①N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
则该元素是________ (填写元素符号)。
②基态锗(Ge)原子的电子排布式是______ 。Ge的最高价氯化物的分子式是________ 。
③Ge元素可能的性质或应用有______ 。
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其最高价氯化物的沸点低于其溴化物的沸点
①Si位于元素周期表第
②N的基态原子核外电子排布式为
③用“>”或“<”填空:
| 原子半径 | 电负性 | 熔点 | 沸点 |
| Al | N | 金刚石 | CH4 |
(2)O、Na、P、Cl四种元素中电负性最大的是
(3)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是
(4)①N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | …… |
| In/(kJ·mol-1) | 578 | 1 817 | 2 745 | 11 578 | …… |
则该元素是
②基态锗(Ge)原子的电子排布式是
③Ge元素可能的性质或应用有
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其最高价氯化物的沸点低于其溴化物的沸点
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
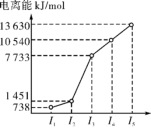
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有__________ 种不同空间运动状态的电子。
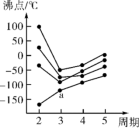
(2)如图所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中 a 点代表的是___________ 。判断依据是_____________________ 。
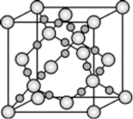
(3)CO2 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于___________ 晶体。
(4)第一电离能介于 Al、P 之间的第三周期元素有___________ 种。 GaCl3 中中心原子的杂化方式为___________ ,写出与 GaCl3 结构相同的一种离子___________ 。
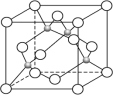
(5)下图是碳化硅的晶胞结构 。若碳化硅晶胞边长为 apm,阿伏加德罗常数为 NA ,则碳化硅晶体的密度为___________ g/cm3.(列出计算式即可)
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有

(2)如图所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中 a 点代表的是

(3)CO2 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于

(4)第一电离能介于 Al、P 之间的第三周期元素有
(5)下图是碳化硅的晶胞结构 。若碳化硅晶胞边长为 apm,阿伏加德罗常数为 NA ,则碳化硅晶体的密度为

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】硫酸氧钒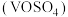 广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:
广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:
方法一:还原法制备

已知:在溶液中,钒主要以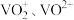 的形式存在。
的形式存在。
(1)基态 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为_____________________
(2)真空干燥时需通入 的作用是
的作用是_____________________________ 。
(3)溶液 转化为
转化为 需要加入还原剂,最佳的还原剂为
需要加入还原剂,最佳的还原剂为_________ (填字母),写出相对应的离子方程式__________________________________________________
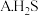
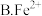

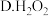
方法二:电解法制备
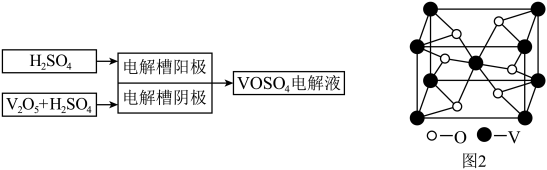
(4)写出电解槽中阴极反应式_________________________________________________________ 。
(5)与“电解法”相比,“还原法”的主要不足之处有_____________________ (写出一点)。
(6)钒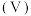 的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为
的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为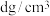 ,
, 表示阿伏加德罗常数的值,则晶胞的体积为
表示阿伏加德罗常数的值,则晶胞的体积为_____________________ 。
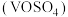 广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:
广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:方法一:还原法制备


已知:在溶液中,钒主要以
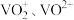 的形式存在。
的形式存在。(1)基态
 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为(2)真空干燥时需通入
 的作用是
的作用是(3)溶液
 转化为
转化为 需要加入还原剂,最佳的还原剂为
需要加入还原剂,最佳的还原剂为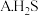
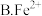

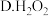
方法二:电解法制备


(4)写出电解槽中阴极反应式
(5)与“电解法”相比,“还原法”的主要不足之处有
(6)钒
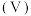 的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为
的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为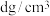 ,
, 表示阿伏加德罗常数的值,则晶胞的体积为
表示阿伏加德罗常数的值,则晶胞的体积为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】铁(Fe)、钴(Co)、镍(Ni)是第四周期第VIII族的元素,称为铁系元素,相关化合物在生产生活中应用广泛。
(1)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103℃,则Fe(CO)5中含有的化学键类型包括____________ (填字母)。
A.极性键 B.非极性键 C.配位键 D.金属键 E.离子键
(2)镍能形成多种配合物,如 、
、 、
、 等,下列有关说法正确的是___________(填字母)。
等,下列有关说法正确的是___________(填字母)。
(3)Co3+的一种配离子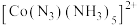 中,Co3+的配位数是
中,Co3+的配位数是_____________ ,Fe、Co、Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点,Fe、Co、Ni明显高于Ca,其原因是_____________ 。
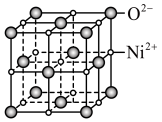
(4)NiO晶胞与NaCl晶胞相似,如图所示_____________ 个;每个氧离子周围与它最近且相等距离的氧离子有_________ 个。
(1)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103℃,则Fe(CO)5中含有的化学键类型包括
A.极性键 B.非极性键 C.配位键 D.金属键 E.离子键
(2)镍能形成多种配合物,如
 、
、 、
、 等,下列有关说法正确的是___________(填字母)。
等,下列有关说法正确的是___________(填字母)。A.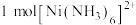 中含有 中含有 键的数目为 键的数目为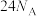 |
B. 中配体是CO,配位原子是C 中配体是CO,配位原子是C |
| C.NH3中N原子为sp3杂化,其空间构型为正四面体形 |
| D.Ni2+在形成配合物时其配位数只能为4,Fe在形成配合物时其配位数只能为5 |
(3)Co3+的一种配离子
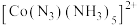 中,Co3+的配位数是
中,Co3+的配位数是(4)NiO晶胞与NaCl晶胞相似,如图所示
您最近一年使用:0次

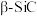 的晶胞结构如图所示,若碳和硅的原子半径分别为apm和bpm,密度为
的晶胞结构如图所示,若碳和硅的原子半径分别为apm和bpm,密度为 ,其原子的空间利用率(即晶胞中原子体积占空间体积的百分率)为
,其原子的空间利用率(即晶胞中原子体积占空间体积的百分率)为 ,
, 的代数式表示,
的代数式表示,