现有A、B、C、D、E、F六种元素,均为前4周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)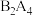 的电子式为
的电子式为___________ (用元素符号表示,下同)。
(2)C元素的原子核外共有___________ 种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3)某同学推断D元素基态原子的轨道表示式为: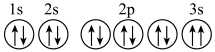 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了___________ (填序号)。
a.泡利不相容原理 b.洪特规则
(4)C、D、E三种元素的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(5)其中五种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,阳离子呈狭长的八面体结构(如下图所示)。阳离子中存在的化学键类型有___________ (填序号)。
该化合物加热时阳离子首先失去的组分是___________ (填化学式),判断理由是___________ 。
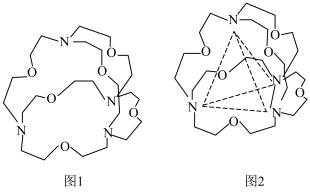
(6)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是___________ (填标号)。 b.
b. c.
c. d.
d.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素基态原子的核外p电子数比s电子数少1 |
| C元素基态原子的核外p轨道中有两个未成对电子 |
D元素的气态基态原子的第一至第四电离能分别是: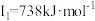 , ,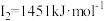 , ,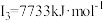 , ,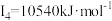 |
| E元素的主族序数比周期数大3 |
| F元素位于元素周期表中的第11列 |
(1)
 的电子式为
的电子式为(2)C元素的原子核外共有
(3)某同学推断D元素基态原子的轨道表示式为:
 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了a.泡利不相容原理 b.洪特规则
(4)C、D、E三种元素的简单离子半径由大到小的顺序是
(5)其中五种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,阳离子呈狭长的八面体结构(如下图所示)。阳离子中存在的化学键类型有

该化合物加热时阳离子首先失去的组分是
(6)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是
 b.
b. c.
c. d.
d.
更新时间:2024-04-15 16:46:46
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。
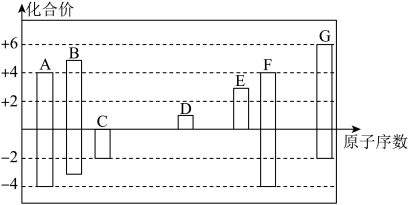
(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为_______ 。
(2)A、B、F三种元素的原子半径由大到小的顺序是_______ (填元素符号)。
(3)A形成的化合物种类繁多,请写出C7H16分子中主链为4个碳原子的结构简式_______ ,其在光照条件下生成的一氯代物有_______ 种不同的结构(不考虑立体异构)。
(4)E元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是_______ 。
(5)B的氧化物和G的氧化物均能形成酸雨。工业上用B的气态氢化物的水溶液作G氧化物的吸收剂,写出足量吸收剂与该氧化物反应的离子方程式:_______ 。
(6)元素C与D按原子个数比1∶1形成的化合物的电子式为_______ 。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(2)A、B、F三种元素的原子半径由大到小的顺序是
(3)A形成的化合物种类繁多,请写出C7H16分子中主链为4个碳原子的结构简式
(4)E元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是
(5)B的氧化物和G的氧化物均能形成酸雨。工业上用B的气态氢化物的水溶液作G氧化物的吸收剂,写出足量吸收剂与该氧化物反应的离子方程式:
(6)元素C与D按原子个数比1∶1形成的化合物的电子式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】第一电离能I1是指气态电中性原子X(g)处于基态时,失去一个电子成为气态基态正离子X+(g)所需的最低能量。如图所示是部分元素原子的第一电离能I1随原子序数变化的关系图。
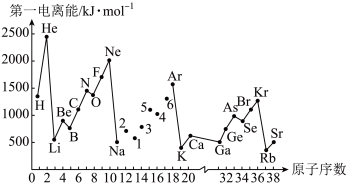
请回答下列问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na~Ar之间六种元素用短线连接起来,构成完整的图象___________ 。 第1、2、4、6号元素简单离子半径的大小关系是________ (用离子符号表示)。
(2)从题图分析可知,同主族元素原子的第一电离能I1变化规律是________ 。
(3)题图中5号元素在周期表中的位置是________ ;处于______ 区。
(4)题图中4、5、6号三种元素的最简单气态氢化物的沸点均比同主族上一周期元素的最简单气态氢化物的沸点低,原因是____________ 。

请回答下列问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na~Ar之间六种元素用短线连接起来,构成完整的图象
(2)从题图分析可知,同主族元素原子的第一电离能I1变化规律是
(3)题图中5号元素在周期表中的位置是
(4)题图中4、5、6号三种元素的最简单气态氢化物的沸点均比同主族上一周期元素的最简单气态氢化物的沸点低,原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有X、Y、Z、Q、E、M、G原子序数依次递增的七种元素,除G元素外其余均为短周期主族元素。X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素原子的外围电子层排布式为nsnnpn+1,Q的基态原子核外成对电子数是成单电子数的3倍,E与Q同周期,M元素的第一电离能在同周期主族元素中从大到小排第三位,G原子最外电子层上只有未成对电子,其内层所有轨道全部充满,但并不是第ⅠA族元素。回答下列问题:
(1)基态G原子的价电子排布式为_______ 。第三周期基态原子未成对电子数与G相同且电负性最大的元素是_______ (填元素名称),GQ受热分解生成G2Q和Q2,请从原子结构角度说明GQ受热易分解的原因_______ 。
(2)Z、Q、M三种元素的第一电离能从大到小的顺序为_______ (填元素符号)
(3)X与Q形成原子个数比为1:1的化合物的化学式为_______ 。
(4)Z、M、E所形成的简单离子的半径由大到小的顺序为_______ (填离子符号)
(5)X、Y、Z、Q的电负性由大到小的顺序为_______ (填元素符号)
(1)基态G原子的价电子排布式为
(2)Z、Q、M三种元素的第一电离能从大到小的顺序为
(3)X与Q形成原子个数比为1:1的化合物的化学式为
(4)Z、M、E所形成的简单离子的半径由大到小的顺序为
(5)X、Y、Z、Q的电负性由大到小的顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知W、X、Y、Z、M分别是元素周期表前四周期的元素,原子序数依次增大。其中基态X原子的最外层电子数是电子层数的3倍,基态W原子核外未成对电子数是同周期最多的元素。W、Y、Z的最高价氧化物的水化物两两可以反应。M为过渡元素,其基态原子的各能级均处于全充满稳定状态。完成下列各题:
(1)W、X均可形成18电子粒子,请写出W形成的18电子分子的电子式___________ 。该分子的水溶液具有弱碱性(类似 ),请写出其第一步电离方程式
),请写出其第一步电离方程式___________ 。
(2)空间站常用X、Y形成的一种化合物做供氧剂,其阴阳离子个数比为___________ 。
(3)Z的氯化物常以二聚物的形式存在,请写出其二聚物的结构式___________ 。
(4)M处于元素周期表的___________ 区,其氢氧化物具有两性,请写出该氢氧化物与氢氧化钠反应的离子方程式___________ 。
(1)W、X均可形成18电子粒子,请写出W形成的18电子分子的电子式
 ),请写出其第一步电离方程式
),请写出其第一步电离方程式(2)空间站常用X、Y形成的一种化合物做供氧剂,其阴阳离子个数比为
(3)Z的氯化物常以二聚物的形式存在,请写出其二聚物的结构式
(4)M处于元素周期表的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同族,它们原子的最外层电子排布式为ns1。B和D也属同族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子的最外层电子数等于D原子的最外层电子数的一半。请回答下列问题:
(1)A是________ ,B是________ ,E是________ 。
(2)写出C元素基态原子的电子排布式:________________________ 。
(3)元素B与D的电负性的大小关系是B____________ (填“>”“<”或“=”,下同)D,E与C的第一电离能大小关系是E________ C。
(4)写出元素E和C的最高价氧化物对应的水化物之间反应的离子方程式:_____________ 。
(1)A是
(2)写出C元素基态原子的电子排布式:
(3)元素B与D的电负性的大小关系是B
(4)写出元素E和C的最高价氧化物对应的水化物之间反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知A、B、C、D、E、F、G是原子序数依次递增的短周期元素,已知A和D为同一主族元素,C和F为同一主族元素,A元素的原子半径是所有主族元素中原子半径最小的,B原子的最外层电子数比次外层多3,G元素的最高正化合价与最低负化合价的代数和为6,E是同周期中金属离子半径最小的元素,F形成的化合物是形成酸雨的主要原因。请回答下列问题:
(1)写出B元素的名称:_____ 。
(2)写出C元素在周期表中的位置_____ 。
(3)E元素的原子结构示意图为_____ 。
(4)B、D、E三种元素的原子半径由大到小的顺序为_____ (填元素符号)。
(5)根据元素周期律,推断:
①C、F元素的氢化物还原性较强的是_____ (填对应氢化物的化学式)。
②F、G的元素最高价氧化物对应水化物酸性较强的是_____ (填对应酸的化学式)。
(6)由C、D形成的一种化合物可与水反应,生成标况下33.6L气体时转移的电子的物质的量为_____ 。
(7)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为_____ 。
(8)镓(Ga)与E同主族,工业制备镓的流程如图所示:
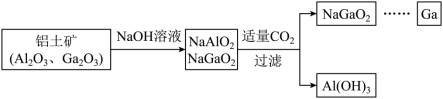
氢氧化镓与NaOH反应的化学方程式为_____ ;酸性:Al(OH)3_____ Ga(OH)3(填“>”或“<”)。
(1)写出B元素的名称:
(2)写出C元素在周期表中的位置
(3)E元素的原子结构示意图为
(4)B、D、E三种元素的原子半径由大到小的顺序为
(5)根据元素周期律,推断:
①C、F元素的氢化物还原性较强的是
②F、G的元素最高价氧化物对应水化物酸性较强的是
(6)由C、D形成的一种化合物可与水反应,生成标况下33.6L气体时转移的电子的物质的量为
(7)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
(8)镓(Ga)与E同主族,工业制备镓的流程如图所示:

氢氧化镓与NaOH反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】元素周期表前四周期A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ms1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有五个未成对电子。
(1)E元素原子的价电子排布式是______ ,在元素周期表中位置是_____ ,其最高价氧化物的化学式是__________ 。
(2)C基态原子的电子排布图为_____ ,若A为非金属元素,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于_____ 键(填“σ”或“π”)。
(3)当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是_______ 。
(4)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,A、B、C、D四种元素的电负性由大到小的顺序是_____ (用元素符号表示)。
(1)E元素原子的价电子排布式是
(2)C基态原子的电子排布图为
(3)当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是
(4)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,A、B、C、D四种元素的电负性由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E五种短周期元素。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上有3个未成对的电子;C元素在地壳中含量最高;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E的最外层电子数与其核外电子总数之比为3:8。
;E的最外层电子数与其核外电子总数之比为3:8。
(1)B的元素符号为_______ ,D元素在周期表中位置为_______ 。
(2)A、C形成的简单氢化物的键角顺序_______ (填化学式),并分析原因:_______ 。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)元素的非金属性C_______ (填“>”或“<”)E,并用化学原理证明(用化学方程式表示)_______ 。
 ;E的最外层电子数与其核外电子总数之比为3:8。
;E的最外层电子数与其核外电子总数之比为3:8。(1)B的元素符号为
(2)A、C形成的简单氢化物的键角顺序
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)元素的非金属性C
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、Q、R五种元素的原子序数依次增大.其中:X的最外层电子排布为 ;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。
;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。
请回答下列问题:
 元素基态原子的电子排布式为
元素基态原子的电子排布式为 ______ ,它的最高价氧化物的水化物的化学式为 ______ 。
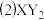 分子的立体构型是
分子的立体构型是 ______ ,中心原子的杂化方式是 ______ 。
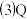 与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为
与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为 ______ 。该晶体中与氮原子距离相等且最近的氮原子有 ______ 个。
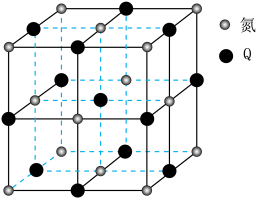
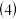 化合物
化合物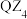 熔点为
熔点为 ,沸点为
,沸点为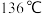 ,熔融态不导电,可知
,熔融态不导电,可知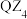 的晶体类型是
的晶体类型是 ______ 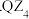 与热水反应的化学方程式为
与热水反应的化学方程式为 ______ 。
 ;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。
;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。请回答下列问题:
 元素基态原子的电子排布式为
元素基态原子的电子排布式为 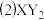 分子的立体构型是
分子的立体构型是 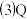 与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为
与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为 
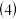 化合物
化合物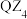 熔点为
熔点为 ,沸点为
,沸点为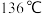 ,熔融态不导电,可知
,熔融态不导电,可知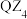 的晶体类型是
的晶体类型是 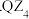 与热水反应的化学方程式为
与热水反应的化学方程式为
您最近一年使用:0次
【推荐1】VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是______ ;

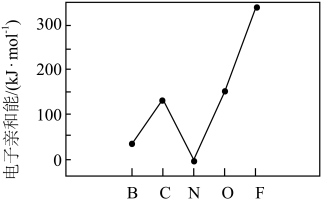
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是_______ ;氮元素的E1呈现异常的原因是________ 。
(3)Se原子序数为_______ ,其核外M层电子的排布式为_________ ;
(4)H2Se的稳定性比H2S_____________ (填“强”或“弱”)。SeO3分子的立体构型为______ 。
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从原子核外电子结构角度来看,Fe2+易被氧化成Fe3+的原因是_________ 。
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是

(3)Se原子序数为
(4)H2Se的稳定性比H2S
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从原子核外电子结构角度来看,Fe2+易被氧化成Fe3+的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氮族、氧族、卤族等在生活生产中都有重要应用。回答下列问题:
(1)NH3分子的VSEPR模型名称为___________ 。配合物 中的H—N—H的键角与游离的
中的H—N—H的键角与游离的 分子的键角比较,前者
分子的键角比较,前者_____ 后者(填“大于”“小于”或“相同”),其原因是___________ 。
(2)已知斥力大小:孤电子对-孤电子对>孤电子对-成键电子对,预测 离子的空间结构为
离子的空间结构为___________ 。
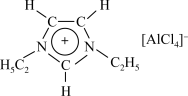
(3)①离子液体优异性能不断被开发利用。常见的离子液体含有如图中的离子等,已知微粒中的大 键可以用
键可以用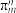 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则阳离子中的大
键中的电子数,则阳离子中的大 键可以表示为
键可以表示为___________ 。为了使正离子以单体形式存在以获得良好的溶解性能,与N原子相连的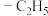 不能被H原子替换,请解释原因:
不能被H原子替换,请解释原因:___________ 。
② 也可以形成离子液体,这种离子中所有原子均满足8电子稳定结构,请写出
也可以形成离子液体,这种离子中所有原子均满足8电子稳定结构,请写出 的结构式
的结构式___________ 。
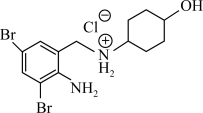
(4)为提高含氮碱性有机药物的水溶性,常用它们的盐酸盐。例如盐酸氨溴索(结构见如图)的阳离子可与水形成氢键,这些氢键表示式为O—H∙∙∙O(H2O)、___________ ,这种盐中C原子的杂化轨道的类型为___________ 。
(1)NH3分子的VSEPR模型名称为
 中的H—N—H的键角与游离的
中的H—N—H的键角与游离的 分子的键角比较,前者
分子的键角比较,前者(2)已知斥力大小:孤电子对-孤电子对>孤电子对-成键电子对,预测
 离子的空间结构为
离子的空间结构为(3)①离子液体优异性能不断被开发利用。常见的离子液体含有如图中的离子等,已知微粒中的大
 键可以用
键可以用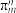 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则阳离子中的大
键中的电子数,则阳离子中的大 键可以表示为
键可以表示为 不能被H原子替换,请解释原因:
不能被H原子替换,请解释原因:
②
 也可以形成离子液体,这种离子中所有原子均满足8电子稳定结构,请写出
也可以形成离子液体,这种离子中所有原子均满足8电子稳定结构,请写出 的结构式
的结构式(4)为提高含氮碱性有机药物的水溶性,常用它们的盐酸盐。例如盐酸氨溴索(结构见如图)的阳离子可与水形成氢键,这些氢键表示式为O—H∙∙∙O(H2O)、

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】K、Al、Cu、H、C、O、S、Cl是常见的八种元素。
(1)从明矾[KAl(SO4)2·12H2O]制备 Al、K2SO4和H2SO4的过程如下图所示:
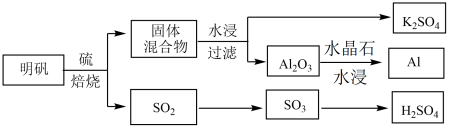
焙烧明矾的化学方程式为_________________________________________________ 。
(2)K位于元素周期表第________ 周期第________ 族。
(3)S的基态原子核外有________ 个未成对电子;Cl的基态原子核外电子排布式为____________ 。
(4)用“>”或“<”填空:
(5)SO2的价层电子对个数是________ ,该分子为结构为________ ;SO3中硫原子采用杂化方式为___________ 。
(6)新制备的Cu(OH)2可将乙醛氧化成乙酸,而自身还原成Cu2O。乙酸的沸点明显高于乙醛,其主要原因是____________________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有________ 个铜原子。
(7)Al单质为面心立方晶体,其晶胞参数a=0.405 nm,列式表示Al单质的密度__________ g·cm-3(列出计算式子,不必计算出结果)。
(1)从明矾[KAl(SO4)2·12H2O]制备 Al、K2SO4和H2SO4的过程如下图所示:

焙烧明矾的化学方程式为
(2)K位于元素周期表第
(3)S的基态原子核外有
(4)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| O | Cl- | KCl | H2SO4 |
(6)新制备的Cu(OH)2可将乙醛氧化成乙酸,而自身还原成Cu2O。乙酸的沸点明显高于乙醛,其主要原因是
(7)Al单质为面心立方晶体,其晶胞参数a=0.405 nm,列式表示Al单质的密度
您最近一年使用:0次



