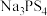 是固态电解质(SSE),具有与液体电解质相当高的离子电导率。回答下列问题:
是固态电解质(SSE),具有与液体电解质相当高的离子电导率。回答下列问题:(1)基态硫原子核外电子占据最高能层的符号是
(2)焰色试验可用于检验钠及其化合物,焰色试验中的特殊焰色属于
(3)在
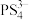 中,S元素显
中,S元素显(4)P的第一电离能
(5)钠原子激发态的电子排布式有
a.
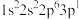 b.
b. c.
c.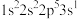 d.
d.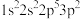
(6)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃,其晶胞结构如图所示。A、B点的原子坐标如图所示,则C点的原子坐标为

更新时间:2024-05-05 14:39:51
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】已知某工业废水中含有大量的 ,还可能大量存在
,还可能大量存在 中的几种,以及部分污泥,通过下列流程可从该废水中回收
中的几种,以及部分污泥,通过下列流程可从该废水中回收 晶体及固体单质。已知氧化性:
晶体及固体单质。已知氧化性: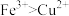 。
。
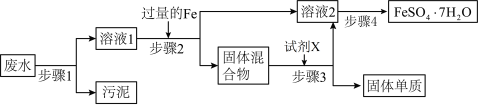
(1)不做任何实验就可以确定上述工业废水中一定不存在的离子是___________ (填离子符号)
(2)根据步骤2中得到固体混合物可以确定上述工业废水中肯定存在的离子是___________ (填离子符号)。
(3) 的存在对回收
的存在对回收 晶体的纯度
晶体的纯度___________ (填“有”或“无)影响,理由是___________ 。
(4)检验上述工业废水中是否存在 常用方法的名称是
常用方法的名称是___________ 。
(5)步骤3中加入的试剂X为________ (填试剂名称),发生反应的离子方程式为_________ 。
(6)步骤4中涉及的操作是:___________ 、___________ 、过滤、洗涤、烘干。烘干操作需在低温条件下进行,原因是___________ 。
 ,还可能大量存在
,还可能大量存在 中的几种,以及部分污泥,通过下列流程可从该废水中回收
中的几种,以及部分污泥,通过下列流程可从该废水中回收 晶体及固体单质。已知氧化性:
晶体及固体单质。已知氧化性: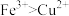 。
。
(1)不做任何实验就可以确定上述工业废水中一定不存在的离子是
(2)根据步骤2中得到固体混合物可以确定上述工业废水中肯定存在的离子是
(3)
 的存在对回收
的存在对回收 晶体的纯度
晶体的纯度(4)检验上述工业废水中是否存在
 常用方法的名称是
常用方法的名称是(5)步骤3中加入的试剂X为
(6)步骤4中涉及的操作是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3个主要水源的入口处采集水样,并进行了分析。实验信息:其中一入口处水源中含有A、B两种物质,一入口处水源中含有C、D两种物质,另一入口处水源中含有E物产, A、B、C 、D、E为五种常见化会物,均由表中的离子组成。
为了鉴别上述化合物,分别完成以下实验。实验结果如下:
① 将它们溶于水后, D溶液为蓝色溶液,其他均为无色溶液;
② 将E溶液滴入C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③ 进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃观察);
④在各溶液中加入硝酸钡溶液,再加入过量稀硝酸, A中有无色气泡逸出,C、D中有白色沉淀生成;
⑤将B、D两溶液混合,未见沉淀生成或气泡逸出。
根据上述实验回答下列问题:
(1)写出B、D的化学式:B_______ ,D_______ 。
(2)将含1 A的溶液与含1
A的溶液与含1  E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为
E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为_______ 。
(3)在A溶液中加入少量澄清石灰水,反应的离子方程式为_______ 。
(4)在C溶液中加入过量NaOH,反应的离子方程式:_______ 。
(5)若向含溶质1 mol的C溶液中逐滴加入 溶液,生成沉淀的质量最大为
溶液,生成沉淀的质量最大为_______ g。
| 阳离子 |  、 、 、 、 、 、 |
| 阴离子 |  、 、 、 、 、 、 |
① 将它们溶于水后, D溶液为蓝色溶液,其他均为无色溶液;
② 将E溶液滴入C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③ 进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃观察);
④在各溶液中加入硝酸钡溶液,再加入过量稀硝酸, A中有无色气泡逸出,C、D中有白色沉淀生成;
⑤将B、D两溶液混合,未见沉淀生成或气泡逸出。
根据上述实验回答下列问题:
(1)写出B、D的化学式:B
(2)将含1
 A的溶液与含1
A的溶液与含1  E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为
E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为(3)在A溶液中加入少量澄清石灰水,反应的离子方程式为
(4)在C溶液中加入过量NaOH,反应的离子方程式:
(5)若向含溶质1 mol的C溶液中逐滴加入
 溶液,生成沉淀的质量最大为
溶液,生成沉淀的质量最大为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】根据如图所示的转化关系推断各物质,已知A为淡黄色固体,常温下B和C为气体,A、D、E、H灼烧时焰色反应为黄色,回答下列问题:

(1)请写出物质的化学式:A___________ ,E___________ 。
(2)图中反应①的反应类型是___________ 。
(3)反应①的化学方程式为___________ ,反应②的化学方程式为___________ ,反应④的离子方程式为___________ 。
(4)D固体中含有少量的E,可采用的除杂方法为___________ (填化学方程式说明)。
(5)请设计实验鉴别D溶液和E溶液:______________________ 。

(1)请写出物质的化学式:A
(2)图中反应①的反应类型是
(3)反应①的化学方程式为
(4)D固体中含有少量的E,可采用的除杂方法为
(5)请设计实验鉴别D溶液和E溶液:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】N、Cu及其相关化合物用途非常广泛。回答下列问题:
(1)基态铜原子的价电子排布式为__________________ 。
(2)铜与钾处于同周期且最外层电子数相同,铜的熔沸点及硬度均比钾大,其原因是___________________________ 。
(3)NH3分子的立体构型为_________ ,中心原子的杂化类型是_________ 。
(4)N、S、P是组成蛋白质的常见元素。三种元素中第一电离能最大的是_________ ,电负性最小的是_________ 。(填元素符号)
(5)已知:Cu2O熔点为1235℃,CuCl熔点为426℃,则可判定Cu2O为_________ (填“离子晶体”或“分子晶体”,下同),CuCl为_________ 。
(6)氮与铜形成的一种化合物的晶胞结构如图所示。
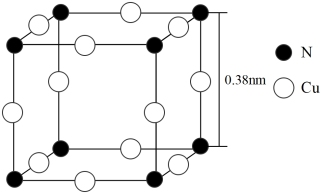
与每个Cu原子紧邻的Cu原子有_________ 个,阿伏伽德罗常数的数值为NA,该晶体的密度为_________ (列出计算式)g·cm-3。
(1)基态铜原子的价电子排布式为
(2)铜与钾处于同周期且最外层电子数相同,铜的熔沸点及硬度均比钾大,其原因是
(3)NH3分子的立体构型为
(4)N、S、P是组成蛋白质的常见元素。三种元素中第一电离能最大的是
(5)已知:Cu2O熔点为1235℃,CuCl熔点为426℃,则可判定Cu2O为
(6)氮与铜形成的一种化合物的晶胞结构如图所示。

与每个Cu原子紧邻的Cu原子有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】MnS 纳米粒子被广泛应用于除去重金属离子中的隔离子。
(1) 锰的价层电子排布式为_____________ ,Mn2+中未成对电子数为_______ 。
(2) 磁性氧化铁纳米粒子除隔效率不如 MnS 纳米粒子,试比较两种纳米材料中的阴离子 的半径大小 :__________ ,常温下H2O是液态 而H2S是气态的原因是__________ 。
(3)Mn 可以形成多种配合物,[Mn(CO )(H2O)2(NH3)3] Cl2• H2O中第二周期元素第一电离能大小关系为_____________ ,配体H2O、NH3中心原子杂化类型均为_________ 。
(4) S 和 Na 形成的晶体晶胞如图所示 ,该晶体的化学式为_____________ ,设晶胞的 棱长为a c m 。试计算 R 晶体的密度:_____________ (阿伏加 德罗常数的值用 NA表示 ) 。
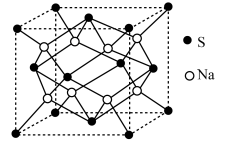
(1) 锰的价层电子排布式为
(2) 磁性氧化铁纳米粒子除隔效率不如 MnS 纳米粒子,试比较两种纳米材料中的阴离子 的半径大小 :
(3)Mn 可以形成多种配合物,[Mn(CO )(H2O)2(NH3)3] Cl2• H2O中第二周期元素第一电离能大小关系为
(4) S 和 Na 形成的晶体晶胞如图所示 ,该晶体的化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+原子核外有3层电子且M层3d轨道电子全充满。请回答下列问题:
(1)E元素在周期表中的位置为_______ ,属于_______ 区。
(2)B、C、D三种元素的第一电离能最大的是_______ (填元素符号),第一电离能最大的原因是_______ 。
(3)D元素与氟元素相比,电负性:D_______ F(填“>”“=”或“<”),下列表述中能证明这一事实的是_______ (填字母)。
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物CA5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,其电子式为_______ 。
(1)E元素在周期表中的位置为
(2)B、C、D三种元素的第一电离能最大的是
(3)D元素与氟元素相比,电负性:D
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物CA5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,其电子式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】碳酸乙烯酯广泛用作电池电解质、酯类合成的中间体等。一种由CH2=CH2、CO2及O2为原料,在铁、铜及碘化物催化下的制备碳酸乙烯酯的反应如下:

(1)Fe2+基态核外电子排布式为____ 。
(2)写出一种与CO2互为等电子体的阴离子:____ 。
(3)碳酸乙烯酯中碳原子杂化轨道类型为____ ;1mol碳酸乙烯酯分子中含 键数目为
键数目为____ 。
(4)FeO晶胞结构如图-1所示,晶体中与每个Fe2+紧邻的Fe2+有____ 个;一种由Sn、Cu、Fe及S组成的化合物的晶胞结构如图-2所示。该化合物的化学式为____ 。
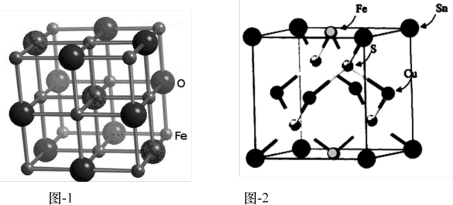

(1)Fe2+基态核外电子排布式为
(2)写出一种与CO2互为等电子体的阴离子:
(3)碳酸乙烯酯中碳原子杂化轨道类型为
 键数目为
键数目为(4)FeO晶胞结构如图-1所示,晶体中与每个Fe2+紧邻的Fe2+有

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是nsnnp2n;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:A_______ ;B_______ ;C_______ ;D_______ 。
②A、B、C三种元素的电负性由大到小的顺序为:_______ 。
③B、C、D、E四种元素的第一电离能由大到小的顺序为:_______ 。
(2)以下是A、B、C、D、E、F元素中某种元素的部分电离能,由此可推断该元素是_______ 。(填元素名称)
(3)F元素位于周期表的_______ 区,未成对电子对数为_______ ,最外层电子所占能级轨道电子云轮廓图的形状为_______ ,与F元素同周期的元素中未成对电子数最多的是_______ 。(填元素符号)
(1)请用元素符号完成下列空白:
①元素:A
②A、B、C三种元素的电负性由大到小的顺序为:
③B、C、D、E四种元素的第一电离能由大到小的顺序为:
(2)以下是A、B、C、D、E、F元素中某种元素的部分电离能,由此可推断该元素是
| I1 | I2 | I3 | I4 | I5 |
| 578 kJ·mol-1 | 1817 kJ·mol-1 | 2745 kJ·mol-1 | 11575 kJ·mol-1 | 14830 kJ·mol-1 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下列是元素周期表中的部分元素,请回答下列有关问题:
(1)①元素的价层电子排布式___________ ,⑦元素基态原子的价层电子轨道表示式为___________ 。
(2)上述表中的元素中,电负性最小的元素是___________ (填元素符号,下同),第三周期第一电离能最大的元素是___________ 。
(3)上述表中元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式,下同),碱性最强的是___________ 。
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ | |||||
(2)上述表中的元素中,电负性最小的元素是
(3)上述表中元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】世界上最早发现并使用锌的是中国,明朝末年天工开物)书中有关于炼锌技术的记载。回答下列问题:
(1)Zn在元素周期表中位于____________ 区。
(2)硫酸锌溶于过量的氨水可形成配合物[Zn(NH3)4]SO4。
①配合物[Zn(NH3)4]SO4中,[Zn(NH3)4]2+的名称是____________ ,中心原子的配位数为______ ;NH3为该配合物的_________________ 。
② 中,中心原子的轨道杂化类型为
中,中心原子的轨道杂化类型为___________________ 。
③NH3极易溶于水,除了因为它们都是极性分子外,还因为_____________________ 。
(3)Zn2+的4s和4p轨道可以形成sp3型杂化轨道,那么[ZnCl4]2-的空间构型为______________ 。
(4)氧化锌的结构有多种,其中一种立方闪锌矿的结构如图所示,若该晶胞的边长为a nm,NA为阿伏加 德罗常数的值,则立方闪锌矿晶体的ρ密度为_________ g/cm3。
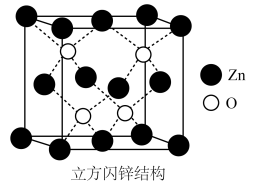
(1)Zn在元素周期表中位于
(2)硫酸锌溶于过量的氨水可形成配合物[Zn(NH3)4]SO4。
①配合物[Zn(NH3)4]SO4中,[Zn(NH3)4]2+的名称是
②
 中,中心原子的轨道杂化类型为
中,中心原子的轨道杂化类型为③NH3极易溶于水,除了因为它们都是极性分子外,还因为
(3)Zn2+的4s和4p轨道可以形成sp3型杂化轨道,那么[ZnCl4]2-的空间构型为
(4)氧化锌的结构有多种,其中一种立方闪锌矿的结构如图所示,若该晶胞的边长为a nm,NA为阿伏加 德罗常数的值,则立方闪锌矿晶体的ρ密度为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】废三元锂离子电池中含有镍、钻、锰、锂、铝等金属元素,是重要的二次资源。由某18650型废三元锂离子电池回收镍、钻、锰的工艺流程如下图所示:
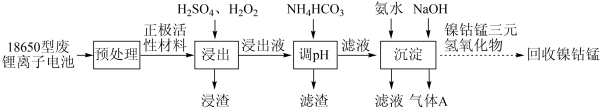
已知:①浸出液中各金属离子的质量浓度如下表。
② 能与
能与 、
、 、
、 形成配合物。
形成配合物。
Ⅰ.回答下列问题:
(1)“浸出”后得到浸出液的操作是___________ 。
(2)正极活性材料中的 在“浸出”过程中转化的化学方程式为
在“浸出”过程中转化的化学方程式为___________ 。
(3)镍、钴、锰的浸出率随时间、温度的变化如图1、图2所示。
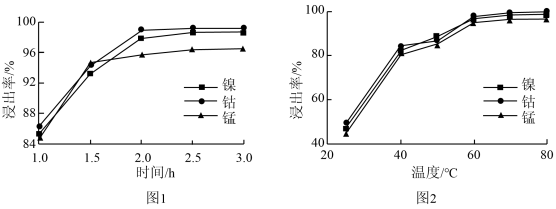
①综合考虑,选择浸出时间为___________ 。
②选择浸出温度范围为60-70℃,理由是___________ 。
(4)“调pH”中有沉淀生成,生成沉淀反应的离子方程式为___________ 。
(5)“沉淀”中气体A为___________ (填化学式)。沉淀后,分离获得镍钴锰三元氢氧化物沉淀并多次洗涤,判断沉淀洗净的方法是___________ 。
(6)已知25℃时,部分物质的溶度积常数如下:
要使滤液中 、
、 、
、 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全)的pH应大于
为沉淀完全)的pH应大于___________ ( ,
, )。
)。
Ⅱ.“氢能”是21世纪的绿色能源,研发新型储氢材料是开发利用氢能的重要研究方向。
(7) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态 的未成对电子数有
的未成对电子数有___________ 个。
② 晶体由
晶体由 和
和 构成,
构成, 中B原子的杂化方式为
中B原子的杂化方式为___________ , 离子的空间构型为
离子的空间构型为___________ , 晶体含有的化学键有
晶体含有的化学键有___________ (填标号)。
A.离子键 B.极性键 C.非极性键 D配位键 E.金属键
(8)某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示:
M是___________ (填元素符号),判断理由为___________ 。
(9)镧镍合金也是一种重要储氢材料。某种镧镍合金储氢后的晶胞结构如图所示,其化学式为___________ 。


已知:①浸出液中各金属离子的质量浓度如下表。
| 金属离子 |  |  |  |  |  |
质量浓度( ) ) | 1600 | 5144 | 1495 | 842 | 254 |
 能与
能与 、
、 、
、 形成配合物。
形成配合物。Ⅰ.回答下列问题:
(1)“浸出”后得到浸出液的操作是
(2)正极活性材料中的
 在“浸出”过程中转化的化学方程式为
在“浸出”过程中转化的化学方程式为(3)镍、钴、锰的浸出率随时间、温度的变化如图1、图2所示。

①综合考虑,选择浸出时间为
②选择浸出温度范围为60-70℃,理由是
(4)“调pH”中有沉淀生成,生成沉淀反应的离子方程式为
(5)“沉淀”中气体A为
(6)已知25℃时,部分物质的溶度积常数如下:
| 物质 |  |  |  |
 | 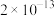 |  | 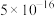 |
 、
、 、
、 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全)的pH应大于
为沉淀完全)的pH应大于 ,
, )。
)。Ⅱ.“氢能”是21世纪的绿色能源,研发新型储氢材料是开发利用氢能的重要研究方向。
(7)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①基态
 的未成对电子数有
的未成对电子数有②
 晶体由
晶体由 和
和 构成,
构成, 中B原子的杂化方式为
中B原子的杂化方式为 离子的空间构型为
离子的空间构型为 晶体含有的化学键有
晶体含有的化学键有A.离子键 B.极性键 C.非极性键 D配位键 E.金属键
(8)某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示:
 | 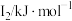 |  |  |  |
| 738 | 1451 | 7733 | 10540 | 13630 |
(9)镧镍合金也是一种重要储氢材料。某种镧镍合金储氢后的晶胞结构如图所示,其化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(1)如图为一个金属铜的晶胞,请完成以下各题。
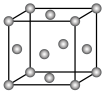
①该晶胞“实际”拥有的铜原子数是_________ 个。
②该晶胞称为________ (填序号)。
A 六方晶胞 B 体心立方晶胞 C 面心立方晶胞 D 简单立方晶胞
③此晶胞立方体的边长为 ,
, 的摩尔质量为
的摩尔质量为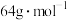 ,金属铜的密度为
,金属铜的密度为 ,则阿伏加 德罗常数为
,则阿伏加 德罗常数为________ (用a、 表示)
表示) 。
。
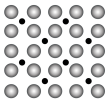
(2)洁净铁(可用于合成氨反应的催化剂)的表面上存在氮原子,如图为氮原子在铁的品面上的单层附着局部示意图(图中小黑色球代表氮原子,大灰色球代表铁原子)。则在图示状况下,铁颗粒表面上 的原子数的比值为
的原子数的比值为____________ 。
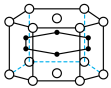
(3)硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如图示意的是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下底面各有一个镁原子,6个硼原子位于棱柱内,则该化合物的化学式可表示为_______ 。
(4)若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。在变化的各阶段被破坏的微粒间的相互作用依次是_______ 。
A 氢键:分子间作用力:非极性键 B 氢键;分子间作用力:极性键
C 氢键;极性键;分子间作用力 D 分子间作用力;氢键:非极性键

①该晶胞“实际”拥有的铜原子数是
②该晶胞称为
A 六方晶胞 B 体心立方晶胞 C 面心立方晶胞 D 简单立方晶胞
③此晶胞立方体的边长为
 ,
, 的摩尔质量为
的摩尔质量为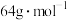 ,金属铜的密度为
,金属铜的密度为 ,则阿伏加 德罗常数为
,则阿伏加 德罗常数为 表示)
表示) 。
。(2)洁净铁(可用于合成氨反应的催化剂)的表面上存在氮原子,如图为氮原子在铁的品面上的单层附着局部示意图(图中小黑色球代表氮原子,大灰色球代表铁原子)。则在图示状况下,铁颗粒表面上
 的原子数的比值为
的原子数的比值为
(3)硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如图示意的是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下底面各有一个镁原子,6个硼原子位于棱柱内,则该化合物的化学式可表示为

(4)若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。在变化的各阶段被破坏的微粒间的相互作用依次是
A 氢键:分子间作用力:非极性键 B 氢键;分子间作用力:极性键
C 氢键;极性键;分子间作用力 D 分子间作用力;氢键:非极性键
您最近一年使用:0次



