某温度下,有反应H2(g)+I2(g)  2HI(g);正反应为放热反应,在带有活塞的密闭容器中达到平衡。下列说法中正确的是( )
2HI(g);正反应为放热反应,在带有活塞的密闭容器中达到平衡。下列说法中正确的是( )
 2HI(g);正反应为放热反应,在带有活塞的密闭容器中达到平衡。下列说法中正确的是( )
2HI(g);正反应为放热反应,在带有活塞的密闭容器中达到平衡。下列说法中正确的是( )| A.体积不变,升温,正反应速率减小 |
| B.温度、压强均不变,充入HI气体,开始时正反应速率增大 |
| C.温度不变,压缩气体的体积,平衡不移动,颜色加深 |
| D.体积、温度不变,充入氮气后,正反应速率将增大 |
11-12高二上·辽宁·期中 查看更多[4]
河南省安阳县第三高级中学2020-2021学年高二上学期第一次阶段考试化学试题江苏省启东中学2020-2021学年高二上学期期初考试化学试题(已下线)2011-2012学年辽南协作体高二上学期期中考试化学试卷(已下线)2014-2015学年黑龙江安达市高级中学高二第一次月考试题化学试卷
更新时间:2016-12-09 06:40:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列条件的改变对反应 的影响说法不正确的是
的影响说法不正确的是
 的影响说法不正确的是
的影响说法不正确的是| A.升高温度能加快化学反应速率 |
| B.增大H2的浓度能加快化学反应速率 |
| C.达到化学平衡状态时,N2能全部转化为NH3 |
| D.增大压强可加快该反应的化学反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列措施对增大反应速率明显有效的是
| A.Na与水反应时,增大水的用量 |
| B.Fe与稀硫酸反应制取氢气时,将稀硫酸改用浓硫酸 |
| C.在K2SO4与BaCl2两溶液反应时,增大压强 |
| D.N2与H2合成氨气时,增大体系的压强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
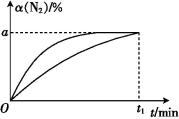
【推荐1】向温度和体积分别为T1和V1、T2和V2的两个密闭容器中均充入1 mol N2和2.8 mol H2,均保持温度和体积不变,发生反应N2(g)+3H2(g)  2NH3(g) ΔH<0,其反应过程中N2的转化率[α(N2)]随时间(t)的变化曲线如图所示。下列说法正确的是
2NH3(g) ΔH<0,其反应过程中N2的转化率[α(N2)]随时间(t)的变化曲线如图所示。下列说法正确的是
 2NH3(g) ΔH<0,其反应过程中N2的转化率[α(N2)]随时间(t)的变化曲线如图所示。下列说法正确的是
2NH3(g) ΔH<0,其反应过程中N2的转化率[α(N2)]随时间(t)的变化曲线如图所示。下列说法正确的是
| A.开始时,T1=T2、V1≠V2 |
| B.开始时,T1≠T2、V1=V2 |
| C.0~t1 min内,两个容器中放出的热量不同 |
| D.0~t1 min内,两个容器中正反应的平均反应速率不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关说法正确的是
| A.升高温度,使反应物分子中活化分子数增多,但活化分子百分数不变 |
B.N2(g)+3H2(g) 2NH3(g)在恒温恒压条件下进行,向容器中通入Ar(g),化学反应速率减小 2NH3(g)在恒温恒压条件下进行,向容器中通入Ar(g),化学反应速率减小 |
| C.在化学反应前后,催化剂的质量和化学性质都没有发生变化,故催化剂一定不参与化学反应 |
| D.100mL2mol•L-1的盐酸与锌反应时,加入适量的NaCl溶液,生成H2的速率不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O可用于制备含氯消毒剂。二氧化氯( )是一种黄绿色气体,易溶于水,在水中的溶解度约为
)是一种黄绿色气体,易溶于水,在水中的溶解度约为 的5倍,其水溶液在较高温度与光照下会生成
的5倍,其水溶液在较高温度与光照下会生成 与
与 。
。 是一种极易爆炸的强氧化性气体。Deacon曾提出在催化剂作用下,通过氧气直接氧化氯化氢成功制备氯气。该反应具有一定的可逆性,热化学方程式可表示为
是一种极易爆炸的强氧化性气体。Deacon曾提出在催化剂作用下,通过氧气直接氧化氯化氢成功制备氯气。该反应具有一定的可逆性,热化学方程式可表示为
 。关于Deacon提出的制
。关于Deacon提出的制 的反应,下列有关说法正确的是
的反应,下列有关说法正确的是
 )是一种黄绿色气体,易溶于水,在水中的溶解度约为
)是一种黄绿色气体,易溶于水,在水中的溶解度约为 的5倍,其水溶液在较高温度与光照下会生成
的5倍,其水溶液在较高温度与光照下会生成 与
与 。
。 是一种极易爆炸的强氧化性气体。Deacon曾提出在催化剂作用下,通过氧气直接氧化氯化氢成功制备氯气。该反应具有一定的可逆性,热化学方程式可表示为
是一种极易爆炸的强氧化性气体。Deacon曾提出在催化剂作用下,通过氧气直接氧化氯化氢成功制备氯气。该反应具有一定的可逆性,热化学方程式可表示为
 。关于Deacon提出的制
。关于Deacon提出的制 的反应,下列有关说法正确的是
的反应,下列有关说法正确的是| A.该反应的△S>0 |
B.每生成标准状况下22.4L ,放出58kJ的热量 ,放出58kJ的热量 |
| C.升高温度,该反应v(逆)增大,v(正)减小,平衡向逆反应方向移动 |
| D.断裂4mol H-Cl键的同时,有4mol H-O键生成,说明该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】反应A(g)+B(g) ⇋3X,在其他条件不变时,通过调节容器体积改变压强,达平衡时c(A)如下表:
下列分析不正确 的是
| 平衡状态 | ① | ② | ③ |
| 容器体积/L | 40 | 20 | 1 |
| c(A)( mol/L) | 0.022a | 0.05a | 0.75a |
| A.①→②的过程中平衡发生了逆向移动 |
| B.①→③的过程中X的状态发生了变化 |
| C.①→③的过程中A的转化率不断增大 |
| D.与①②相比,③中X的物质的量最大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
A. ,碳的质量不再改变说明反应已达平衡 ,碳的质量不再改变说明反应已达平衡 |
B. ,其他条件不变,缩小反应容器体积,正逆反应速率不变 ,其他条件不变,缩小反应容器体积,正逆反应速率不变 |
C.若压强不再随时间变化能说明反应达 已经平衡,则A、C不能同时是气体 已经平衡,则A、C不能同时是气体 |
D.恒温条件下,在恒容密闭容器中加入0.10 mol NO和足量固体活性炭,发生反应: ,达到平衡状态后向容器中再充入0.10 mol NO,再次平衡时NO的体积分数将增大 ,达到平衡状态后向容器中再充入0.10 mol NO,再次平衡时NO的体积分数将增大 |
您最近一年使用:0次




