常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是
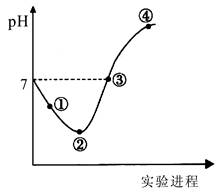

| A.曲线起点处水的电离程度最大,可用pH试纸测定溶液pH |
| B.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO- |
| C.氯气~氯水体系中:c(H+)=c(Cl2) +c(HClO)+c(ClO-) |
| D.③点所示溶液中:c(Na+) = c(Cl-)+c(ClO-) |
更新时间:2016-12-09 08:16:50
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列各溶液中,微粒的物质的量浓度关系正确的是
A.1.0mol/LNa2CO3溶液:c(OH-)=c(HCO )+c(H+)+2c(H2CO3) )+c(H+)+2c(H2CO3) |
B.1.0mol/LNH4Cl溶液:c(NH )=c(Cl-) )=c(Cl-) |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
D.1.0mol/LNaHCO3溶液中:c(OH-)+c(HCO )=c(H+)+c(Na+) )=c(H+)+c(Na+) |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,将0.2mol·L-1NaOH的溶液逐滴加入10mL0.2mol·L-1一元酸HA溶液中,pH的变化曲线如图所示,下列说法不正确的是


| A.HA电离常数Ka的数量级约为10-3 |
| B.a点溶液中c(HA)=9.9×10-7mol/L |
| C.b点溶液中c(HA)+c(A-)≈0.067mol·L-1 |
| D.pH=7时,c(A-)=0.1mol·L-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,将一定浓度的HA和HB两种酸分别与0.1mol/LNaOH溶液等体积混合,实验记录如下表:
下列说法正确的是
| 混合液 | pH | 加入的酸 | 酸的浓度/(mol/L) |
| ① | 8.6 | HA | 0.10 |
| ② | 2.0 | HB | 0.12 |
| A.HA为强酸,HB为弱酸 |
| B.溶液①中存在:c(A-)>c(Na+)>c(OH-)>c(H+) |
| C.升高温度,溶液①中c(H+)增大,pH减小 |
| D.溶液②中存在:c(Na+)+c(H+)=c(OH-)+c(B-) |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.除去FeSO4 溶液中的 Fe3+, 可向溶液中加入铜粉, 通过反应 Cu + 2Fe3+ = Cu2+ + 2Fe2+除去 Fe3+ |
| B.常温下,pH为5的 NH4Cl 溶液和pH为5的稀盐酸中,水的电离程度相同 |
C.由于存在水的电离,0.1 mol•L-1 的 H2C2O4溶液中, c(H+)/c(C2O )略大于2 )略大于2 |
D.向氨水中滴加等浓度的盐酸溶液,滴加过程中,c(NH )先增大后减小 )先增大后减小 |
您最近半年使用:0次

 数小于0.1NA
数小于0.1NA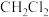 所含价电子总数为2NA
所含价电子总数为2NA


