室温下,将0.2mol·L-1NaOH的溶液逐滴加入10mL0.2mol·L-1一元酸HA溶液中,pH的变化曲线如图所示,下列说法不正确的是


| A.HA电离常数Ka的数量级约为10-3 |
| B.a点溶液中c(HA)=9.9×10-7mol/L |
| C.b点溶液中c(HA)+c(A-)≈0.067mol·L-1 |
| D.pH=7时,c(A-)=0.1mol·L-1 |
更新时间:2022-07-07 21:34:50
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】氢硫酸是一种弱酸(Ka1=1.3×10-7、Ka2=7.0×10-15)。室温下用0.1mol/LNaOH溶液吸收H2S得X溶液。下列说法正确的是
| A.X溶液中一定存在:c(H2S)>c(HS-) |
B.25℃时,若X溶液中c(HS-)=c(S2-),则c(OH-)=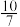 mol•L-1 mol•L-1 |
| C.当X溶液的pH=7时,溶液中存在:c(Na+)=c(HS-)+c(S2-) |
| D.Na2C2O4[Ka1(H2C2O4)=5.9×10-2]能与H2S发生反应:Na2C2O4+H2S=H2C2O4+Na2S |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
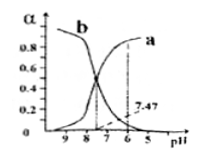
【推荐2】常温下,用一定浓度的盐酸滴定某浓度的氨水。滴定终点附近溶液的pH和导电能力的变化如图所示(利用溶液导电能力的变化可判断滴定终点,溶液总体积变化忽略不计)。下列说法错误的是( )
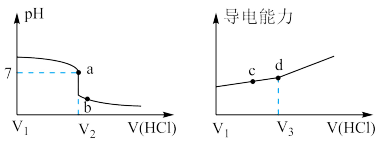

A.a点对应的溶液中: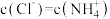 |
B.a→b过程中, 不断增大 不断增大 |
C.c→d溶液导电性增强的主要原因是 和 和 增大 增大 |
D.根据溶液pH和导电能力的变化可判断: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知HClO Ka=3.0×10-8,H2CO3 Ka1=4.1×10-7 Ka2=5.6×10-11试判断下列反应的离子方程式书写正确的是
A.硫酸铝溶液中加过量氨水:Al3++4NH3·H2O=AlO +4NH +4NH +2H2O +2H2O |
B.NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO |
C.惰性电极电解MgCl2水溶液Mg2++2Cl-+2H2O Mg(OH)2↓+H2↑+Cl2↑ Mg(OH)2↓+H2↑+Cl2↑ |
D.澄清石灰水与足量小苏打溶液混合:Ca2++OH-+HCO =CaCO3↓+H2O =CaCO3↓+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下向 溶液中滴加等浓度的
溶液中滴加等浓度的 溶液,滴定过程中溶液
溶液,滴定过程中溶液 随加入的
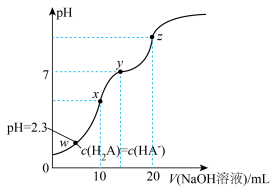
随加入的 溶液体积的变化曲线如图所示。下列说法正确的是
溶液体积的变化曲线如图所示。下列说法正确的是
 溶液中滴加等浓度的
溶液中滴加等浓度的 溶液,滴定过程中溶液
溶液,滴定过程中溶液 随加入的
随加入的 溶液体积的变化曲线如图所示。下列说法正确的是
溶液体积的变化曲线如图所示。下列说法正确的是
A.常温下, 的数量级为 的数量级为 |
| B.从w点至z点,水的电离程度逐渐增大 |
C.z点的离子浓度关系: |
D.在滴加 溶液过程中, 溶液过程中, |
您最近一年使用:0次

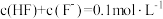 ,
, (X为
(X为 、
、 、
、 或
或 )与
)与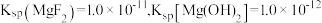 ,②
,②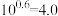 ,③坐标:
,③坐标: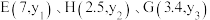 ,下列叙述错误的是
,下列叙述错误的是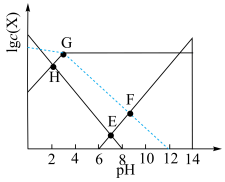
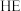 代表
代表 与
与 时,
时,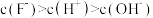

 悬浊液中通入
悬浊液中通入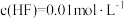 时,
时,


