下列说法正确的是
| A.除去FeSO4 溶液中的 Fe3+, 可向溶液中加入铜粉, 通过反应 Cu + 2Fe3+ = Cu2+ + 2Fe2+除去 Fe3+ |
| B.常温下,pH为5的 NH4Cl 溶液和pH为5的稀盐酸中,水的电离程度相同 |
C.由于存在水的电离,0.1 mol•L-1 的 H2C2O4溶液中, c(H+)/c(C2O )略大于2 )略大于2 |
D.向氨水中滴加等浓度的盐酸溶液,滴加过程中,c(NH )先增大后减小 )先增大后减小 |
19-20高二下·四川成都·期末 查看更多[2]
更新时间:2020-07-20 16:50:23
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】常温下,0.1mol/L醋酸钠溶液的 。下列相关说法
。下列相关说法不正确 的是
 。下列相关说法
。下列相关说法A.醋酸钠溶液显碱性的原因是: |
B.常温下,醋酸钠溶液中: |
C.向10mL上述溶液中滴加5滴饱和 溶液, 溶液,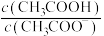 逐渐增大 逐渐增大 |
| D.在pH均为9的醋酸钠溶液和氨水中,水的电离程度:醋酸钠溶液>氨水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
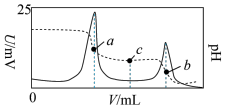
【推荐2】某研究小组利用电位滴定法研究盐酸滴加亚磷酸钠(NaHPO3)溶液的过程,得到电极电位U和溶液pH随盐酸滴加的体积变化曲线如图所示。下列说法正确的是
②亚磷酸(H3PO3)是二元弱酸,其电离常数分别是Ka1=10-14,Ka2=10-6.7。
②亚磷酸(H3PO3)是二元弱酸,其电离常数分别是Ka1=10-14,Ka2=10-6.7。
| A.a点对应溶液的pH>7 |
| B.b点对应第二次电极电位突跃,溶液的溶质是H3PO3 |
C.c点对应的溶液中存在:c(H+)<c(OH-)+c( )+2c( )+2c( ) ) |
| D.水的电离程度:a>b>c |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 时,用
时,用 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中 和
和 或
或 和
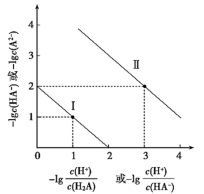
和 关系如图所示,下列说法不正确的是
关系如图所示,下列说法不正确的是
 时,用
时,用 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中 和
和 或
或 和
和 关系如图所示,下列说法不正确的是
关系如图所示,下列说法不正确的是
A. 为弱酸,其 为弱酸,其 约为 约为 |
B.滴定过程中,当 时, 时,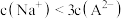 |
C.向 溶液中加入等体积等浓度的 溶液中加入等体积等浓度的 溶液,完全反应后溶液显碱性 溶液,完全反应后溶液显碱性 |
D.已知 的 的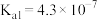 , , ,则足量 ,则足量 溶液中滴入少量 溶液中滴入少量 溶液,发生的离子反应为: 溶液,发生的离子反应为: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】分别测定不同浓度 溶液、
溶液、 溶液和
溶液和 溶液的电导率(
溶液的电导率( )数值,测定结果的数据处理如下表。
)数值,测定结果的数据处理如下表。
已知: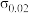 代表
代表 溶液的电导率数值;其他条件相同时,电导率越大,溶液导电性越好。
溶液的电导率数值;其他条件相同时,电导率越大,溶液导电性越好。
下列说法不正确 的是
 溶液、
溶液、 溶液和
溶液和 溶液的电导率(
溶液的电导率( )数值,测定结果的数据处理如下表。
)数值,测定结果的数据处理如下表。| 溶液 | 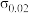 |  | 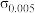 | 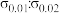 |  |
 溶液 溶液 | 4839 | 2478 | 1252 | 51.2% | 50.5% |
 溶液 溶液 | 10958 | 5593 | 2797 | 51.0% | 50.0% |
 溶液 溶液 | 267 | 182 | 126 | 68.2% | 69.2% |
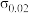 代表
代表 溶液的电导率数值;其他条件相同时,电导率越大,溶液导电性越好。
溶液的电导率数值;其他条件相同时,电导率越大,溶液导电性越好。下列说法
A.仅由 的数据不能说明三种电解质的强弱 的数据不能说明三种电解质的强弱 |
B.表中数据不能说明同等条件下 与 与 的导电能力强弱 的导电能力强弱 |
C. 比值数据能说明 比值数据能说明 存在电离平衡 存在电离平衡 |
D. 溶液的 溶液的 数据能说明溶液越稀, 数据能说明溶液越稀, 的电离程度越大 的电离程度越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
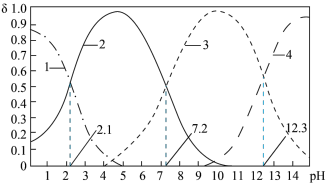
【推荐1】25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数 随溶液pH的变化曲线如下图所示。下列说法正确的是
随溶液pH的变化曲线如下图所示。下列说法正确的是
 随溶液pH的变化曲线如下图所示。下列说法正确的是
随溶液pH的变化曲线如下图所示。下列说法正确的是
A.曲线1和曲线2分别表示 (H3PO4)和 (H3PO4)和 (HPO42-)的变化 (HPO42-)的变化 |
| B.25℃时,H3PO4的电离常数K1=10-2.1 |
| C.pH=7.2时,溶液中c(H2PO4-)+c(HPO42-)+c(OH-)=c(Na+)+c(H+) |
| D.pH=12.3时,溶液中由水电离出的c(H+)=10-12.3 mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,用0.10mol·L-1的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示:
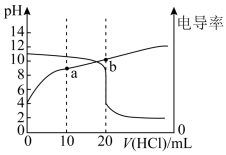
下列说法错误的是

下列说法错误的是
| A.BOH的Kb约为1×10-5 |
| B.a点:c(B+)+2c(H+)=2c(OH-)+c(BOH) |
| C.滴加盐酸的过程中,溶液中水的电离程度先减小后增大 |
| D.b点:c(B+)<0.05mol·L-1 |
您最近一年使用:0次

 溶液中加入
溶液中加入 溶液,当水电离的
溶液,当水电离的 ,滴加NaOH溶液的体积可出现两种情况,则HR为弱酸
,滴加NaOH溶液的体积可出现两种情况,则HR为弱酸 ,则HR为弱酸
,则HR为弱酸 的HR和
的HR和 的
的 溶液等体积混合后,溶液显酸性,则HR为弱酸
溶液等体积混合后,溶液显酸性,则HR为弱酸 及其盐,可通过离子交换树脂中的固体活性成分
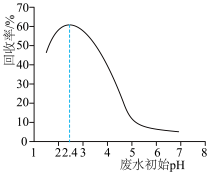
及其盐,可通过离子交换树脂中的固体活性成分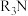 水解生成的阳离子静电吸附回收,其回收率(被吸附在树脂上甲酸根的物质的量分数)与废水初始
水解生成的阳离子静电吸附回收,其回收率(被吸附在树脂上甲酸根的物质的量分数)与废水初始 关系如图,下列说法不正确的是(已知
关系如图,下列说法不正确的是(已知 时,甲酸
时,甲酸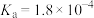 )
)

 的废水中
的废水中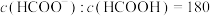
 ,随
,随 ,离子交换树脂活性成分主要以
,离子交换树脂活性成分主要以

