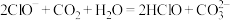某温度下,0.200 mol•L-1的HA溶液与0.200 mol•L-1的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如下表,下列说法正确的是
| 微粒 | X | Y | Na+ | A- |
| 浓度/(mol·L-1) | 8.00 10-4 10-4 | 2.50 10-10 10-10 | 0.100 | 9.92 10-2 10-2 |
| A.0.1mol·L-1HA溶液的pH=1 | B.该温度下Kw=1.0 10-14 10-14 |
| C.微粒X表示OH-,Y表示H+ | D.混合溶液中:n(A-)+n(X)=n(Na+) |
更新时间:2017-02-23 19:35:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.加入铝粉能产生H2的溶液中,一定存在大量的Na+、Ba2+、AlO2-、NO3- |
| B.100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
| C.室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液,可除去苯中少量苯酚 |
D.已知I3- I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】水的电离平衡曲线如图所示,下列说法正确的是


| A.图中A、B、D三点处Kw的大小关系:B>A>D |
B.25℃时,向pH=1的稀硫酸中逐滴加入pH=8的稀氨水,溶液中 的比值逐渐减小 的比值逐渐减小 |
| C.在25℃时,保持温度不变,在水中加入适量NH4Cl固体,体系可从A点变化到C点 |
D.A点所对应的溶液中,可同时大量存在Na+、Fe2+、ClO-、SO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知在溶液中 。室温下,在实验室里用0.01 mol·L-1的氢氧化钠溶液滴定20 mL的0.01 mol·L-1HX溶液,滴定曲线如图所示。下列叙述正确的是
。室温下,在实验室里用0.01 mol·L-1的氢氧化钠溶液滴定20 mL的0.01 mol·L-1HX溶液,滴定曲线如图所示。下列叙述正确的是

 。室温下,在实验室里用0.01 mol·L-1的氢氧化钠溶液滴定20 mL的0.01 mol·L-1HX溶液,滴定曲线如图所示。下列叙述正确的是
。室温下,在实验室里用0.01 mol·L-1的氢氧化钠溶液滴定20 mL的0.01 mol·L-1HX溶液,滴定曲线如图所示。下列叙述正确的是
| A.B点时c(X-) >c(Na+) |
| B.室温时0.01 mol·L-1的HX溶液pH=6 |
| C.A点时溶液中水的电离程度大于纯水的电离程度 |
| D.若C点时加入NaOH溶液40 mL,所得溶液中:c(X-)+2 c(HX) = c(OH-) - c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各组离子一定能大量共存的是
A.在酸性溶液中:K+、Fe2+、Cl-、 |
B.在含大量Fe3+的溶液中: 、Na+、Cl-、I- 、Na+、Cl-、I- |
C.常温下,在pH=13的溶液中: 、Al3+、 、Al3+、 、 、 |
D.与铝反应能产生大量氢气的溶液中:Na+、K+、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】人体血液中存在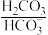 、
、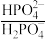 等缓冲对。常温下,水溶液中部分缓冲对的微粒浓度之比的对数值lgx[x表示
等缓冲对。常温下,水溶液中部分缓冲对的微粒浓度之比的对数值lgx[x表示 或
或 与溶液pH的关系如图所示。下列说法错误的是
与溶液pH的关系如图所示。下列说法错误的是
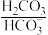 、
、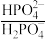 等缓冲对。常温下,水溶液中部分缓冲对的微粒浓度之比的对数值lgx[x表示
等缓冲对。常温下,水溶液中部分缓冲对的微粒浓度之比的对数值lgx[x表示 或
或 与溶液pH的关系如图所示。下列说法错误的是
与溶液pH的关系如图所示。下列说法错误的是
A.曲线I表示lg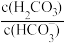 与溶液pH的变化关系 与溶液pH的变化关系 |
| B.Ka1(H2CO3)>Ka2(H3PO4) |
| C.a→b的过程中,水的电离程度逐渐减小 |
D.当pH增大时,lg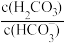 -lg -lg 的值逐渐增大 的值逐渐增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,下列实验探究方案不能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液 | 除去苯中的少量苯酚 |
| B | 向5 mL   溶液中滴加1 mL 溶液中滴加1 mL  KI溶液,再滴加几滴KSCN溶液,观察溶液颜色变化 KI溶液,再滴加几滴KSCN溶液,观察溶液颜色变化 |  和KI反应为可逆反应 和KI反应为可逆反应 |
| C | 在相同条件下,向一支试管中加入2 mL 5%  和1 mL 和1 mL  ,向另一支试管中加入2 mL 5% ,向另一支试管中加入2 mL 5%  和1 mL 和1 mL  溶液,观察并比较实验现象 溶液,观察并比较实验现象 |  对 对 分解速率的影响 分解速率的影响 |
| D | 用pH计测量  溶液和 溶液和 NaClO溶液,比较溶液pH大小 NaClO溶液,比较溶液pH大小 |  结合 结合 的能力比 的能力比 的弱 的弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 三氟乙酸酸性强于三氯乙酸 | F原子电负性大于Cl原子,吸电子能力强 |
| B | 常温下,铜与稀硫酸不反应,与稀硝酸反应 | 硝酸酸性强于硫酸 |
| C | 常温下溶解度: 大于 大于 |  水解程度大于 水解程度大于 |
| D |  、 、 混合气体通入 混合气体通入 溶液中产生的白色沉淀是 溶液中产生的白色沉淀是 | 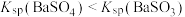 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,关于下列溶液的说法正确的是


| A.25℃时①10﹣3mol/L的盐酸;②pH=3的NH4Cl溶液;③pH=11的氨水中,水的电离程度为:②>③>① |
| B.pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) |
| C.pH=8.0的KHS溶液中,c(K+)>c(HS﹣)>c(OH﹣)>c(S2﹣)>c(H+) |
| D.图中a点溶液中各离子浓度的关系是:c(OH﹣)=c(H+)+c(CH3COO﹣)+c(CH3COOH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA为阿伏加德罗常数的数值。下列说法正确的是
| A.12 g NaHSO4晶体中含有阳离子数目为0.1NA |
| B.标准状况下,2.24LSO3中电子的数目为4NA |
| C.标准状况下,11.2LCl2通入水中,溶液中氯离子数为0.5NA |
| D.向1L0.1mol·L-1CH3COOH溶液通氨气至中性,铵根离子数为0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】25°C时,下列说法不正确的是
| A.等体积Na2CO3和NaHCO3溶液,以甲基橙作指示剂,达滴定终点时,消耗等量的HCl标准液,则NaHCO3浓度更大 |
| B.欲证明HA为弱酸,可将pH=3的HA溶液稀释为原体积的10倍后,测定pH>4 |
C.均为0.10 mol·L-1的Na2CO3、Na2SO3、Na2SO4溶液中阴离子的浓度依次减小〔已知:Ka(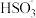 )=6.1×10-8;Ka( )=6.1×10-8;Ka( )=4.7×10-11〕 )=4.7×10-11〕 |
| D.常温下pH=11的纯碱溶液中水电离产生的n(H+)大于该溶液中n(H+) |
您最近一年使用:0次

 。某温度下,向c(H+)=1×10-6 mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的c(H+)=1×10-2 mol·L-1.下列对该溶液的叙述不正确的是
。某温度下,向c(H+)=1×10-6 mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的c(H+)=1×10-2 mol·L-1.下列对该溶液的叙述不正确的是


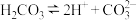
 ,漂白性增强的原因是
,漂白性增强的原因是