碳和氯元素及其化合物与人类的生产、生活密切相关。
(1)①一定条件下,氯气与氨气反应可以制备氯胺(NH2C1),已知部分化学键的键能:
则上述反应的热化学方程式为:____________ 。
②氯胺是一种长效缓释含氯消毒剂,有缓慢而持久的杀菌作用,可以杀死H7N9禽流感病毒,其消毒原理为与水缓慢反应生成强氧化性的物质,该反应的化学方程式为______________ :
Ⅱ、碳的化合物的转换在生产、生活中具有重要的应用。特别是CO2的低碳转型对抵御气候变化具有重要意义。
(2)在三个容积均为1L的密闭容器中以不同的氢碳比 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
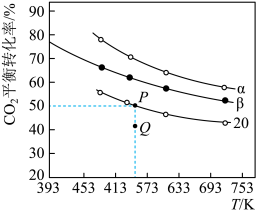
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示(α、β、2.0分别代表三种氢碳比时的变化曲线)。
C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示(α、β、2.0分别代表三种氢碳比时的变化曲线)。
请回答下列问题:
①反应的△H_____ 0,氢碳比α____ β,Q点v(正)_____ v(逆)(填“大于”或“小于”)
②若起始时,CO2的浓度为0.5mol·L-1;则P点对应温度的平衡常数的值为_______ 。
(3)已知:碳酸H2CO3,K1=4.3×10-7、K2=5.6×10-11、草酸H2C2O4,K1=6.0×10-2、K2=6.0×10-5
①下列微粒可以大量共存的是_______ (填字母)。
a. 、
、 b.H2CO3、
b.H2CO3、 c.
c.  、
、 d.H2C2O4、
d.H2C2O4、
②若将等物质的量浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子(除OH-外)浓度由大到小的顺序是_________ 。
③通过技术判断中和反应2Fe(OH)3(s)+3H2C2O4 2Fe3++6H2O+3
2Fe3++6H2O+3 在常温下能否发生反应
在常温下能否发生反应________ 。(已知:Ksp[Fe(OH)3]=1.0×10-39;66=4.67×104)
(1)①一定条件下,氯气与氨气反应可以制备氯胺(NH2C1),已知部分化学键的键能:
| 化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
| 键能/kJ·mol-1 | 391.3 | 243.0 | 191.2 | 431.8 |
则上述反应的热化学方程式为:
②氯胺是一种长效缓释含氯消毒剂,有缓慢而持久的杀菌作用,可以杀死H7N9禽流感病毒,其消毒原理为与水缓慢反应生成强氧化性的物质,该反应的化学方程式为
Ⅱ、碳的化合物的转换在生产、生活中具有重要的应用。特别是CO2的低碳转型对抵御气候变化具有重要意义。
(2)在三个容积均为1L的密闭容器中以不同的氢碳比
 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示(α、β、2.0分别代表三种氢碳比时的变化曲线)。
C2H4(g)+4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示(α、β、2.0分别代表三种氢碳比时的变化曲线)。请回答下列问题:
①反应的△H
②若起始时,CO2的浓度为0.5mol·L-1;则P点对应温度的平衡常数的值为
(3)已知:碳酸H2CO3,K1=4.3×10-7、K2=5.6×10-11、草酸H2C2O4,K1=6.0×10-2、K2=6.0×10-5
①下列微粒可以大量共存的是
a.
 、
、 b.H2CO3、
b.H2CO3、 c.
c.  、
、 d.H2C2O4、
d.H2C2O4、
②若将等物质的量浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子(除OH-外)浓度由大到小的顺序是
③通过技术判断中和反应2Fe(OH)3(s)+3H2C2O4
 2Fe3++6H2O+3
2Fe3++6H2O+3 在常温下能否发生反应
在常温下能否发生反应
更新时间:2017-03-17 23:48:24
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应,回答下列问题:
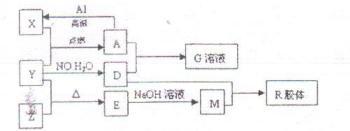
(1)组成单质Y的元素在周期表中的位置是__________ ;M中存在的化学键类型为_______ ;R的化学式是__________ 。
(2)已知A与1mol Al反应转化为X时(所有物质均为固体),放出akJ热量。写出该反应的热化学方程式:__________
(3)写出A和D的稀溶液反应生成G的离子方程式:__________

(1)组成单质Y的元素在周期表中的位置是
(2)已知A与1mol Al反应转化为X时(所有物质均为固体),放出akJ热量。写出该反应的热化学方程式:
(3)写出A和D的稀溶液反应生成G的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据要求,回答下列问题:
(1)有机物 M 经过太阳光光照可转化成有机物 N,转化过程如下:
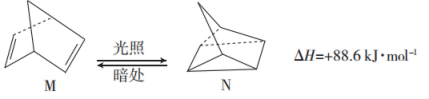
两者稳定性大小是:N______ M(填“>”“<”或“=”)。
(2)已知:CH3OH(l)的燃烧热△H1=-726.5 k·mol-1;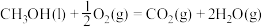 △H2。则△H1
△H2。则△H1______ △H2(填“>”“<”或“=”)。
(3)使 Cl2(g)和H2O(g)通过灼热的炭层,生成HCl(g)和 CO2(g)。每消耗1mol Cl2(g)放出 145 kJ 热量,则该反应的热化学方程式为______ 。
(4)火箭和导弹表面的涂层是耐高温的物质。将铝粉、二氧化钛粉和石墨粉按一定比例混合在高温下煅烧,所得物质可作耐高温材料,反应的热化学方程式为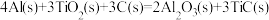 △H =-1176 kJ·mol-1。则反应过程中,每转移 2 mol 电子,放出的热量为
△H =-1176 kJ·mol-1。则反应过程中,每转移 2 mol 电子,放出的热量为______ kJ。
(1)有机物 M 经过太阳光光照可转化成有机物 N,转化过程如下:

两者稳定性大小是:N
(2)已知:CH3OH(l)的燃烧热△H1=-726.5 k·mol-1;
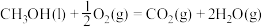 △H2。则△H1
△H2。则△H1(3)使 Cl2(g)和H2O(g)通过灼热的炭层,生成HCl(g)和 CO2(g)。每消耗1mol Cl2(g)放出 145 kJ 热量,则该反应的热化学方程式为
(4)火箭和导弹表面的涂层是耐高温的物质。将铝粉、二氧化钛粉和石墨粉按一定比例混合在高温下煅烧,所得物质可作耐高温材料,反应的热化学方程式为
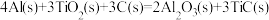 △H =-1176 kJ·mol-1。则反应过程中,每转移 2 mol 电子,放出的热量为
△H =-1176 kJ·mol-1。则反应过程中,每转移 2 mol 电子,放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2SO2(g)+O2(g) 2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:

(1)a=_____ kJ•mol-1.
(2)该反应常用V2O5作催化剂使图中ΔH_____ (填“升高”“降低”或“不变”)。
(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:_____ 。
(4)工业上用H2和Cl2反应制HCl,各键能数据为:H—H:436kJ/mol,Cl—Cl:243kJ/mol,H—Cl:431kJ/mol。该反应的热化学方程式是_____ 。
(5)已知:①C(s)+O2(g)=CO2(g) ΔH=ΔH1;②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;则TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=_____ 。(列出关于ΔH1、ΔH2、ΔH3的表达式)
 2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
2SO3(g) ΔH=akJ•mol-1,反应过程的能量变化如图所示。已知1molSO2(g)完全转化为1molSO3(g)放热99kJ。请回答:
(1)a=
(2)该反应常用V2O5作催化剂使图中ΔH
(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:
(4)工业上用H2和Cl2反应制HCl,各键能数据为:H—H:436kJ/mol,Cl—Cl:243kJ/mol,H—Cl:431kJ/mol。该反应的热化学方程式是
(5)已知:①C(s)+O2(g)=CO2(g) ΔH=ΔH1;②2CO(g)+O2(g)=2CO2(g) ΔH=ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=ΔH3;则TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为________ 热反应,且m+n______ p(填“>”、“=”或“<”)。
(2)减压时,A的质量分数__________ 。(填“增大”、“减小”或“不变”,下同)
(3)若容积不变加入B,则A的转化率__________ ,B的转化率__________ 。
(4)若升高温度,则平衡时B、C的浓度之比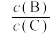 将
将__________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量__________ 。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色__________ ;而维持容器内压强不变,充入氖气时,混合物颜色__________ 。(填“变深”、“变浅”或“不变”)
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的逆反应为
(2)减压时,A的质量分数
(3)若容积不变加入B,则A的转化率
(4)若升高温度,则平衡时B、C的浓度之比
 将
将(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色
您最近一年使用:0次
【推荐2】CO用途广泛,工业应用时离不开平衡思想的指导:
Ⅰ.在一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H 2O,在催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0,体系中CO2的浓度随时间变化情况如图:
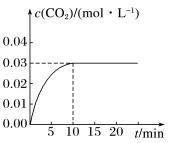
(1)该反应在800℃时的平衡常数K=_______ 。
(2)欲使平衡常数K增大,可采取的措施有_______ 。
(3)若保持温度和容器的体积不变,在上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率_______ (填“升高”“降低”或“不变”)。
(4)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13mol·L-1,则此时正、逆反应速率的大小:v正_______ v逆(填“>”“<”或“=”)。
Ⅱ.还原法炼铅,包含反应PbO(s)+CO(g)=Pb(s)+CO2(g) ΔH ,该反应的平衡常数的对数值与温度的关系如表:
(5)该反应的ΔH_______ 0(填“>”“<”或“=”)。
(6)当lgK=1时,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为_______ (保留两位有效数字);若再向容器中充入一定量的CO气体后,平衡发生移动,达到新平衡时,CO的百分含量_______ (填“增大”“减小”或“不变”)。
Ⅰ.在一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H 2O,在催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0,体系中CO2的浓度随时间变化情况如图:

(1)该反应在800℃时的平衡常数K=
(2)欲使平衡常数K增大,可采取的措施有
(3)若保持温度和容器的体积不变,在上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率
(4)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13mol·L-1,则此时正、逆反应速率的大小:v正
Ⅱ.还原法炼铅,包含反应PbO(s)+CO(g)=Pb(s)+CO2(g) ΔH ,该反应的平衡常数的对数值与温度的关系如表:
| 温度/℃ | 300 | 727 | 1227 |
| lgK | 6.17 | 2.87 | 1.24 |
(5)该反应的ΔH
(6)当lgK=1时,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业上用CO生产燃料甲醇。一定条件下发生反应:CO (g)+2H2 (g) CH3OH (g)。
CH3OH (g)。
(1)该反应的平衡常数表达式为:K=______________________
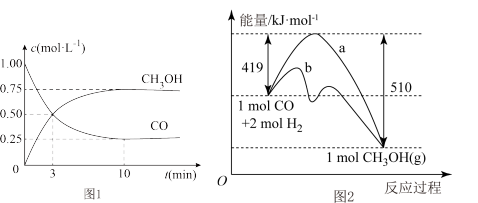
(2)图1是反应时CO和CH3OH(g)的浓度随时间的变化情况。从反应开始到平衡,用CO浓度变化表示的平均反应速率v(CO)=____________ 。
(3)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应是________ (填“吸热”或“放热”)反应,反应的热化学方程式是__________________________________________ 。
(4)适宜的催化剂能_______ (选填序号)。
a.改变反应的热效应 b.降低生产能耗 c.加快反应速率 d.提高反应物的转化率
(5)恒容条件下,下列措施中能使n (CH3OH)/n (CO)增大的有________ (选填序号)。
a. 升高温度 b. 使用催化剂 c.再充入2mol H2
 CH3OH (g)。
CH3OH (g)。
(1)该反应的平衡常数表达式为:K=
(2)图1是反应时CO和CH3OH(g)的浓度随时间的变化情况。从反应开始到平衡,用CO浓度变化表示的平均反应速率v(CO)=
(3)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应是
(4)适宜的催化剂能
a.改变反应的热效应 b.降低生产能耗 c.加快反应速率 d.提高反应物的转化率
(5)恒容条件下,下列措施中能使n (CH3OH)/n (CO)增大的有
a. 升高温度 b. 使用催化剂 c.再充入2mol H2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在密闭容器中进行如下反应:CO2(g)+C(s)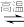 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
(1)增加C,平衡_____ ,c(CO2)____ 。
(2)缩小反应容器的容积,保持温度不变,则平衡____ ,c(CO2)_____ 。
(3)保持反应容器的容积和温度不变,通入N2,则平衡____ ,c(CO2)____ 。
 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。(1)增加C,平衡
(2)缩小反应容器的容积,保持温度不变,则平衡
(3)保持反应容器的容积和温度不变,通入N2,则平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】煤的洁净技术(包括固硫技术和脱硫技术两类)可有效降低燃煤废气中SO2的含量,已成为我国解决环境问题的主导技术之一。通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。石灰石是常用的固硫剂,固硫过程中涉及的部分反应如下:
①CaCO3(s) CaO(s) + CO2(g) △H1= +178.30kJ/mol
CaO(s) + CO2(g) △H1= +178.30kJ/mol
②CaO(s) + SO2(g) + 0.5O2(g) CaSO4(s) △H2= -501.92 kJ/mol
CaSO4(s) △H2= -501.92 kJ/mol
③CO(g) + 0.5O2(g) CO2(g) △H3
CO2(g) △H3
④CaSO4(s) + CO(g) CaO(s) + SO2(g) + CO2(g) △H4= +218.92kJ/mol
CaO(s) + SO2(g) + CO2(g) △H4= +218.92kJ/mol
(1)温度升高,反应①的化学平衡常数________ (填“增大”“减小”或“不变”)。
(2)△H3=________ kJ/mol。
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:________ 。
①CaCO3(s)
 CaO(s) + CO2(g) △H1= +178.30kJ/mol
CaO(s) + CO2(g) △H1= +178.30kJ/mol②CaO(s) + SO2(g) + 0.5O2(g)
 CaSO4(s) △H2= -501.92 kJ/mol
CaSO4(s) △H2= -501.92 kJ/mol③CO(g) + 0.5O2(g)
 CO2(g) △H3
CO2(g) △H3④CaSO4(s) + CO(g)
 CaO(s) + SO2(g) + CO2(g) △H4= +218.92kJ/mol
CaO(s) + SO2(g) + CO2(g) △H4= +218.92kJ/mol(1)温度升高,反应①的化学平衡常数
(2)△H3=
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:
您最近一年使用:0次
【推荐3】将0.4molN2O4充入2L固定容积的密闭容器中发生反应:N2O4(g) 2NO2(g) △H。分别在T1和T2时,测得NO2的物质的量随时间的变化如下图所示:
2NO2(g) △H。分别在T1和T2时,测得NO2的物质的量随时间的变化如下图所示:
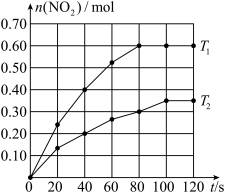
(1)该反应的△H_______ (填“>”“<”或“=”)0,理由是_______ 。
(2) T1时,40~80s内用N2O4的浓度变化表示的反应速率为_______ mol·L-1·s-1。
(3) T1时,反应的平衡常数K=_______ 。恒温恒容条件下,下列能说明该反应达到平衡状态的是_______ (填序号)。
①v(NO2)=2v(N2O4);②反应体系的总压强保持恒定不变;③混合气体的密度保持恒定不变;④体系颜色保持不变;⑤容器内NO2和N2O4的浓度相等
(4)T2时,改变条件使反应重新达到平衡时, 的值变小,则采取的措施可能是_______(填字母)。
的值变小,则采取的措施可能是_______(填字母)。
 2NO2(g) △H。分别在T1和T2时,测得NO2的物质的量随时间的变化如下图所示:
2NO2(g) △H。分别在T1和T2时,测得NO2的物质的量随时间的变化如下图所示:
(1)该反应的△H
(2) T1时,40~80s内用N2O4的浓度变化表示的反应速率为
(3) T1时,反应的平衡常数K=
①v(NO2)=2v(N2O4);②反应体系的总压强保持恒定不变;③混合气体的密度保持恒定不变;④体系颜色保持不变;⑤容器内NO2和N2O4的浓度相等
(4)T2时,改变条件使反应重新达到平衡时,
 的值变小,则采取的措施可能是_______(填字母)。
的值变小,则采取的措施可能是_______(填字母)。| A.增大 N2O4的起始浓度 | B.升高温度 |
| C.向混合气体中通入NO2 | D.使用高效催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】容积可变的密闭容器中,反应2SO2(g)十O2(g)  2SO3(g)在一定条件下达到平衡,完成下列填空:
2SO3(g)在一定条件下达到平衡,完成下列填空:
(1)工业上该反应是在________ (填设备名称)进行的,所用的催化剂是________ 。
(2)其他条件不变时,降低温度,平衡向正反应方向移动,则正反应为_______ (选填“吸热”“放热”)。下图为反应速率(ν)与时间(t)的关系,判断在t1时刻曲线发生变化的原因是__________ (选填编号)。

a.增大O2的浓度
b. 扩大容器体积
c. 加入催化剂
d. 升高温度
(3)改变条件后,平衡混合物中SO3的百分含量_______ (选填“增大”“减小”“不变”)。
(4)工业上用氨水来吸收SO2尾气,最终形成化肥(NH4)2 SO4,将(NH4)2 SO4固体溶于水,溶液呈_______ 性,理由是____________________ (用离子方程式表示),该溶液体系中存在多种守恒,请任写出其中一种守恒关系(用离子浓度表示) _______________________ 。
 2SO3(g)在一定条件下达到平衡,完成下列填空:
2SO3(g)在一定条件下达到平衡,完成下列填空:(1)工业上该反应是在
(2)其他条件不变时,降低温度,平衡向正反应方向移动,则正反应为

a.增大O2的浓度
b. 扩大容器体积
c. 加入催化剂
d. 升高温度
(3)改变条件后,平衡混合物中SO3的百分含量
(4)工业上用氨水来吸收SO2尾气,最终形成化肥(NH4)2 SO4,将(NH4)2 SO4固体溶于水,溶液呈
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)在海底和青藏高原都发现了名为“可燃冰”的环保型新能源,主要成分是 ,
, 在光照下可与
在光照下可与 反应,也可用
反应,也可用 和
和 制备二甲醚和甲醇等新型燃料。
制备二甲醚和甲醇等新型燃料。
①在一定条件下,发生反应: △H>0。在其它条件不变的情况下降低温度,逆反应速率将
△H>0。在其它条件不变的情况下降低温度,逆反应速率将_______ (填“增大”、“减小”或“不变”)。若在2L密闭容器中发生反应,T℃时,通入2mol  (g)和2mol
(g)和2mol  (g),反应达平衡后,生成1mol CO,此时向容器中加入1mol CO和3mol
(g),反应达平衡后,生成1mol CO,此时向容器中加入1mol CO和3mol  的混合气体(保持温度不变),则平衡将
的混合气体(保持温度不变),则平衡将_________ 移动(填“正向”、“逆向”或“不”)移动,达到新平衡后平衡常数K=_______ 。
② (g)和
(g)和 (g)生成的CO和
(g)生成的CO和 在一定条件下可发生如下反应:
在一定条件下可发生如下反应:
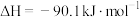 。恒容条件下,下列措施中能使
。恒容条件下,下列措施中能使 增大的有
增大的有_______ (选填序号)。
a.再充入1mol b.使用催化剂 c.再充入2mol CO d.升高温度
b.使用催化剂 c.再充入2mol CO d.升高温度
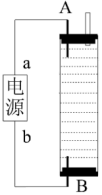
(2)①学生甲想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和NaCl溶液,通电时,为使 被完全吸收制得有较强杀菌能力的消毒液,设计了图的装置,a电极为该装置的
被完全吸收制得有较强杀菌能力的消毒液,设计了图的装置,a电极为该装置的______ 极,与a电极相连的电极反应为___________ ,该消毒液有效成分为_______ 。
② 极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的
极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的 沉淀,受到学生甲制作家用环保型消毒液发生器的启发,学生乙认为,此装置也可以用于制备较为纯净的
沉淀,受到学生甲制作家用环保型消毒液发生器的启发,学生乙认为,此装置也可以用于制备较为纯净的 沉淀,若通电后,B极表面有无色气泡产生,且溶液中产生大量的白色沉淀,较长时间不变色。下列说法正确的是
沉淀,若通电后,B极表面有无色气泡产生,且溶液中产生大量的白色沉淀,较长时间不变色。下列说法正确的是____________ 。
A.电源a是负极 B.电解质溶液一定是NaOH溶液
C.A、B两端都必须用铁做电极 D.B极附近溶液pH增大
(1)在海底和青藏高原都发现了名为“可燃冰”的环保型新能源,主要成分是
 ,
, 在光照下可与
在光照下可与 反应,也可用
反应,也可用 和
和 制备二甲醚和甲醇等新型燃料。
制备二甲醚和甲醇等新型燃料。①在一定条件下,发生反应:
 △H>0。在其它条件不变的情况下降低温度,逆反应速率将
△H>0。在其它条件不变的情况下降低温度,逆反应速率将 (g)和2mol
(g)和2mol  (g),反应达平衡后,生成1mol CO,此时向容器中加入1mol CO和3mol
(g),反应达平衡后,生成1mol CO,此时向容器中加入1mol CO和3mol  的混合气体(保持温度不变),则平衡将
的混合气体(保持温度不变),则平衡将②
 (g)和
(g)和 (g)生成的CO和
(g)生成的CO和 在一定条件下可发生如下反应:
在一定条件下可发生如下反应:
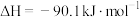 。恒容条件下,下列措施中能使
。恒容条件下,下列措施中能使 增大的有
增大的有a.再充入1mol
 b.使用催化剂 c.再充入2mol CO d.升高温度
b.使用催化剂 c.再充入2mol CO d.升高温度(2)①学生甲想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和NaCl溶液,通电时,为使
 被完全吸收制得有较强杀菌能力的消毒液,设计了图的装置,a电极为该装置的
被完全吸收制得有较强杀菌能力的消毒液,设计了图的装置,a电极为该装置的
②
 极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的
极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的 沉淀,受到学生甲制作家用环保型消毒液发生器的启发,学生乙认为,此装置也可以用于制备较为纯净的
沉淀,受到学生甲制作家用环保型消毒液发生器的启发,学生乙认为,此装置也可以用于制备较为纯净的 沉淀,若通电后,B极表面有无色气泡产生,且溶液中产生大量的白色沉淀,较长时间不变色。下列说法正确的是
沉淀,若通电后,B极表面有无色气泡产生,且溶液中产生大量的白色沉淀,较长时间不变色。下列说法正确的是A.电源a是负极 B.电解质溶液一定是NaOH溶液
C.A、B两端都必须用铁做电极 D.B极附近溶液pH增大
您最近一年使用:0次

 (吸热反应)
(吸热反应)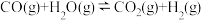 (放热反应)
(放热反应) 和
和 。反应平衡时,
。反应平衡时, 的物质的量为
的物质的量为 ,
, 的物质的量为
的物质的量为 。
。 的体积分数可能大于
的体积分数可能大于
 的转化率
的转化率

