硫酰氯(SO2C12)和亚硫酰氯(SOCl2)均是重要的化工试剂,遇水发生剧烈反应,常用作脱水剂。
已知SO2Cl2(g)+SCl2(g) 2SOCl2(g) K1 △H=-5.6kJ/mol (I)
2SOCl2(g) K1 △H=-5.6kJ/mol (I)
SOCl2(g) SO2(g)+Cl2(g) K2 △H=+471.7kJ/mol (Ⅱ)
SO2(g)+Cl2(g) K2 △H=+471.7kJ/mol (Ⅱ)
(1)SO2(g)+Cl2(g) +SCl2(g) 2SOCl2(g)的平衡常数K=
2SOCl2(g)的平衡常数K=_____ (用K1、K2表示),△H=______ kJ/mol。
(2)若在绝热、恒容的密闭容器中,投入一定量的SO2C12(g)和SCl2(g),发生反应(I),下列示意图能说明t1时刻反应达到平衡状态的是____________ (填序号)。
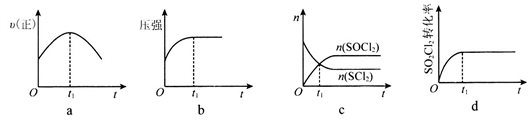
(3)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol SO2C12,10 min后反应(II)达到平衡。测得10 min内v(SO2)=7.5×10-3mol.L-1.min-1。则平衡时SO2C12的转化率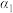 =
=___________ 。若其它条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时SO2的转化率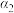
______ 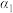 (填“>”、“<”或“=”)。若要增大SO2C12的转化率,可以采取的措施有
(填“>”、“<”或“=”)。若要增大SO2C12的转化率,可以采取的措施有_________ (列举一种)。
(4)将SOCl2与AlCl3·6H2O混合并加热,可得到无水AlC13,试解释原因____________________ 。
(5)若用SOC12作FeCl3·nH2O的脱水剂,设计实验证明脱水过程中发生了氧化还原反应____________ 。
(6)已知SO2C12遇水强烈水解生成两种强酸。向SO2C12溶于水所得溶液中逐滴加入AgNO3溶液,最先生成的沉淀是_____ ;当第二种离子开始沉淀时,溶液中c(Ag+)为0.01 mol·L-1,则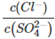 =
=______ 。
[已知Ksp(AgC1)=1.8×10-10,Ksp(Ag2SO4)=1.2×10-5]
已知SO2Cl2(g)+SCl2(g)
 2SOCl2(g) K1 △H=-5.6kJ/mol (I)
2SOCl2(g) K1 △H=-5.6kJ/mol (I)SOCl2(g)
 SO2(g)+Cl2(g) K2 △H=+471.7kJ/mol (Ⅱ)
SO2(g)+Cl2(g) K2 △H=+471.7kJ/mol (Ⅱ)(1)SO2(g)+Cl2(g) +SCl2(g)
 2SOCl2(g)的平衡常数K=
2SOCl2(g)的平衡常数K=(2)若在绝热、恒容的密闭容器中,投入一定量的SO2C12(g)和SCl2(g),发生反应(I),下列示意图能说明t1时刻反应达到平衡状态的是

(3)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol SO2C12,10 min后反应(II)达到平衡。测得10 min内v(SO2)=7.5×10-3mol.L-1.min-1。则平衡时SO2C12的转化率
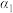 =
=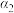
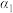 (填“>”、“<”或“=”)。若要增大SO2C12的转化率,可以采取的措施有
(填“>”、“<”或“=”)。若要增大SO2C12的转化率,可以采取的措施有(4)将SOCl2与AlCl3·6H2O混合并加热,可得到无水AlC13,试解释原因
(5)若用SOC12作FeCl3·nH2O的脱水剂,设计实验证明脱水过程中发生了氧化还原反应
(6)已知SO2C12遇水强烈水解生成两种强酸。向SO2C12溶于水所得溶液中逐滴加入AgNO3溶液,最先生成的沉淀是
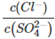 =
=[已知Ksp(AgC1)=1.8×10-10,Ksp(Ag2SO4)=1.2×10-5]
更新时间:2017-05-12 11:02:59
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】利用化学反应原理研究碳、硫及其化合物的性质具有重要意义。
(1)工业上用炭还原辉铜矿(主要成分是Cu2S),可制取金属铜。
已知反应的热化学方程式如下:
C(s)+S2 (g) ═CS2 (g) △H1=150 KJ/mol
Cu2S(s)+H2 (g) ═2Cu(s)+H2S (g) △H2=59.5KJ/mol
2H2S (g) ═2H2 (g) +S2 (g) △H3=170KJ/mol
通过计算,可知用炭还原Cu2S 制取金属铜和CS2(g) 的热化学方程式为___________ 。
(2)为研究反应2H2S(g) 2H2(g)+S2(g)对上述工业过程的影响,兴趣小组进行如下探究:
2H2(g)+S2(g)对上述工业过程的影响,兴趣小组进行如下探究:
①向三个体积均为1L的恒容密闭容器中分别加入1molH2S,进行H2S分解实验。不同温度下测得H2S 的转化率与时间的关系如图1所示:

T1温度下,0~5min S2(g)的平均反应速率v(S2)=____________ mol.L-1.min-1,反应平衡常数K=_____ mol•L-1.温度T1、T2、T3由高到低的顺序是__________ 。
②T4温度时,向1L的恒容密闭容器中加入1.8molH2(g)、1.2molS2(g),达到平衡后测得S2(g)和H2S(g)的浓度相等,则T4_____ T1(填“<”、“=”或“>”)。
(3)T℃时,向某浓度的草酸溶液中逐滴加入一定浓度的NaOH 溶液,所得溶液中三种微粒H2C2O4、HC2O4-、C2O42-的物质的量分数(δ) 与pH的关系如图2所示:
①草酸的电离常数分别为K1与K2,则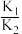 =
=_____ 。
②按投料比n(Na2C2O4):n(NaHC2O4)=2:1配成溶液,下列有关该溶液的叙述正确的是_____ (填序号)。
A.该溶液的pH为4.2
B.3c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-)
C.3c(Na+)=5[c(HC2O4-)+c(C2O42-)+c(H2C2O4)]
D.3c(OH-)+c(C2O42-)=3c(H+)+2c(HC2O4-)+5c(H2C2O4)
(4)含碳的甲醇(CH3OH)的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。
①写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:___________________ 。
②常温下,向100 mL0.1mol/L的NaOH溶液中通入一定量的CO2。为探究反应后混合溶液的成分,向其中逐滴加入0.1 mol/L的HCl溶液。溶液产生气体前,消耗V( HCl)=V1;溶液刚好不再产生气体时,消耗V( HCl) =V2。当V1 <V2 <2Vl时,混合溶液中溶质的成分为________
(1)工业上用炭还原辉铜矿(主要成分是Cu2S),可制取金属铜。
已知反应的热化学方程式如下:
C(s)+S2 (g) ═CS2 (g) △H1=150 KJ/mol
Cu2S(s)+H2 (g) ═2Cu(s)+H2S (g) △H2=59.5KJ/mol
2H2S (g) ═2H2 (g) +S2 (g) △H3=170KJ/mol
通过计算,可知用炭还原Cu2S 制取金属铜和CS2(g) 的热化学方程式为
(2)为研究反应2H2S(g)
 2H2(g)+S2(g)对上述工业过程的影响,兴趣小组进行如下探究:
2H2(g)+S2(g)对上述工业过程的影响,兴趣小组进行如下探究:①向三个体积均为1L的恒容密闭容器中分别加入1molH2S,进行H2S分解实验。不同温度下测得H2S 的转化率与时间的关系如图1所示:

T1温度下,0~5min S2(g)的平均反应速率v(S2)=
②T4温度时,向1L的恒容密闭容器中加入1.8molH2(g)、1.2molS2(g),达到平衡后测得S2(g)和H2S(g)的浓度相等,则T4
(3)T℃时,向某浓度的草酸溶液中逐滴加入一定浓度的NaOH 溶液,所得溶液中三种微粒H2C2O4、HC2O4-、C2O42-的物质的量分数(δ) 与pH的关系如图2所示:
①草酸的电离常数分别为K1与K2,则
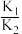 =
=②按投料比n(Na2C2O4):n(NaHC2O4)=2:1配成溶液,下列有关该溶液的叙述正确的是
A.该溶液的pH为4.2
B.3c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-)
C.3c(Na+)=5[c(HC2O4-)+c(C2O42-)+c(H2C2O4)]
D.3c(OH-)+c(C2O42-)=3c(H+)+2c(HC2O4-)+5c(H2C2O4)
(4)含碳的甲醇(CH3OH)的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。
①写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:
②常温下,向100 mL0.1mol/L的NaOH溶液中通入一定量的CO2。为探究反应后混合溶液的成分,向其中逐滴加入0.1 mol/L的HCl溶液。溶液产生气体前,消耗V( HCl)=V1;溶液刚好不再产生气体时,消耗V( HCl) =V2。当V1 <V2 <2Vl时,混合溶液中溶质的成分为
您最近一年使用:0次
【推荐2】“碳达峰·碳中和”是我国社会发展重大战略之一,研究甲烷的燃烧技术可减少CO2的排放并实现资源利用。
Ⅰ.甲烷直接燃烧可达到2800℃左右的高温,主要发生反应ⅰ,可能发生副反应ⅱ。
ⅰ.
ⅱ.
ⅲ.……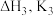
(1)利用 和
和 计算
计算 时,反应ⅲ是
时,反应ⅲ是_______ ;
_______ (用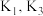 表示)。
表示)。
Ⅱ.化学链燃烧技术有利于 的捕获和综合利用。较高温度下,将恒定流速的
的捕获和综合利用。较高温度下,将恒定流速的 在
在 时刻通入反应器与载氧体
时刻通入反应器与载氧体 反应,原理如图1所示,流出气体中各组分的浓度随反应时间变化如图2所示。待反应①完成后,
反应,原理如图1所示,流出气体中各组分的浓度随反应时间变化如图2所示。待反应①完成后, 时刻向反应器中通入一段时间氩气,
时刻向反应器中通入一段时间氩气, 时刻再通入一段时间空气,发生反应②,实现载氧体的循环再生。
时刻再通入一段时间空气,发生反应②,实现载氧体的循环再生。
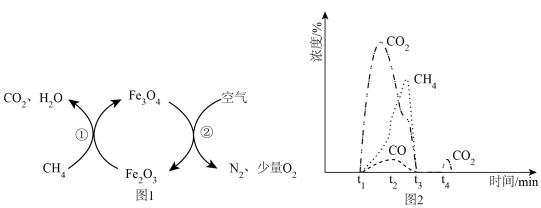
(2)①的化学反应方程式是_______ ,载氧体的主要作用是_______ (填“提供电子”或“接受电子”)。
(3)恒压条件下,反应①在某密闭容器中反应,平衡后通入 气,测得一段时间内
气,测得一段时间内 物质的量上升,其原因是
物质的量上升,其原因是_______ 。
(4)结合图2,依据 时刻产生
时刻产生 ,用化学方程式及简要文字解释
,用化学方程式及简要文字解释 时刻流出
时刻流出 速率突然增大的可能原因
速率突然增大的可能原因_______ 。
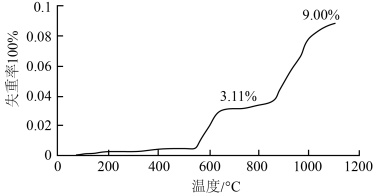
已知:失重率=
Ⅲ.某同学采用重量分析法探究载氧体的还原产物及循环效果,实验过程如下:在装置中放置一定量的 ,加热条件下通入足量
,加热条件下通入足量 ,充分均匀反应,分析固体失重率。
,充分均匀反应,分析固体失重率。
(5) 时载氧体的还原产物主要为
时载氧体的还原产物主要为 。
。结合简单计算 说明 时,载氧体的主要还原产物为
时,载氧体的主要还原产物为_______ ,依据是_______ 。
Ⅳ.有人设想利用“ ”间的转化实现
”间的转化实现 的化学链燃烧过程,按图1的呈现方式。
的化学链燃烧过程,按图1的呈现方式。
(6)将该转化关系在虚线框内画出_______ 。

Ⅰ.甲烷直接燃烧可达到2800℃左右的高温,主要发生反应ⅰ,可能发生副反应ⅱ。
ⅰ.

ⅱ.

ⅲ.……
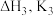
(1)利用
 和
和 计算
计算 时,反应ⅲ是
时,反应ⅲ是
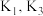 表示)。
表示)。Ⅱ.化学链燃烧技术有利于
 的捕获和综合利用。较高温度下,将恒定流速的
的捕获和综合利用。较高温度下,将恒定流速的 在
在 时刻通入反应器与载氧体
时刻通入反应器与载氧体 反应,原理如图1所示,流出气体中各组分的浓度随反应时间变化如图2所示。待反应①完成后,
反应,原理如图1所示,流出气体中各组分的浓度随反应时间变化如图2所示。待反应①完成后, 时刻向反应器中通入一段时间氩气,
时刻向反应器中通入一段时间氩气, 时刻再通入一段时间空气,发生反应②,实现载氧体的循环再生。
时刻再通入一段时间空气,发生反应②,实现载氧体的循环再生。
(2)①的化学反应方程式是
(3)恒压条件下,反应①在某密闭容器中反应,平衡后通入
 气,测得一段时间内
气,测得一段时间内 物质的量上升,其原因是
物质的量上升,其原因是(4)结合图2,依据
 时刻产生
时刻产生 ,用化学方程式及简要文字解释
,用化学方程式及简要文字解释 时刻流出
时刻流出 速率突然增大的可能原因
速率突然增大的可能原因
已知:失重率=

Ⅲ.某同学采用重量分析法探究载氧体的还原产物及循环效果,实验过程如下:在装置中放置一定量的
 ,加热条件下通入足量
,加热条件下通入足量 ,充分均匀反应,分析固体失重率。
,充分均匀反应,分析固体失重率。(5)
 时载氧体的还原产物主要为
时载氧体的还原产物主要为 。
。 时,载氧体的主要还原产物为
时,载氧体的主要还原产物为Ⅳ.有人设想利用“
 ”间的转化实现
”间的转化实现 的化学链燃烧过程,按图1的呈现方式。
的化学链燃烧过程,按图1的呈现方式。(6)将该转化关系在虚线框内画出

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】甲烷和二氧化碳在催化剂作用下可以转化为合成气(主要包含 、
、 和少量
和少量 的混合气体)。
的混合气体)。
主反应为:Ⅰ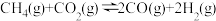
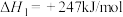
主要副反应有:Ⅱ
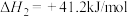
Ⅲ
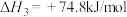
Ⅳ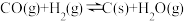
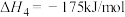
(1)写出甲烷和水蒸气反应生成 和氢气的热化学方程式
和氢气的热化学方程式___________ 。
(2)下列说法正确的是___________ 。
A.其它条件一定,减小压强,有利于主反应平衡Ⅰ向逆方向进行,平衡常数减小
B.其它条件一定时,不断增大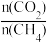 的值,不仅可以提高
的值,不仅可以提高 的转化率,
的转化率, 和
和 百分含量也会更高
百分含量也会更高
C.使用催化剂不能提高主反应的平衡转化率
D.由主反应知,及时分离出产物,平衡正向进行,正反应速率提高
(3)在压强为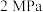 ,投料比为1∶1的条件下,图a是原料的平衡转化率随温度变化的变化曲线;图b是不同温度下,反应平衡时气体产物的体积分数随温度变化的变化曲线。
,投料比为1∶1的条件下,图a是原料的平衡转化率随温度变化的变化曲线;图b是不同温度下,反应平衡时气体产物的体积分数随温度变化的变化曲线。
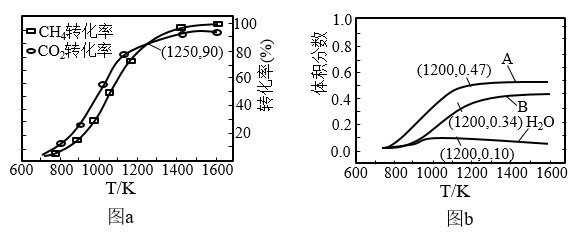
②当温度低于1250 K时,原料的平衡转化率 小于
小于 ,原因可能是
,原因可能是___________ 。
②图b中A和B分别代表产物___________ 和___________ ,当温度高于1050 K, 的含量随温度升高而下降的主要原因是
的含量随温度升高而下降的主要原因是___________ 。
③温度为1200 K时,反应Ⅳ的平衡常数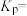
___________ (用分压计算,分压=总压×物体积分数,保留两位小数。)
(4)在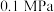 、
、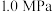 和
和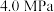 压强下,
压强下, 平衡转化率
平衡转化率 随温度的变化如图所示,则
随温度的变化如图所示,则
___________  (填“>”或“<”或“=”),判断的依据是
(填“>”或“<”或“=”),判断的依据是___________ 。

 、
、 和少量
和少量 的混合气体)。
的混合气体)。主反应为:Ⅰ
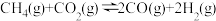
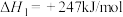
主要副反应有:Ⅱ

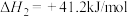
Ⅲ

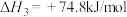
Ⅳ
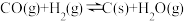
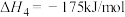
(1)写出甲烷和水蒸气反应生成
 和氢气的热化学方程式
和氢气的热化学方程式(2)下列说法正确的是
A.其它条件一定,减小压强,有利于主反应平衡Ⅰ向逆方向进行,平衡常数减小
B.其它条件一定时,不断增大
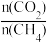 的值,不仅可以提高
的值,不仅可以提高 的转化率,
的转化率, 和
和 百分含量也会更高
百分含量也会更高C.使用催化剂不能提高主反应的平衡转化率
D.由主反应知,及时分离出产物,平衡正向进行,正反应速率提高
(3)在压强为
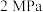 ,投料比为1∶1的条件下,图a是原料的平衡转化率随温度变化的变化曲线;图b是不同温度下,反应平衡时气体产物的体积分数随温度变化的变化曲线。
,投料比为1∶1的条件下,图a是原料的平衡转化率随温度变化的变化曲线;图b是不同温度下,反应平衡时气体产物的体积分数随温度变化的变化曲线。
②当温度低于1250 K时,原料的平衡转化率
 小于
小于 ,原因可能是
,原因可能是②图b中A和B分别代表产物
 的含量随温度升高而下降的主要原因是
的含量随温度升高而下降的主要原因是③温度为1200 K时,反应Ⅳ的平衡常数
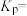
(4)在
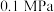 、
、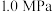 和
和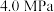 压强下,
压强下, 平衡转化率
平衡转化率 随温度的变化如图所示,则
随温度的变化如图所示,则
 (填“>”或“<”或“=”),判断的依据是
(填“>”或“<”或“=”),判断的依据是
您最近一年使用:0次
【推荐1】I.2022年3月30日,我国在酒泉卫星发射中心用长征十一号运载火箭,成功将天平二号A、B、C卫星发射升空。卫星,火箭的第一、二级发动机中,所用的燃料为偏二甲肼和四氧化二氮,偏二甲肼可用肼来制备。用肼 作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①
②
(1)写出气态肼和 反应的热化学方程式:
反应的热化学方程式:_____ 。
(2)已知 和
和 反应生成
反应生成 吸收
吸收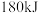 能量,反应过程中能量变化如下图所示。
能量,反应过程中能量变化如下图所示。
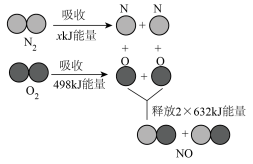
根据图示回答下列问题:断裂 吸收的能量x值为
吸收的能量x值为_____ 。
Ⅱ. (红棕色)和
(红棕色)和 (无色)之间发生反应:
(无色)之间发生反应: 。将一定量
。将一定量 气体充入体积为2L的恒容密闭容器中,控制反应温度为T。
气体充入体积为2L的恒容密闭容器中,控制反应温度为T。
(3)下列可以说明该反应达到平衡的是_____。
(4)在温度为T的条件下,向该恒容密闭容器中充入 随时间的变化曲线如图所示。
随时间的变化曲线如图所示。

①在图中画出 时间段内,
时间段内,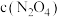 随时间的变化曲线
随时间的变化曲线_____ 。
②1~4四个点中, 的点有
的点有_____ 。
③反应进行到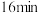 时,
时, 的转化率是
的转化率是_____ 。
④下列措施能使该反应速率加快的是_____ 。
A.增大 的浓度 B.增大容器体积 C.加入合适的催化剂 D.恒容条件下充入
的浓度 B.增大容器体积 C.加入合适的催化剂 D.恒容条件下充入
 作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:①

②

(1)写出气态肼和
 反应的热化学方程式:
反应的热化学方程式:(2)已知
 和
和 反应生成
反应生成 吸收
吸收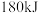 能量,反应过程中能量变化如下图所示。
能量,反应过程中能量变化如下图所示。
根据图示回答下列问题:断裂
 吸收的能量x值为
吸收的能量x值为Ⅱ.
 (红棕色)和
(红棕色)和 (无色)之间发生反应:
(无色)之间发生反应: 。将一定量
。将一定量 气体充入体积为2L的恒容密闭容器中,控制反应温度为T。
气体充入体积为2L的恒容密闭容器中,控制反应温度为T。(3)下列可以说明该反应达到平衡的是_____。
A.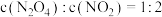 | B. |
| C.容器内气体的颜色不再变化 | D.混合气体的压强不再变化 |
 随时间的变化曲线如图所示。
随时间的变化曲线如图所示。
①在图中画出
 时间段内,
时间段内,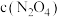 随时间的变化曲线
随时间的变化曲线②1~4四个点中,
 的点有
的点有③反应进行到
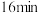 时,
时, 的转化率是
的转化率是④下列措施能使该反应速率加快的是
A.增大
 的浓度 B.增大容器体积 C.加入合适的催化剂 D.恒容条件下充入
的浓度 B.增大容器体积 C.加入合适的催化剂 D.恒容条件下充入
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氨的用途十分广泛,是现代工业、农业生产最基础的化工原料之一。
I.以氨为原料可生产尿素:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) ΔH, 其反应分两步进行:
CO(NH2)2(l)+H2O(g) ΔH, 其反应分两步进行:
①2NH3(g)+CO2(g) NH2COONH4(l) ΔH1=−117kJ·mol−1
NH2COONH4(l) ΔH1=−117kJ·mol−1
②NH2COONH4(l) CO(NH2)2(l)+H2O(g) ΔH2=+15kJ·mol−1
CO(NH2)2(l)+H2O(g) ΔH2=+15kJ·mol−1
(1)生产尿素的决速步骤是第二步,可判断活化能较小的是_______ (填“①”或“②”)。
(2)总反应的ΔH=_______ 。
Ⅱ.传统的“哈伯法”合成氨原理为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol−1 ΔS=−200J·K−1·mol−1
2NH3(g) ΔH=-92.4kJ·mol−1 ΔS=−200J·K−1·mol−1
(3)上述反应在常温下_______ (填“能”或“不能”)自发进行。
(4)一定条件下,在恒温恒容的密闭容器中充入等物质的量的N2和H2发生反应生成NH3下列状态能说明反应达到平衡的是_______(填标号)。
(5)科研小组模拟不同条件下的合成氨反应,向体积可变的密闭容器中充入6mol N2和10mol H2,不同温度下平衡时氨气的体积分数与总压强(p)的关系如图所示。
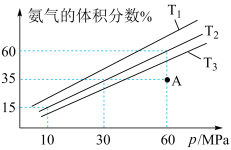
①T1、T2、T3由小到大的顺序为_______ 。
②在T2、60MPa条件下,平衡时N2的转化率为_______ %;平衡常数Kp=_______ (保留两位有效数字)。(用平衡分压代替平衡浓度,分压=总压x物质的量分数)
I.以氨为原料可生产尿素:2NH3(g)+CO2(g)
 CO(NH2)2(l)+H2O(g) ΔH, 其反应分两步进行:
CO(NH2)2(l)+H2O(g) ΔH, 其反应分两步进行:①2NH3(g)+CO2(g)
 NH2COONH4(l) ΔH1=−117kJ·mol−1
NH2COONH4(l) ΔH1=−117kJ·mol−1②NH2COONH4(l)
 CO(NH2)2(l)+H2O(g) ΔH2=+15kJ·mol−1
CO(NH2)2(l)+H2O(g) ΔH2=+15kJ·mol−1(1)生产尿素的决速步骤是第二步,可判断活化能较小的是
(2)总反应的ΔH=
Ⅱ.传统的“哈伯法”合成氨原理为:N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4kJ·mol−1 ΔS=−200J·K−1·mol−1
2NH3(g) ΔH=-92.4kJ·mol−1 ΔS=−200J·K−1·mol−1(3)上述反应在常温下
(4)一定条件下,在恒温恒容的密闭容器中充入等物质的量的N2和H2发生反应生成NH3下列状态能说明反应达到平衡的是_______(填标号)。
| A.容器内气体的平均摩尔质量不变 | B.N2的体积分数不变 |
| C.混合气体的颜色不再改变 | D.3v正(NH3)=2v逆(H2) |

①T1、T2、T3由小到大的顺序为
②在T2、60MPa条件下,平衡时N2的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】将一定量纯净的氨基甲酸铵( )固体置于密闭容器中(假设容器容积不变),在一定温度下使其达到分解平衡:
)固体置于密闭容器中(假设容器容积不变),在一定温度下使其达到分解平衡: (正反应为吸热反应)。回答下列问题:
(正反应为吸热反应)。回答下列问题:
(1)可以判断该分解反应已经达到化学平衡状态的是__________________ (填标号,双选)。
a. b.密闭容器中总压强不变
b.密闭容器中总压强不变
c.密闭容器中混合气体的密度不变 d.密闭容器中氨的体积分数不变
(2)当反应达到平衡状态时,其他条件不变,在容器中充入少量HCl气体,平衡将向____________ (填“正反应方向”或“逆反应方向”,下同)移动。当反应达到平衡状态时,其他条件不变,温度升高,平衡将向__________________________ 移动。
 )固体置于密闭容器中(假设容器容积不变),在一定温度下使其达到分解平衡:
)固体置于密闭容器中(假设容器容积不变),在一定温度下使其达到分解平衡: (正反应为吸热反应)。回答下列问题:
(正反应为吸热反应)。回答下列问题:(1)可以判断该分解反应已经达到化学平衡状态的是
a.
 b.密闭容器中总压强不变
b.密闭容器中总压强不变c.密闭容器中混合气体的密度不变 d.密闭容器中氨的体积分数不变
(2)当反应达到平衡状态时,其他条件不变,在容器中充入少量HCl气体,平衡将向
您最近一年使用:0次
【推荐1】碳的化合物的转换在生产、生活中具有重要的应用,如航天员呼吸产生的 用Sabatier反应处理,实现空间站中
用Sabatier反应处理,实现空间站中 的循环利用。
的循环利用。
Sabatier反应: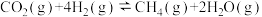 ;
;
水电解反应: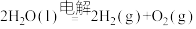 。
。
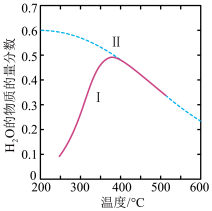
I.将原料气按 置于密闭容器中发生Sabatier反应,测得
置于密闭容器中发生Sabatier反应,测得 的物质的量分数与温度的关系如下图所示(曲线Ⅱ表示平衡曲线)。
的物质的量分数与温度的关系如下图所示(曲线Ⅱ表示平衡曲线)。
(1)在密闭恒温(高于100℃)恒容装置中进行该反应,下列能说明达到平衡状态的是_____ 。
A.混合气体密度不再改变B.混合气体压强不再改变
C.混合气体平均摩尔质量不再改变D.
(2)380℃以后曲线I与曲线Ⅱ重合并且下降的原因是_________________ 。
(3)200℃达到平衡时体系的总压强为p,该反应平衡常数 的计算表达式为
的计算表达式为_____ 。(不必化简,用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数)
物质的量分数)
(4)Sabatier反应在空间站运行时,下列措施能提高 转化率的是
转化率的是_____ (填标号)。
A.适当减压B.合理控制反应器中气体的流速
C.反应器前段加热,后段冷却D.提高原料气中 所占比例
所占比例
Ⅱ.一种新的循环利用方案是用Bosch反应代替Sabatier反应。Bosch反应中 和
和 生成了C和
生成了C和 。
。
(5)①已知 、
、 的生成焓分别为
的生成焓分别为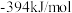 、
、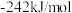 ,Bosch反应的热化学方程式为
,Bosch反应的热化学方程式为_________________ 。(生成焓指一定条件下由对应单质生成1mol化合物时的反应热)
(6)一定条件下,若无催化剂Bosch反应必须在高温下才能启动,而使用催化剂,则在较低温度下就能启动,试分析原因是_________________ 。
(7)Bosch反应的优点是_________________ 。
 用Sabatier反应处理,实现空间站中
用Sabatier反应处理,实现空间站中 的循环利用。
的循环利用。Sabatier反应:
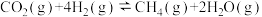 ;
;水电解反应:
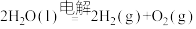 。
。I.将原料气按
 置于密闭容器中发生Sabatier反应,测得
置于密闭容器中发生Sabatier反应,测得 的物质的量分数与温度的关系如下图所示(曲线Ⅱ表示平衡曲线)。
的物质的量分数与温度的关系如下图所示(曲线Ⅱ表示平衡曲线)。
(1)在密闭恒温(高于100℃)恒容装置中进行该反应,下列能说明达到平衡状态的是
A.混合气体密度不再改变B.混合气体压强不再改变
C.混合气体平均摩尔质量不再改变D.

(2)380℃以后曲线I与曲线Ⅱ重合并且下降的原因是
(3)200℃达到平衡时体系的总压强为p,该反应平衡常数
 的计算表达式为
的计算表达式为 总压
总压 物质的量分数)
物质的量分数)(4)Sabatier反应在空间站运行时,下列措施能提高
 转化率的是
转化率的是A.适当减压B.合理控制反应器中气体的流速
C.反应器前段加热,后段冷却D.提高原料气中
 所占比例
所占比例Ⅱ.一种新的循环利用方案是用Bosch反应代替Sabatier反应。Bosch反应中
 和
和 生成了C和
生成了C和 。
。(5)①已知
 、
、 的生成焓分别为
的生成焓分别为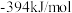 、
、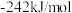 ,Bosch反应的热化学方程式为
,Bosch反应的热化学方程式为(6)一定条件下,若无催化剂Bosch反应必须在高温下才能启动,而使用催化剂,则在较低温度下就能启动,试分析原因是
(7)Bosch反应的优点是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为_______ 。利用反应6NO2+8NH3 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是______ L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH1=﹣196.6 kJ•mol-1
2SO3(g) ΔH1=﹣196.6 kJ•mol-1
2NO(g)+O2(g) 2NO2(g) ΔH2=﹣113.0kJ•mol-1
2NO2(g) ΔH2=﹣113.0kJ•mol-1
则反应NO2(g)+ SO2(g) SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=________ kJ•mol-1。
一定条件下,将2molNO2与2molSO2置于容积固定的恒温密闭容器中发生上述反应,下列能说明反应达到平衡状态的是__________ (填字母)
a.混合气体密度保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1molSO3的同时生成1molNO2
该反应达平衡状态后,若再向该容器充入1molNO2与1molSO2,则SO2的转化率将_______ (填“增大”“减小”或“不变”)。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g) ΔH=﹣a kJ•mol-1。在一定温度下,将1molCO(g)和2molH2(g)充入到体积为10L的密闭容器中,发生反应。经过5min达到平衡,此时容器内压强为反应前的0.8倍。则v(CH3OH)为
CH3OH(g) ΔH=﹣a kJ•mol-1。在一定温度下,将1molCO(g)和2molH2(g)充入到体积为10L的密闭容器中,发生反应。经过5min达到平衡,此时容器内压强为反应前的0.8倍。则v(CH3OH)为_______ ,正反应放出的热量为______ 。
(4)已知N2O4(g) 2NO2(g) ΔH>0,现将1molN2O4充入一恒压密闭容器中,下列示意图能说明反应达到平衡状态的是
2NO2(g) ΔH>0,现将1molN2O4充入一恒压密闭容器中,下列示意图能说明反应达到平衡状态的是_______ 。
A.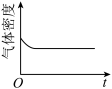 B.
B.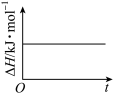 C.
C.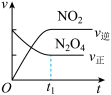 D.
D.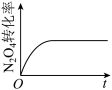
(1)NO2可用水吸收,相应的化学反应方程式为
 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是(2)已知:2SO2(g)+O2(g)
 2SO3(g) ΔH1=﹣196.6 kJ•mol-1
2SO3(g) ΔH1=﹣196.6 kJ•mol-12NO(g)+O2(g)
 2NO2(g) ΔH2=﹣113.0kJ•mol-1
2NO2(g) ΔH2=﹣113.0kJ•mol-1则反应NO2(g)+ SO2(g)
 SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=一定条件下,将2molNO2与2molSO2置于容积固定的恒温密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.混合气体密度保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1molSO3的同时生成1molNO2
该反应达平衡状态后,若再向该容器充入1molNO2与1molSO2,则SO2的转化率将
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)
 CH3OH(g) ΔH=﹣a kJ•mol-1。在一定温度下,将1molCO(g)和2molH2(g)充入到体积为10L的密闭容器中,发生反应。经过5min达到平衡,此时容器内压强为反应前的0.8倍。则v(CH3OH)为
CH3OH(g) ΔH=﹣a kJ•mol-1。在一定温度下,将1molCO(g)和2molH2(g)充入到体积为10L的密闭容器中,发生反应。经过5min达到平衡,此时容器内压强为反应前的0.8倍。则v(CH3OH)为(4)已知N2O4(g)
 2NO2(g) ΔH>0,现将1molN2O4充入一恒压密闭容器中,下列示意图能说明反应达到平衡状态的是
2NO2(g) ΔH>0,现将1molN2O4充入一恒压密闭容器中,下列示意图能说明反应达到平衡状态的是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】习总书记提出“绿水青山就是金山银山”,对氮、碳元素形成的有毒气体进行处理成为科学研究热点。请回答下列问题:
I.氮元素的化合物种类繁多,研究氮氧化物的反应机理对于消除污染有重要指导作用。
(1)可用O3氧化法处理氮氧化物,已知:
①2NO(g)+O2(g)=2NO2(g) ΔH1=-113kJ/mol
②4NO2(g)+O2(g)=2N2O5(g) ΔH2=-57kJ/mol
③6NO2(g)+O3(g)=3N2O5(g) ΔH2=-227kJ/mol
用O3氧化脱除NO的总反应是:NO(g)+O3(g)=NO2(g)+O2(g) ΔH4=___________ 。
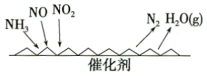
(2)用NH3催化还原氮氧化物(SCR)技术是常见的烟气氮氧化物脱除技术,反应原理如图。当NO2与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应。写出该反应的化学方程式___________ 。
II.CO2的回收与利用
(1)由CO2转化为羧酸是CO2资源化利用的重要方法。在催化作用下CO2和CH4合成CH3COOH的化学方程式为___________ ;在合成CH3COOH的反应中,下列有关说法正确的是___________ (填字母序号)。
A.利用催化剂可以提高反应物的转化率
B.有22.4LCH4(标况)参与反应时转移4mol电子
C.CH4→CH3COOH过程中,所有的化学键都发生断裂
D.该反应为放热反应
(2)CO2和H2合成甲醇也是CO2资源化利用的重要方法。测得平衡时甲醇产率与反应温度、压强的关系如图所示。
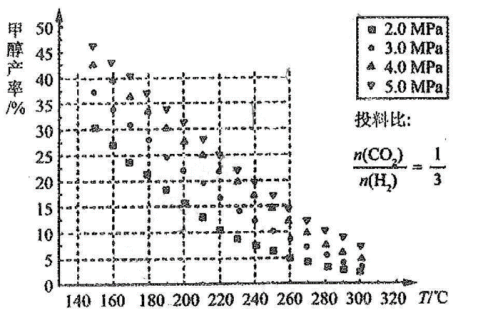
①已知该反应的热化学方程式为:CO2(g)+3H2(g)=CH3OH(g)+H2O(l) ΔH=-130.9kJ/mol,此反应的活化能E(a)正___________ E(a)逆(填“>”或“<”)。
②下列措施不能使CO2的平衡转化率提高的是___________ (填字母序号)。
A.改用更高效的催化剂
B.增大H2与CO2的投料比
C.升高温度D.增大压强
③200℃时,将2molCO2和4molH2充入2L密闭容器中,在催化作用下反应达到平衡。若平衡时CO2的转化率为50%,则此温度下该反应的平衡常数K=___________ (已知CH3OH的沸点为64.7℃)。
I.氮元素的化合物种类繁多,研究氮氧化物的反应机理对于消除污染有重要指导作用。
(1)可用O3氧化法处理氮氧化物,已知:
①2NO(g)+O2(g)=2NO2(g) ΔH1=-113kJ/mol
②4NO2(g)+O2(g)=2N2O5(g) ΔH2=-57kJ/mol
③6NO2(g)+O3(g)=3N2O5(g) ΔH2=-227kJ/mol
用O3氧化脱除NO的总反应是:NO(g)+O3(g)=NO2(g)+O2(g) ΔH4=
(2)用NH3催化还原氮氧化物(SCR)技术是常见的烟气氮氧化物脱除技术,反应原理如图。当NO2与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应。写出该反应的化学方程式

II.CO2的回收与利用
(1)由CO2转化为羧酸是CO2资源化利用的重要方法。在催化作用下CO2和CH4合成CH3COOH的化学方程式为
A.利用催化剂可以提高反应物的转化率
B.有22.4LCH4(标况)参与反应时转移4mol电子
C.CH4→CH3COOH过程中,所有的化学键都发生断裂
D.该反应为放热反应
(2)CO2和H2合成甲醇也是CO2资源化利用的重要方法。测得平衡时甲醇产率与反应温度、压强的关系如图所示。

①已知该反应的热化学方程式为:CO2(g)+3H2(g)=CH3OH(g)+H2O(l) ΔH=-130.9kJ/mol,此反应的活化能E(a)正
②下列措施不能使CO2的平衡转化率提高的是
A.改用更高效的催化剂
B.增大H2与CO2的投料比
C.升高温度D.增大压强
③200℃时,将2molCO2和4molH2充入2L密闭容器中,在催化作用下反应达到平衡。若平衡时CO2的转化率为50%,则此温度下该反应的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】 是制造微电子器件、光电子器件的新型半导体材料。综合利用炼锌矿渣{主要含铁酸镓
是制造微电子器件、光电子器件的新型半导体材料。综合利用炼锌矿渣{主要含铁酸镓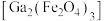 、铁酸锌
、铁酸锌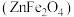 ,还含少量
,还含少量 及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。 在酸性条件下不稳定,易转化为
在酸性条件下不稳定,易转化为 。
。
②常温下,“浸出液”中的金属离子对应的氢氧化物的溶度积常数如下表,离子浓度小于 时可视为沉淀完全。
时可视为沉淀完全。
③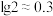 ,
,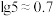 。
。
回答下列问题:
(1)写出两条加快“浸出”速率的措施:_____ 。
(2) 中铁元素的化合价为
中铁元素的化合价为_____ , 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为_____
(3)“调 ”时需调节溶液
”时需调节溶液 的最小值为
的最小值为_____ 。
(4)“滤液1”中主要含有的金属阳离子为_____ ,检验“滤液1”中是否含有 的试剂为
的试剂为_____ (填名称)。
(5)“转化2”加入铁粉时主要发生反应的离子方程式为_____ 。
(6)“电解”反萃取液(溶质为 )制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为
)制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为_____ (填化学式)。
(7)采用MOCVD(金属有机化合物化学气相沉积)技术制备GaN时,反应会产生一种标准状况下密度约为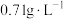 的可燃性气体,写出该反应的化学方程式:
的可燃性气体,写出该反应的化学方程式:_____ (不写条件)。
 是制造微电子器件、光电子器件的新型半导体材料。综合利用炼锌矿渣{主要含铁酸镓
是制造微电子器件、光电子器件的新型半导体材料。综合利用炼锌矿渣{主要含铁酸镓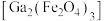 、铁酸锌
、铁酸锌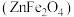 ,还含少量
,还含少量 及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
 在酸性条件下不稳定,易转化为
在酸性条件下不稳定,易转化为 。
。②常温下,“浸出液”中的金属离子对应的氢氧化物的溶度积常数如下表,离子浓度小于
 时可视为沉淀完全。
时可视为沉淀完全。| 氢氧化物 |  |  |  |  |
 |  |  | 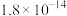 | 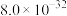 |
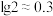 ,
,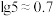 。
。回答下列问题:
(1)写出两条加快“浸出”速率的措施:
(2)
 中铁元素的化合价为
中铁元素的化合价为 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为(3)“调
 ”时需调节溶液
”时需调节溶液 的最小值为
的最小值为(4)“滤液1”中主要含有的金属阳离子为
 的试剂为
的试剂为(5)“转化2”加入铁粉时主要发生反应的离子方程式为
(6)“电解”反萃取液(溶质为
 )制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为
)制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为(7)采用MOCVD(金属有机化合物化学气相沉积)技术制备GaN时,反应会产生一种标准状况下密度约为
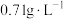 的可燃性气体,写出该反应的化学方程式:
的可燃性气体,写出该反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点。甲胺铅碘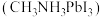 用作全固态钙钛矿敏化太阳能电池的敏化剂,可由
用作全固态钙钛矿敏化太阳能电池的敏化剂,可由 、
、 及HI为原料合成,回答下列问题:
及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为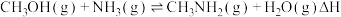 。已知该反应中相关化学键的键能数据如下:
。已知该反应中相关化学键的键能数据如下:
则该反应的
_______  。
。
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为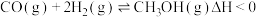 。在一定条件下,将
。在一定条件下,将 和
和 通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,
通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时, 的体积分数
的体积分数 变化趋势如图所示:
变化趋势如图所示:

①平衡时,M点 的体积分数为
的体积分数为 ,则CO的转化率为
,则CO的转化率为_______ 。
②X轴上a点的数值比b点_______ (填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是_______ 。
(3)工业上可采用 的方法来制取高纯度的CO和
的方法来制取高纯度的CO和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 标注。甲醇
标注。甲醇 脱氢反应的第一步历程,有两种可能方式:
脱氢反应的第一步历程,有两种可能方式:
方式A: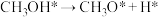
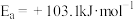
方式B: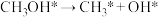
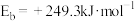
由活化能E值推测,甲醇裂解过程主要历经的方式应为_______ (填A、B)。如图为计算机模拟的各步反应的能量变化示意图:
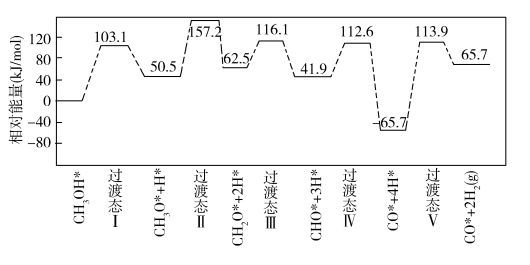
该历程中,放热最多的步骤的化学方程式为_______ 。
(4)用NaHS作污水处理的沉淀剂,可以处理工业废水中的 。已知:
。已知: 时,
时, 的电离平衡常数
的电离平衡常数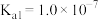 ,
,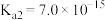 ,CuS的溶度积为
,CuS的溶度积为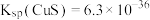 。反应
。反应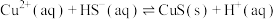 的平衡常数
的平衡常数
_______ (结果保留1位小数)。
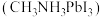 用作全固态钙钛矿敏化太阳能电池的敏化剂,可由
用作全固态钙钛矿敏化太阳能电池的敏化剂,可由 、
、 及HI为原料合成,回答下列问题:
及HI为原料合成,回答下列问题:(1)制取甲胺的反应为
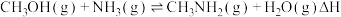 。已知该反应中相关化学键的键能数据如下:
。已知该反应中相关化学键的键能数据如下:| 共价键 | 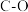 |  |  | 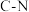 |  |
键能 | 351 | 463 | 393 | 293 | 414 |
则该反应的

 。
。(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为
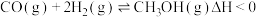 。在一定条件下,将
。在一定条件下,将 和
和 通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,
通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时, 的体积分数
的体积分数 变化趋势如图所示:
变化趋势如图所示:
①平衡时,M点
 的体积分数为
的体积分数为 ,则CO的转化率为
,则CO的转化率为②X轴上a点的数值比b点
(3)工业上可采用
 的方法来制取高纯度的CO和
的方法来制取高纯度的CO和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 标注。甲醇
标注。甲醇 脱氢反应的第一步历程,有两种可能方式:
脱氢反应的第一步历程,有两种可能方式:方式A:
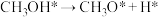
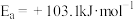
方式B:
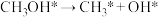
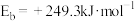
由活化能E值推测,甲醇裂解过程主要历经的方式应为

该历程中,放热最多的步骤的化学方程式为
(4)用NaHS作污水处理的沉淀剂,可以处理工业废水中的
 。已知:
。已知: 时,
时, 的电离平衡常数
的电离平衡常数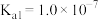 ,
,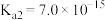 ,CuS的溶度积为
,CuS的溶度积为 。反应
。反应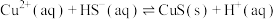 的平衡常数
的平衡常数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】从海水中提取金属镁的工艺流程可简单图示如下:

(1)步骤①的目的是将海水中的Mg2+沉淀为Mg(OH)2,若浓缩海水中c(Mg2+)=2.0 mol·L-1,Mg2+开始形成沉淀时溶液的pH约为________ (已知Ksp[Mg(OH)2]=1.8×10-11,log3=0.48)
(2)步骤③的操作由蒸发浓缩,______ ,过滤,_______ 四个环节组成。
(3)步骤④是在HCl气流中加热晶体得到无水MgCl2,简要说明HCl气体的作用_________ 。

(1)步骤①的目的是将海水中的Mg2+沉淀为Mg(OH)2,若浓缩海水中c(Mg2+)=2.0 mol·L-1,Mg2+开始形成沉淀时溶液的pH约为
(2)步骤③的操作由蒸发浓缩,
(3)步骤④是在HCl气流中加热晶体得到无水MgCl2,简要说明HCl气体的作用
您最近一年使用:0次



