工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)ΔH 在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g)ΔH 在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
下列说法正确的是( )
 N2(g)+CO2(g)+2H2O(g)ΔH 在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g)ΔH 在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:| 温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | …… | 0.15 |
| A.0~10 min内,T1时V(CH4)的平均反应速率比T2时的平均反应速率小 |
| B.T2时,CH4的平衡转化率为35% |
| C.T1时,40min后,断裂4molC-H键同时生成4molO-H |
| D.该反应的ΔH >0,T1<T2 |
更新时间:2017-09-01 07:01:32
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】一定温度下, 的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是
的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是
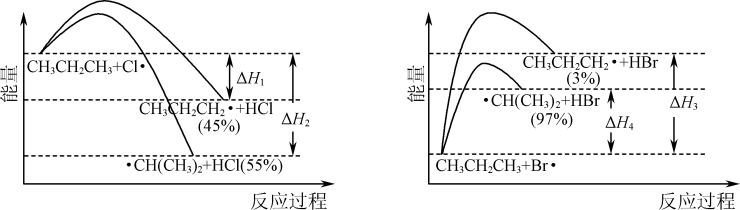
 的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是
的氯化、溴化反应势能图及一段时间后产物的选择性如图,下列叙述不正确的是 
A. |
| B.升高温度,体系中n(1-氯丙烷)∶n(2-氯丙烷)的值增大 |
| C.以丙烷为原料合成丙醇时,“先溴代再水解”有利于提高2-丙醇的含量 |
| D.由图可知,丙烷中碳氢键的键能不完全相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】西湖大学科研团队正在研究“聚酮合成酶(由链霉菌产生)”在有空气存在下“组装”物质的机理。物质A的“组装”过程如图所示,下列有关说法错误的是
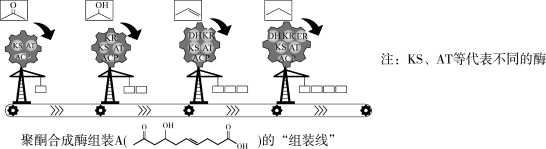

| A.温度会影响“组装线”的“组装”效率 |
| B.“组装”过程中可能有CO2和H2O生成 |
| C.将四种“聚酮合成酶”交换顺序,也可以组装出该物质 |
| D.上述流程如能大规模应用,可实现化工生产的“绿色化” |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】短周期元素X、Y、Z、W 在元素周期表中的位置如下图所示,其中X 形成化合物种类最多,下列说法正确的是:
| X | Y | |
| Z | W |
| A.X 位于第二周期 IV 族 |
| B.Y 的气态氢化物的水溶液中只存在两个平衡状态 |
| C.W 的最高价氧化物是太阳能电池和电脑芯片中不可缺少的材料 |
| D.常温下,将 Z 单质投入到 Y 的最高价氧化物对应的水化物的浓溶液中,无明显现象 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】如果一个反应的ΔH-TΔS=0,则此反应
| A.能自发进行 | B.处于平衡状态 | C.不进行 | D.是放热反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】在容积一定的密闭器中发生可逆反应:A(g)+2B(g)  2C(g)
2C(g)  H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是
H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是

 2C(g)
2C(g)  H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是
H=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示。下列说法不正确的是
A.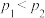 ,纵坐标指A的质量分数 ,纵坐标指A的质量分数 |
B. ,纵坐标指C的质量分数 ,纵坐标指C的质量分数 |
C. ,纵坐标指混合气体的平均摩尔质量 ,纵坐标指混合气体的平均摩尔质量 |
D. ,纵坐标指A的转化率 ,纵坐标指A的转化率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将一定量的CO2与H2通入某密闭容器中合成甲醇,在催化剂作用下发生下述反应:
Ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g)∆H1<0
CH3OH(g)+H2O(g)∆H1<0
Ⅱ.CO2(g)+H2(g) H2O(g)+CO(g)∆H2
H2O(g)+CO(g)∆H2
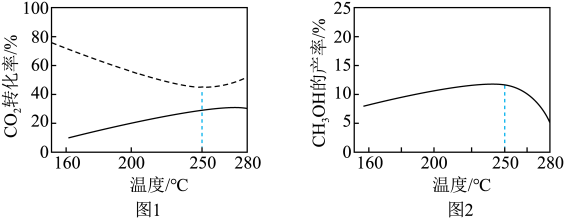
催化反应相同时间,测得不同温度下CO2的转化率如图-1所示(图中虚线表示相同条件下CO2的平衡转化率随温度的变化),CH3OH的产率如图-2所示。
下列有关说法正确的是
Ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)∆H1<0
CH3OH(g)+H2O(g)∆H1<0Ⅱ.CO2(g)+H2(g)
 H2O(g)+CO(g)∆H2
H2O(g)+CO(g)∆H2催化反应相同时间,测得不同温度下CO2的转化率如图-1所示(图中虚线表示相同条件下CO2的平衡转化率随温度的变化),CH3OH的产率如图-2所示。

下列有关说法正确的是
| A.∆H2<0 |
| B.250℃时,容器内反应达平衡 |
| C.250℃前,随温度升高CO2的平衡转化率减小,可能因为该温度范围内仅发生反应Ⅰ |
| D.250℃后,随温度升高CH3OH的产率减小,可能是因为催化剂对反应Ⅰ的活性降低 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】乙二醇在生产、生活中有着广泛的用途,某工艺制取乙二醇所涉及的反应如下:
反应Ⅰ

反应Ⅱ

在压强一定的条件下,将 、
、 按1:3进料比通入装有催化剂的反应器中,测得
按1:3进料比通入装有催化剂的反应器中,测得 的转化率与
的转化率与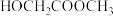 、
、 的选择性[
的选择性[ ]。
]。
反应Ⅰ


反应Ⅱ


在压强一定的条件下,将
 、
、 按1:3进料比通入装有催化剂的反应器中,测得
按1:3进料比通入装有催化剂的反应器中,测得 的转化率与
的转化率与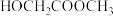 、
、 的选择性[
的选择性[ ]。
]。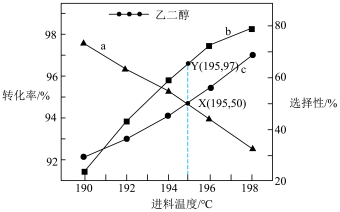
A.曲线a表示 转化率 转化率 |
| B.195℃时,反应Ⅰ的平衡常数约为2904 |
C.190~198℃范围内,温度升高,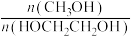 的值减小 的值减小 |
D.其它条件相同时,增大压强和升高温度均可以提高平衡时 的产量 的产量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】向某恒容密闭容器中充入一定量的Xe和 ,发生反应
,发生反应 。
。

不同温度下平衡常数如表,平衡时的分布分数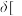 如
如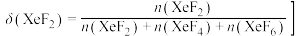 随温度的变化如图。下列说法不正确的是
随温度的变化如图。下列说法不正确的是
 ,发生反应
,发生反应 。
。
温度 |
|
|
250 |
|
|
400 |
|
|
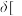 如
如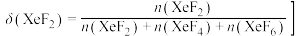 随温度的变化如图。下列说法不正确的是
随温度的变化如图。下列说法不正确的是
| A.反应ⅲ低温自发 |
B.当 与 与 的投料比为1:1时,平衡转化率: 的投料比为1:1时,平衡转化率: 大于Xe 大于Xe |
C.升高温度,平衡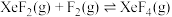 正向移动 正向移动 |
D.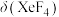 在 在 后减小的原因是反应ⅱ逆向移动的程度较大 后减小的原因是反应ⅱ逆向移动的程度较大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】80℃时,NO2(g)+SO2(g) SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(NO2)/mol ·L-1 | 0.10 | 0.20 | 0.20 |
| c(SO2)/mol ·L-1 | 0.10 | 0.10 | 0.20 |
| A.平衡时,乙中SO2的转化率大于50% |
| B.当反应平衡时,丙中c(SO2)是甲中的2倍 |
| C.温度升至90℃,上述反应平衡常数为25/16,则正反应为吸热反应 |
| D.其他条件不变,若起始时向容器乙中充入0.10mol ·L-1 NO2和0.20 mol ·L-1 SO2,达到平衡时c(NO)与原平衡不同 |
您最近一年使用:0次

 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是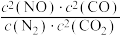



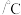


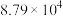
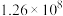
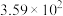

 hH(g)达到平衡后,A、B、H的物质的量分别为amol、bmol和hmol。已知a+b=2h,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是
hH(g)达到平衡后,A、B、H的物质的量分别为amol、bmol和hmol。已知a+b=2h,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是

