目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究。已知在不同温度下的化学反应平衡常数(K1、K2、K3)如下表所示:
请回答下列问题:
(1)反应②是________ (填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=________ (用K1、K2表示);根据反应③判断ΔS___ 0(填“>”、“=”或“<”),在______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol/L、0.8mol/L、0.3mol/L、0.15mol/L,则此时v正________ v逆(填“>”、“=”或“<”)。
| 化学反应 | 焓变 | 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | ΔH1 | K1 | 2.5 | 0.34 | 0.15 |
②CO2(g)+H2(g) CO(g)+H2O(g) CO(g)+H2O(g) | ΔH2 | K2 | 1.0 | 1.70 | 2.52 |
③CO2(g)+3H2(g) CH3OH(g)+H2O(g) CH3OH(g)+H2O(g) | ΔH3 | K3 | |||
请回答下列问题:
(1)反应②是
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(3)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol/L、0.8mol/L、0.3mol/L、0.15mol/L,则此时v正
17-18高二上·甘肃天水·阶段练习 查看更多[4]
河北省秦皇岛市第一中学2020-2021学年高二上学期12月月考化学试题湖北省武汉市汉南区职教中心2019-2020学年高二上学期期中考试化学试题(已下线)黄金30题系列++高二化学(选修4)+++大题好拿分【基础版】甘肃省天水市第一中学2017-2018学年高二上学期第一阶段考试(理)化学试题
更新时间:2017-10-12 05:38:47
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知下列热化学方程式:
①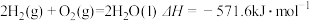
②
(1)氢气的摩尔燃烧焓是______________ 。
(2)已知: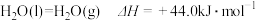 。写出丙烷
。写出丙烷 燃烧生成二氧化碳和液态水的热化学方程式:
燃烧生成二氧化碳和液态水的热化学方程式:___________________________ 。
(3)实验测得 和
和 的混合气体共
的混合气体共 ,完全燃烧生成液态水时放热
,完全燃烧生成液态水时放热 ,则混合气体中
,则混合气体中 和
和 的体积比是
的体积比是__________ 。
(4)当反应②中转移10mol电子时,燃烧的丙烷 的质量是
的质量是_________ g,生成的CO2在标准状况下的体积是_________ L。
①
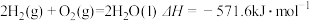
②

(1)氢气的摩尔燃烧焓是
(2)已知:
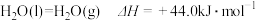 。写出丙烷
。写出丙烷 燃烧生成二氧化碳和液态水的热化学方程式:
燃烧生成二氧化碳和液态水的热化学方程式:(3)实验测得
 和
和 的混合气体共
的混合气体共 ,完全燃烧生成液态水时放热
,完全燃烧生成液态水时放热 ,则混合气体中
,则混合气体中 和
和 的体积比是
的体积比是(4)当反应②中转移10mol电子时,燃烧的丙烷
 的质量是
的质量是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】NH4VO3在高温下分解产生的V2O5可作为硫酸工业中2SO2(g)+O2(g) 2SO3(g),ΔH=p的催化剂,其催化原理如图所示。
2SO3(g),ΔH=p的催化剂,其催化原理如图所示。

过程a和过程b的热化学方程式为V2O5(s)+SO2(g) V2O4(s)+SO3(g),ΔH=q;V2O4(s)+O2(g)+2SO2(g)
V2O4(s)+SO3(g),ΔH=q;V2O4(s)+O2(g)+2SO2(g) 2VOSO4(s),ΔH=r。请写出过程c的热化学方程式:
2VOSO4(s),ΔH=r。请写出过程c的热化学方程式:___________ 。
 2SO3(g),ΔH=p的催化剂,其催化原理如图所示。
2SO3(g),ΔH=p的催化剂,其催化原理如图所示。
过程a和过程b的热化学方程式为V2O5(s)+SO2(g)
 V2O4(s)+SO3(g),ΔH=q;V2O4(s)+O2(g)+2SO2(g)
V2O4(s)+SO3(g),ΔH=q;V2O4(s)+O2(g)+2SO2(g) 2VOSO4(s),ΔH=r。请写出过程c的热化学方程式:
2VOSO4(s),ΔH=r。请写出过程c的热化学方程式:
您最近一年使用:0次
【推荐3】氮氧化物(NOx)是一种主要的大气污染物,必须进行处理。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
①ΔH 1___________ 0,ΔH 3___________ 0.(填“>”或“<”)
②N2(g)+O2(g) = 2NO(g) ΔH=___________ kJ·mol-1
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) =5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是___________ (填字母)。
A.
B.
C 。
。
(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
H2O(l) = H2O(g) ΔH=+44 kJ·mol-1
则CH4 (g)+2NO2(g)=N2 (g)+CO2(g)+2H2O(g) ΔH=___________ ,1.6 g CH4还原NO2 生成N2和液态水时放出的热量为___________ kJ。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
| 反应 | N2(g)→2N(g) | O2(g)→2O(g) | N(g)+O(g)→NO(g) |
| 反应热 | ΔH 1 | ΔH 2 | ΔH 3 |
| 热量值kJ·mol-1 | 945 | 498 | 630 |
①ΔH 1
②N2(g)+O2(g) = 2NO(g) ΔH=
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) =5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是
A.

B.

C
 。
。(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
H2O(l) = H2O(g) ΔH=+44 kJ·mol-1
则CH4 (g)+2NO2(g)=N2 (g)+CO2(g)+2H2O(g) ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】反应2X(g) Y(g)+Z(g)在不同条件下进行3组实验,Y、Z的起始浓度为0,反应物X的浓度随反应时间的变化曲线如图所示。回答下列问题。
Y(g)+Z(g)在不同条件下进行3组实验,Y、Z的起始浓度为0,反应物X的浓度随反应时间的变化曲线如图所示。回答下列问题。

(1)实验①中0∼10min内,用Z表示的平均化学反应速率为___________ 。
(2)该反应的ΔH___________ 0(填“ ”或“
”或“ ”)。
”)。
(3)若实验①、②相比较,实验②只改变了一个条件,则实验②改变的条件为___________ 。
(4)下列条件既能加快反应速率又能使平衡正向移动的是___________ (填序号)。
a.缩小容器体积 b.再充入1mol Y c.升高温度 d.使用催化剂
(5)820℃时,该反应的平衡常数K=___________ 。
 Y(g)+Z(g)在不同条件下进行3组实验,Y、Z的起始浓度为0,反应物X的浓度随反应时间的变化曲线如图所示。回答下列问题。
Y(g)+Z(g)在不同条件下进行3组实验,Y、Z的起始浓度为0,反应物X的浓度随反应时间的变化曲线如图所示。回答下列问题。
(1)实验①中0∼10min内,用Z表示的平均化学反应速率为
(2)该反应的ΔH
 ”或“
”或“ ”)。
”)。(3)若实验①、②相比较,实验②只改变了一个条件,则实验②改变的条件为
(4)下列条件既能加快反应速率又能使平衡正向移动的是
a.缩小容器体积 b.再充入1mol Y c.升高温度 d.使用催化剂
(5)820℃时,该反应的平衡常数K=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】治理汽车尾气中NO和CO污染的一种方法是将其转化为无害的CO2和N2,反应原理为2NO(g)+2CO(g) 2CO2(g)+N2(g) △H<0。某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.4molNO和0.4molCO,在三种不同实验条件下进行上述反应体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
2CO2(g)+N2(g) △H<0。某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.4molNO和0.4molCO,在三种不同实验条件下进行上述反应体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
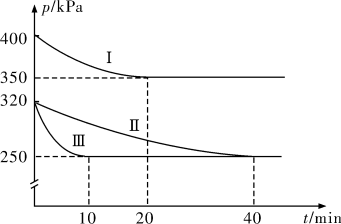
(1)与实验Ⅱ相比,实验Ⅰ和实验Ⅲ分别仅改变一种反应条件,所改变的条件为实验Ⅰ:__ ,实验Ⅲ:__
(2)三组实验中CO的平衡转化率αⅠ(CO)、αⅡ(CO)和αⅢ(CO)的大小关系为__ 。
(3)实验Ⅲ的平衡常数K=__ 。
 2CO2(g)+N2(g) △H<0。某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.4molNO和0.4molCO,在三种不同实验条件下进行上述反应体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
2CO2(g)+N2(g) △H<0。某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.4molNO和0.4molCO,在三种不同实验条件下进行上述反应体系各自保持温度不变),反应体系总压强随时间的变化如图所示。
(1)与实验Ⅱ相比,实验Ⅰ和实验Ⅲ分别仅改变一种反应条件,所改变的条件为实验Ⅰ:
(2)三组实验中CO的平衡转化率αⅠ(CO)、αⅡ(CO)和αⅢ(CO)的大小关系为
(3)实验Ⅲ的平衡常数K=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】在化学反应

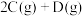
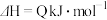 过程中的能量变化如图所示,回答下列问题。
过程中的能量变化如图所示,回答下列问题。

(1)Q________ 0(填“>”“<”或“=”)。
(2)熵变
________ 0(填“>”“<”或“=”)。
(3)该反应________ 自发进行(填“能”或“不能”)。
(4)升高温度平衡常数K________ (填“增大”“减小”或“不变”),平衡向________ (填“正反应”或“逆反应”)方向移动。


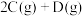
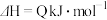 过程中的能量变化如图所示,回答下列问题。
过程中的能量变化如图所示,回答下列问题。
(1)Q
(2)熵变

(3)该反应
(4)升高温度平衡常数K
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列问题
(1)已知反应CO(g)+2H2(g) CH3OH(g),在恒容密闭容器中按
CH3OH(g),在恒容密闭容器中按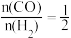 加入CO和H2合成甲醇,测得起始压强p0=102 kPa。CO的平衡转化率[α(CO)]随温度的变化曲线如图所示,R点时反应的平衡常数Kp=
加入CO和H2合成甲醇,测得起始压强p0=102 kPa。CO的平衡转化率[α(CO)]随温度的变化曲线如图所示,R点时反应的平衡常数Kp=___________ (kPa)-2(用平衡分压代替平衡浓度计算,p分=p总×物质的量分数),R、S两点平衡常数大小:Kp(R)___________ (填“>”“=”或“<”)Kp(S)。

(2)CO可用于合成甲醇,反应的化学方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应的ΔH
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应的ΔH___________ 0(填“>”或“<”)。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是___________ 。

(1)已知反应CO(g)+2H2(g)
 CH3OH(g),在恒容密闭容器中按
CH3OH(g),在恒容密闭容器中按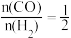 加入CO和H2合成甲醇,测得起始压强p0=102 kPa。CO的平衡转化率[α(CO)]随温度的变化曲线如图所示,R点时反应的平衡常数Kp=
加入CO和H2合成甲醇,测得起始压强p0=102 kPa。CO的平衡转化率[α(CO)]随温度的变化曲线如图所示,R点时反应的平衡常数Kp=
(2)CO可用于合成甲醇,反应的化学方程式为CO(g)+2H2(g)
 CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应的ΔH
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应的ΔH
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】完成下列问题。
(1)向2L的密闭容器中通入2molX气体和3molY气体,一定条件下发生以下反应: ⇌
⇌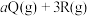 ,10s末测得R的物质的量为
,10s末测得R的物质的量为 ,Q的浓度为
,Q的浓度为 。请回答:
。请回答:
①化学方程式中a=___________ 。
②10s末X的物质的量浓度为___________ 。
③反应开始至10s内,用Y表示的化学反应速率为___________
④恒温恒容条件下,向该反应容器中通入1mol氦气,反应速率___________ (填“增大”或“减小”或“不变”)。
⑤恒温恒压条件下,向该反应容器中通入1mol氨气,反应速率___________ 。
(2)在一定体积的密闭容器中,进行如下化学反应: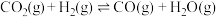 。该反应的化学平衡常数K和温度t的关系如下表:
。该反应的化学平衡常数K和温度t的关系如下表:
回答下列问题:
①该反应的化学平衡常数表达式为:K=___________ 。
②该反应为___________ 反应(填“吸热”或“放热”)。
③能判断该反应是否达到化学平衡状态的依据是___________ (填序号)。
a.容器中压强不变 b.混合气体中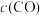 不变
不变
c.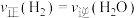 d.
d.
(4)某温度下,平衡浓度符合下式: ,则此时的温度为
,则此时的温度为______ ℃。
(1)向2L的密闭容器中通入2molX气体和3molY气体,一定条件下发生以下反应:
 ⇌
⇌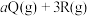 ,10s末测得R的物质的量为
,10s末测得R的物质的量为 ,Q的浓度为
,Q的浓度为 。请回答:
。请回答:①化学方程式中a=
②10s末X的物质的量浓度为
③反应开始至10s内,用Y表示的化学反应速率为
④恒温恒容条件下,向该反应容器中通入1mol氦气,反应速率
⑤恒温恒压条件下,向该反应容器中通入1mol氨气,反应速率
(2)在一定体积的密闭容器中,进行如下化学反应:
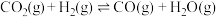 。该反应的化学平衡常数K和温度t的关系如下表:
。该反应的化学平衡常数K和温度t的关系如下表:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应的化学平衡常数表达式为:K=
②该反应为
③能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中
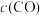 不变
不变c.
 d.
d.
(4)某温度下,平衡浓度符合下式:
 ,则此时的温度为
,则此时的温度为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
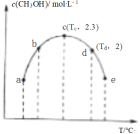
【推荐1】向1L恒容密闭容器中充入3molCO2、7molH2的混合气体,控制适当条件发生反应: 。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
回答下列问题:
(1)第10min时,正反应速率υ(c)_______ (填“>”“<”或“=”,下同)υ(d),c点处对应反应体系中c(H2)=_______  。
。
(2)该反应的
_______ (填“>”或“<”)0,a、b、c、d、e五点对应温度下,反应肯定处于非平衡状态的是_______ (填字母)。
(3)实际生产中,通常会采用下列方法以提高单位时间内CH3OH的产率_______(填字母)。
(4)若d点时容器总压为12kPa,则Kp=_______ (用平衡分压代替平衡浓度,分压=总压 物质的量分数)。
物质的量分数)。
 。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
回答下列问题:
(1)第10min时,正反应速率υ(c)
 。
。(2)该反应的

(3)实际生产中,通常会采用下列方法以提高单位时间内CH3OH的产率_______(填字母)。
| A.使用催化剂 | B.不断分离出产物 |
| C.低温下进行反应 | D.不断补充原料 |
 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1).用合成气生成甲醇的反应:CO(g)+2H2(g)  CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
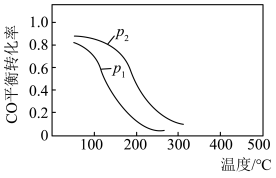
①ΔH________ (填“>”“<”或“= ”)0。
②写出一条可同时提高反应速率和CO转化率的措施:________________________ 。
③下列说法正确的是________ (填字母)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
④0~3 min内用CH3OH表示的反应速率v(CH3OH)=__________________ 。
⑤ 200 ℃时,该反应的平衡常数K=________ 。向上述200 ℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡________ (填“正向”“逆向”或“不”)移动。
 CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①ΔH
②写出一条可同时提高反应速率和CO转化率的措施:
③下列说法正确的是
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
④0~3 min内用CH3OH表示的反应速率v(CH3OH)=
⑤ 200 ℃时,该反应的平衡常数K=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】二甲醚(CH3OCH3)是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)⇌CH3OCH3(g)+H2O(g)△H=﹣23.5J•mol﹣1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.

①上述由甲醇制二甲醚的反应属于_____ 反应.在T1℃时,反应的平衡常数为___ ;
②相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4mol•L﹣1,c(H2O)=0.6mol•L﹣1、c(CH3OCH3)=1.2mol•L﹣1,此时正、逆反应速率的大小:v(正)_____ v(逆)(填“>”、“<”或“=”).

①上述由甲醇制二甲醚的反应属于
②相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4mol•L﹣1,c(H2O)=0.6mol•L﹣1、c(CH3OCH3)=1.2mol•L﹣1,此时正、逆反应速率的大小:v(正)
您最近一年使用:0次

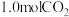 和
和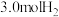 ,在一定温度范围内发生如下转化:
,在一定温度范围内发生如下转化: (x>0)。在不同催化剂作用下,相同时间内
(x>0)。在不同催化剂作用下,相同时间内 的转化率随温度的变化如图所示:
的转化率随温度的变化如图所示:

 。
。

