某温度时,在一个容积为3L的密闭容器中,A、B、C三种气态物质的物质的量随时间变化曲线如图所示。请回答以下问题:
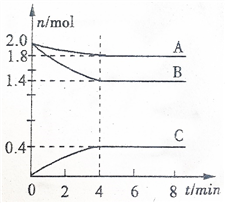
(1)该反应的化学方程式是_________________________________ 。
(2)反应从开始到平衡时,气体B的平均反应速率是___________________ 。
(3)该反应的化学平衡常数表达式是______________________________ 。
(4)其他条件不变,升高温度,逆反应速率将____________ (填“加快”、“减慢”或“不变”)。
(5)反应达平衡后,其他条件不变,增加容器体积,平衡将__________ (填“正向移动”、“逆向移动”或“不移动”)。

(1)该反应的化学方程式是
(2)反应从开始到平衡时,气体B的平均反应速率是
(3)该反应的化学平衡常数表达式是
(4)其他条件不变,升高温度,逆反应速率将
(5)反应达平衡后,其他条件不变,增加容器体积,平衡将
更新时间:2017-11-03 16:17:40
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】氮及其化合物在工农业生产、生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ·molˉl
C(s)+O2(g)=CO2(g) △H=―393.5 kJ·molˉl
2C(s)+O 2(g)=2CO(g) △H=―221kJ·molˉl 若某反应的平衡常数表达式为: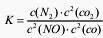 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式 ______________________________ 。
(2)N2O5在一定条件下可发生分解:2N2O5(g) 4NO2(g)+O2(g)。某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
4NO2(g)+O2(g)。某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
① 反应开始时体系压强为P0,第3.00 min时体系压强为p1,则p1:p0=_____________ ;2.00min~5.00 min内,O2的平均反应速率为 _______________ 。
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是______________ 。
a.容器中压强不再变化 b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5) d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O4与NO2 之间存在反应:N2O4(g) 2NO2(g) △H=QkJ·molˉ1。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图所示。
2NO2(g) △H=QkJ·molˉ1。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图所示。

如图中a点对应温度下,已知N2O4的起始压强p0为200 kPa,该温度下反应的平衡常数Kp=________ (小数点后保留一位数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)将固体氢氧化钠投入0.1mol/L的HN3(氢叠氮酸)溶液当中,溶液的体积1L(溶液体积变化忽略不计)溶液的pH变化如图所示,HN3的电离平衡常数K=1×10-5,B点时溶液的pH=7,计算B点时加入氢氧化钠的物质的量________ mol(保留两位有效数字)。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ·molˉl
C(s)+O2(g)=CO2(g) △H=―393.5 kJ·molˉl
2C(s)+O 2(g)=2CO(g) △H=―221kJ·molˉl 若某反应的平衡常数表达式为:
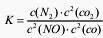 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式 (2)N2O5在一定条件下可发生分解:2N2O5(g)
 4NO2(g)+O2(g)。某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
4NO2(g)+O2(g)。某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
① 反应开始时体系压强为P0,第3.00 min时体系压强为p1,则p1:p0=
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是
a.容器中压强不再变化 b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5) d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O4与NO2 之间存在反应:N2O4(g)
 2NO2(g) △H=QkJ·molˉ1。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图所示。
2NO2(g) △H=QkJ·molˉ1。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图所示。
如图中a点对应温度下,已知N2O4的起始压强p0为200 kPa,该温度下反应的平衡常数Kp=
(4)将固体氢氧化钠投入0.1mol/L的HN3(氢叠氮酸)溶液当中,溶液的体积1L(溶液体积变化忽略不计)溶液的pH变化如图所示,HN3的电离平衡常数K=1×10-5,B点时溶液的pH=7,计算B点时加入氢氧化钠的物质的量
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】从能量的变化和反应的快慢等角度研究化学反应具有重要意义。
(1)已知一定条件下,反应N2+3H2 2NH3为放热反应;:
2NH3为放热反应;:
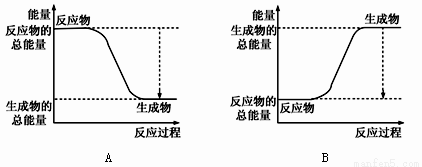
①下图能正确表示该反应中能量变化的是________ ;
②根据下表数据,计算生成1molNH3时该反应放出的热量为______ kJ;
③一定温度下,将3molH2和1molN2通入容积为2 L的密闭容器中发生反应。若5min达到平衡,测得c(NH3)=0.4mol/L,则0至5min内N2的平均化学反应速率v(N2)=______ ,反应开始与平衡时气体的物质的量之比为__________ ;若达到平衡时,该容器内混合气体总压强为p,混合气体起始压强为p0 ,请用p0、p来表示达到平衡时H2的转化率为__________ 。
④ 在③反应条件下,能够判断该反应已经达到化学平衡状态的是______________ 。
A.容器内混合气体密度不变
B.混合气体的压强不变
C.单位时间内生成n mol N2 的同时生成2n mol NH3
D. v (N2)=2v(NH3)
(2)原电池可将化学能转化为电能。由A、B、C、D四种金属按下表中装置进行实验:
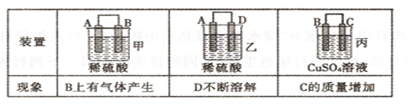
①装置甲中SO 向
向________ 极移动(填“A”或“B”);
②四种金属活动性由强到弱的顺序是_____________ ;
③若装置丙中的电极为质量相等的铁棒和铜棒,电池工作一段时间后,取出洗净、干燥、称量,两电极质量差为6g,则导线中通过电子的物质的量为______ mol。
(1)已知一定条件下,反应N2+3H2
 2NH3为放热反应;:
2NH3为放热反应;:①下图能正确表示该反应中能量变化的是

②根据下表数据,计算生成1molNH3时该反应放出的热量为
| 化学键 | H-H | N≡N | N-H |
| 断开1mol键所吸收的能量 | 436kJ | 946kJ | 391kJ |
③一定温度下,将3molH2和1molN2通入容积为2 L的密闭容器中发生反应。若5min达到平衡,测得c(NH3)=0.4mol/L,则0至5min内N2的平均化学反应速率v(N2)=
④ 在③反应条件下,能够判断该反应已经达到化学平衡状态的是
A.容器内混合气体密度不变
B.混合气体的压强不变
C.单位时间内生成n mol N2 的同时生成2n mol NH3
D. v (N2)=2v(NH3)
(2)原电池可将化学能转化为电能。由A、B、C、D四种金属按下表中装置进行实验:

①装置甲中SO
 向
向②四种金属活动性由强到弱的顺序是
③若装置丙中的电极为质量相等的铁棒和铜棒,电池工作一段时间后,取出洗净、干燥、称量,两电极质量差为6g,则导线中通过电子的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.在恒温条件下,将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):____________________ 。
(2)0~10min化学反应速度V(X)=__________________ 。
(3)比较Y在0~10min和10~20min时平均反应速率的大小:v(0~10)_______ v(10~20)(填“<”、“>”或“=”),原因是________________ 。
(4) a、b、c、d四个点中,表示化学反应处于平衡状态的点是_________ ,理由是__________ 。
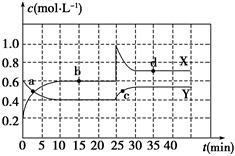
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):
(2)0~10min化学反应速度V(X)=
(3)比较Y在0~10min和10~20min时平均反应速率的大小:v(0~10)
(4) a、b、c、d四个点中,表示化学反应处于平衡状态的点是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】肌肉中的肌红蛋白(Mb)可与O2结合生成MbO2:Mb(aq)+O2(g)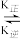 MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:
MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:
(1)计算37℃、P(O2)为2.00kPa时,上述反应的平衡常数K=_______ kPa﹣1。(气体和溶液中的溶质分别用分压和物质的量浓度表达)
(2)导出平衡时肌红蛋白与O2的结合度(α)与O2的压强[P(O2)]之间的关系式α=_______ (用含有k正、k逆的式子表示)。
(3)37℃时,若空气中氧气分压为20.0kPa,人正常呼吸时α的最大值为_______ %(计算结果保留小数点后两位)
(4)一般情况下,高烧患者体内MbO2的浓度会比其健康时_______ (填“高”或“低”,下同);在温度不变的条件下,游客在高山山顶时体内MbO2的浓度比其在山下时_______ 。
(5)37℃时,下图中坐标为(1.00,50.0)的点对应的反应状态为向_______ 进行(填“左”或“右”),此时v正:v逆=_______ (填数值)。
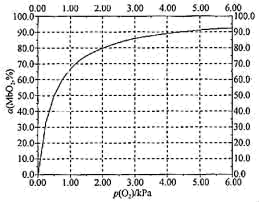
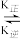 MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:
MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:| P(O2) | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
| α(MbO2%) | 50.0 | 67.0 | 80.0 | 85.0 | 88.0 | 90.3 | 91.0 |
(1)计算37℃、P(O2)为2.00kPa时,上述反应的平衡常数K=
(2)导出平衡时肌红蛋白与O2的结合度(α)与O2的压强[P(O2)]之间的关系式α=
(3)37℃时,若空气中氧气分压为20.0kPa,人正常呼吸时α的最大值为
(4)一般情况下,高烧患者体内MbO2的浓度会比其健康时
(5)37℃时,下图中坐标为(1.00,50.0)的点对应的反应状态为向

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】在一个容积为2L的密闭容器中,加入0.8mol的A2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+B2(g)⇌2AB(g) △H<0,反应中各物质的浓度随时间的变化情况如图所示。
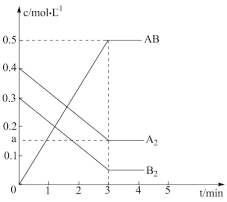
(1)在上述反应达到平衡后,第4min时,若将容器的体积快速扩大一倍(其他条件不变),请在图中画出4min~5min的AB浓度的变化线_______ 。
(2)在相同条件下,若开始时向此容器中加入的A2(g)、B2(g)和AB(g)的物质的量分别为0.4mol、0.2mol、0.8mol。则反应向_______ 反应方向进行(填“正”或“逆”)。判断依据是_______ 。反应达到平衡后,各物质的体积分数与原平衡相比_______ (填序号)
①A2、B2减小,AB增大 ②A2、B2增大,AB减小 ③均不变 ④无法确定

(1)在上述反应达到平衡后,第4min时,若将容器的体积快速扩大一倍(其他条件不变),请在图中画出4min~5min的AB浓度的变化线
(2)在相同条件下,若开始时向此容器中加入的A2(g)、B2(g)和AB(g)的物质的量分别为0.4mol、0.2mol、0.8mol。则反应向
①A2、B2减小,AB增大 ②A2、B2增大,AB减小 ③均不变 ④无法确定
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】(1)在密闭容器中有H2O(g) +C(s)  CO(g) + H2(g)反应,一定条件下达到平衡,①增大水蒸气浓度,平衡向
CO(g) + H2(g)反应,一定条件下达到平衡,①增大水蒸气浓度,平衡向______ 反应方向移动(填“正”、“逆”或“不”下同),CO的浓度将____ 。(填“增大”、“减小”或“不变”下同)
②增加H2浓度平衡向____ 反应方向移动,CO的浓度将____ 。
(2)用注射器吸入少量NO2和N2O4的混合气体,发生如下反应:
2NO2(g) N2O4(g) 当活塞迅速向外拉时,平衡向
N2O4(g) 当活塞迅速向外拉时,平衡向____ 反应方向移动,气体的颜色先变_____ (“浅”、“深”或“不变”下同),后变______ ;最终和最初相比,_____ 更深(填“前”或“后”)。
 CO(g) + H2(g)反应,一定条件下达到平衡,①增大水蒸气浓度,平衡向
CO(g) + H2(g)反应,一定条件下达到平衡,①增大水蒸气浓度,平衡向②增加H2浓度平衡向
(2)用注射器吸入少量NO2和N2O4的混合气体,发生如下反应:
2NO2(g)
 N2O4(g) 当活塞迅速向外拉时,平衡向
N2O4(g) 当活塞迅速向外拉时,平衡向
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
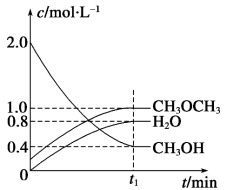
(1)该条件下反应平衡常数表达式K=__ ;在t1℃时,反应的平衡常数为__ ,达到平衡时n(CH3OCH3):n(CH3OH):n(H2O)=__ 。
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4mol·L-1、c(H2O)=0.6 mol·L-1、c(CH3OCH3)=2.4 mol·L-1,此时正、逆反应速率的大小:v正__ v逆(填“>”、“<”或“=”),反应向__ 反应方向进行(填“正”或“逆”)。
 CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
(1)该条件下反应平衡常数表达式K=
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4mol·L-1、c(H2O)=0.6 mol·L-1、c(CH3OCH3)=2.4 mol·L-1,此时正、逆反应速率的大小:v正
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】锰元素广泛分布在自然界中,其单质和化合物在工农业生产中有着重要的应用。
(1)已知相关热化学方程式为:
4Al(s)+3O2(g)=2Al2O2(s) △H1=a kJ•mol﹣1
3MnO2(s)=Mn3O4(s)+O2(g) △H2=bkJ•mol﹣1
3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) △H3=ckJ•mol﹣1
则3MnO2(s)+4Al(s)=3Mn(s)+2Al2O3(s) △H=__ kJ•mol﹣1(用含a、b、c的代数式表示).
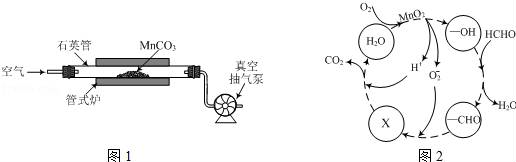
(2)MnCO3广泛用作锰盐原料.通过如图装置焙烧MnCO3可以制取MnO2,反应方程式为:2MnCO3(s)+O2(g)═2MnO2(s)+2CO2(g)。
①2MnCO3(s)+O2(g)⇌2MnO2(s)+2CO2(g)的化学平衡常数表达式K=______ 。
②用真空抽气泵不断抽气的目的除保证反应持续进行外,还有______ 。
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________ (填序号)。(如图中V正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)

(3)MnO2常用作催化剂。MnO2催化降解甲醛的反应机理如图所示,图中X表示的粒子是______ ,该反应的总反应方程式为______ 。
(4)MnSO4是重要微量元素肥料。用惰性电极电解MnSO4溶液可以制得更好活性的MnO2,电解时总反应的离子方程式为:______ ,电解过程中阴极附近的pH______ (选填“增大”、“减小”或“不变”)
(1)已知相关热化学方程式为:
4Al(s)+3O2(g)=2Al2O2(s) △H1=a kJ•mol﹣1
3MnO2(s)=Mn3O4(s)+O2(g) △H2=bkJ•mol﹣1
3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) △H3=ckJ•mol﹣1
则3MnO2(s)+4Al(s)=3Mn(s)+2Al2O3(s) △H=
(2)MnCO3广泛用作锰盐原料.通过如图装置焙烧MnCO3可以制取MnO2,反应方程式为:2MnCO3(s)+O2(g)═2MnO2(s)+2CO2(g)。

①2MnCO3(s)+O2(g)⇌2MnO2(s)+2CO2(g)的化学平衡常数表达式K=
②用真空抽气泵不断抽气的目的除保证反应持续进行外,还有
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是

(3)MnO2常用作催化剂。MnO2催化降解甲醛的反应机理如图所示,图中X表示的粒子是
(4)MnSO4是重要微量元素肥料。用惰性电极电解MnSO4溶液可以制得更好活性的MnO2,电解时总反应的离子方程式为:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】氨气在工农业生产中有着重要作用,请回答下列各有关问题。
(1)用氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) △H<0.某温度下,向容积为100L的密闭容器中通入4mol NH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%。下图中的曲线表示该反应在前25 s内NH3浓度随时间的变化而变化。
CO(NH2)2(l)+H2O(g) △H<0.某温度下,向容积为100L的密闭容器中通入4mol NH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%。下图中的曲线表示该反应在前25 s内NH3浓度随时间的变化而变化。
①0~25s、25s~40s内NH3的化学反应速率分别为__________ 、__________ 。存在差异的原因是______________________ 。
②该温度下此反应的平衡常数为_______________ 。
③请在图中画出反应从25s延续至60s时c(NH3)随时间变化的图象。并在其他条件不变的情况下画出使用催化剂时c(NH3)随时间的变化图象_______________
(2)尿素在一定条件下能将燃煤产生的烟气中的氮氧化物NOx转化为N2,下图表示的是尿素与某种烟气(主要为N2、NO和O2)中的NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率随温度变化的曲线
①曲线a对应CO(NH2)2 与NO的物质的量的比值是______ 。
②CO(NH2)2 与NO反应的化学方程式为________________ 。
③曲线a中,NO的起始浓度为6×10-4 mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为______ mg/(m3•s)。
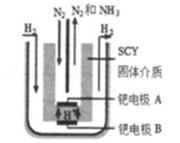
(3)希腊科学家采用高质子导电性的SYC陶瓷(能传递H+)为介质,用吸附在它外表面的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如下图)。钯电极A是电解池的____ (填“阳”或“阴”)极,该电极上的电极反应式是_________________ 。
(1)用氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g)
 CO(NH2)2(l)+H2O(g) △H<0.某温度下,向容积为100L的密闭容器中通入4mol NH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%。下图中的曲线表示该反应在前25 s内NH3浓度随时间的变化而变化。
CO(NH2)2(l)+H2O(g) △H<0.某温度下,向容积为100L的密闭容器中通入4mol NH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%。下图中的曲线表示该反应在前25 s内NH3浓度随时间的变化而变化。
①0~25s、25s~40s内NH3的化学反应速率分别为
②该温度下此反应的平衡常数为
③请在图中画出反应从25s延续至60s时c(NH3)随时间变化的图象。并在其他条件不变的情况下画出使用催化剂时c(NH3)随时间的变化图象
(2)尿素在一定条件下能将燃煤产生的烟气中的氮氧化物NOx转化为N2,下图表示的是尿素与某种烟气(主要为N2、NO和O2)中的NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率随温度变化的曲线

①曲线a对应CO(NH2)2 与NO的物质的量的比值是
②CO(NH2)2 与NO反应的化学方程式为
③曲线a中,NO的起始浓度为6×10-4 mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为
(3)希腊科学家采用高质子导电性的SYC陶瓷(能传递H+)为介质,用吸附在它外表面的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如下图)。钯电极A是电解池的
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
I.已知:NO2(g)+SO2(g) SO3(g)+NO(g)
SO3(g)+NO(g)
(1)一定条件下,将NO2与SO2以体积比1:2置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________ 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO2和NO2的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
e.气体密度保持不变
(2)若保持体积不变,升高温度,体系颜色加深,则说明该反应的∆H________ 0(填”>””<”或”=”)
II.对于反应2SO2(g)+O2(g) 2SO3(g);ΔH=-196.6kJ/mol。
2SO3(g);ΔH=-196.6kJ/mol。
在一定温度下,向一个容积不变的容器中,通入3mol SO2和2mol O2及固体催化剂,使之反应。平衡时容器内气体压强为起始时的90%。此时
(3)加入3mol SO2和2mol O2发生反应,达到平衡时,放出的热量为___________ 。
(4)保持同一温度,在相同的容器中,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,欲使起始时反应表现为向正反应方向进行,且平衡时SO3的体积分数为2/9,a的取值范围是____________ 。
(5)保持同一温度,在相同容器中,将起始物质的量改为3mol SO2、6mol O2、3mol SO3(g)及固体催化剂,则平衡_________ 移动。(填“正向、不、逆向或无法确定是否”)
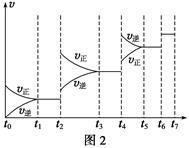
(6)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是__________ ;图中表示平衡混合物中SO3的含量最高的一段时间是____________ 。
(7)各阶段平衡时对应的平衡常数如下表所示:
K1、K2、K3、K4之间的关系为__________________ 。
I.已知:NO2(g)+SO2(g)
 SO3(g)+NO(g)
SO3(g)+NO(g)(1)一定条件下,将NO2与SO2以体积比1:2置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO2和NO2的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
e.气体密度保持不变
(2)若保持体积不变,升高温度,体系颜色加深,则说明该反应的∆H
II.对于反应2SO2(g)+O2(g)
 2SO3(g);ΔH=-196.6kJ/mol。
2SO3(g);ΔH=-196.6kJ/mol。在一定温度下,向一个容积不变的容器中,通入3mol SO2和2mol O2及固体催化剂,使之反应。平衡时容器内气体压强为起始时的90%。此时
(3)加入3mol SO2和2mol O2发生反应,达到平衡时,放出的热量为
(4)保持同一温度,在相同的容器中,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g)及固体催化剂,欲使起始时反应表现为向正反应方向进行,且平衡时SO3的体积分数为2/9,a的取值范围是
(5)保持同一温度,在相同容器中,将起始物质的量改为3mol SO2、6mol O2、3mol SO3(g)及固体催化剂,则平衡
(6)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是

(7)各阶段平衡时对应的平衡常数如下表所示:
| t1~t2 | t3~t4 | t5~t6 | t6~t7 |
| K1 | K2 | K3 | K4 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】如图表示反应N2(g)+3H2(g)  2NH3(g); △H<0 在某一时间段反应速率与反应过程的曲线关系图,
2NH3(g); △H<0 在某一时间段反应速率与反应过程的曲线关系图,
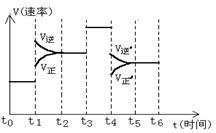
①达到平衡后,若只改变一个条件,则t1条件为______ ;t3条件为______ ;t4条件为______ ;
②则图中氨的百分含量最低的时间段是:( )
③请在右图中画出t6时刻既增加氢气浓度同时又减小氨气浓度的速率随时间的变化图。_____
 2NH3(g); △H<0 在某一时间段反应速率与反应过程的曲线关系图,
2NH3(g); △H<0 在某一时间段反应速率与反应过程的曲线关系图,
①达到平衡后,若只改变一个条件,则t1条件为
②则图中氨的百分含量最低的时间段是:
| A.t0-t1 | B.t2-t3 | C.t3-t4 | D.t5-t6 |
③请在右图中画出t6时刻既增加氢气浓度同时又减小氨气浓度的速率随时间的变化图。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】密闭容器中加入4molA、1.2molC和一定量的B三种气体,一定条件下发生反应,各物质的浓度随时间变化如甲图所示[已知t0~t1阶段保持恒温、恒容,且c(B)未画出]。乙图为t2时刻后改变反应条件,反应速率随时间的变化情况,已知在t2、t3、t4、t5时刻各改变一种不同的条件,其中t3时刻为使用催化剂。

(1)若t1=15s,则t0~t1阶段的反应速率为υ(C)=___________ 。
(2)t4时刻改变的条件为_____________ 。
(3)已知t0~t1阶段该反应放出或吸收的热量为Q kJ(Q 为正值),试写出该反应的热化学方程式:__________________________

(1)若t1=15s,则t0~t1阶段的反应速率为υ(C)=
(2)t4时刻改变的条件为
(3)已知t0~t1阶段该反应放出或吸收的热量为Q kJ(Q 为正值),试写出该反应的热化学方程式:
您最近一年使用:0次



