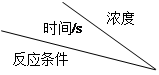(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应:COS(g)+ H2O(g)
 H2S(g) +CO2(g) △H=-34 kJ·mol1
H2S(g) +CO2(g) △H=-34 kJ·mol1氢解反应:COS(g) +H2(g)
 H2S(g)+CO(g) △H=+7 kJ·mol1。
H2S(g)+CO(g) △H=+7 kJ·mol1。已知:2H2(g) +O2(g)=== 2H2O(g) △H=-484 kJ·mol1。
写出表示CO燃烧热的热化学方程式:
(2)氢解反应达到平衡后,保持体系的温度和总压强不变,通入适量的He,正反应速率
(3)某温度下,向体积为2L的恒容密闭容器中通入2molCOS(g)和4molH2O(g),发生水解反应,5 min后反应达到平衡,测得COS(g)的转化率为75%。
回答下列问题:
①反应从起始至5 min 内,v(H2S)=
②该温度下,上述水解反应的平衡常数K=
相似题推荐
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1;该反应属于
(2)常温常压下,1mol乙醇(C2H5OH)完全燃烧生成CO2气体和液态水放出的热量为1367kJ,写出表示乙醇燃烧热的热化学方程式:
(3)根据盖斯定律计算:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1 ①
P(红磷,s)+
 O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1 ②
P4O10(s) ΔH=-738.5kJ·mol-1 ②则白磷转化为红磷的热化学方程式为
(4)已知破坏1molH-H键、1molI-I键、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘单质反应生成2molHI需要放出
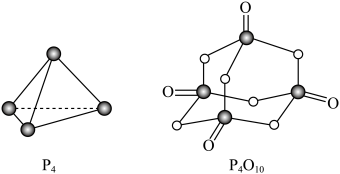
(5)白磷与氧可发生如下反应:P4+5O2=P4O10,已知断裂下列化学键需要吸收的能量分别为:P-P键akJ·mol-1、P-O键bkJ·mol-1、P=O键ckJ·mol-1、O=O键dkJ·mol-1。根据图示的分子结构和有关数据计算该反应的反应热为
(6)常温下,pH=1的H2SO4溶液,由水电离出来的c(H+)=
(7)H3BO3溶液中存在以下平衡:H3BO3(aq)+H2O(l)⇌[B(OH)4]-(aq)+H+(aq)。已知0.70mol/LH3BO3溶液在298K达到平衡时,c(H+)=2.0×10-5mol/L,水的电离忽略不计,求此温度下该反应的平衡常数K(保留2位有效数字):
(1)已知有关反应的能量变化如下图:

写出CH4(g)与H2O(g)反应制取CO(g)和H2(g)的热化学方程式:
(2)“CH4-CO2催化重整法”制氢气:CH4(g)+CO2(g)
 2CO (g)+2H2(g),ΔH
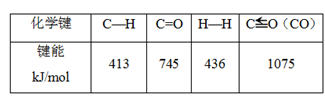
2CO (g)+2H2(g),ΔH不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。上述反应中相关的化学键键能数据如下表所示。①根据键能计算,该反应的ΔH=
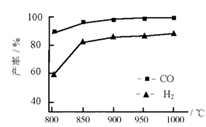
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图所示。实际生产中此反应优选温度为900℃,原因是
③某温度下,将1 mol CH4、2 mol CO2以及催化剂进行加入2 L容器中,达到平衡时α(CH4)=50%,平衡常数K=
(3)合成气在进入合成塔前常用醋酸二氨合铜(Ⅰ)溶液来吸收其中的CO杂质,其反应是:Cu(NH3)2(CH3COO)+CO+NH3
 Cu(NH3)3(CH3COO)·CO ΔH<0
Cu(NH3)3(CH3COO)·CO ΔH<0必须除去原料气中CO的原因是
醋酸二氨合铜(Ⅰ)吸收CO的生产适宜条件应是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
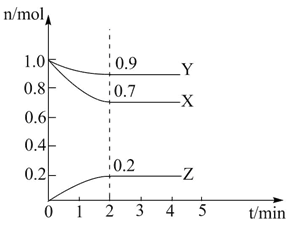
(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=
Ⅱ.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比
(1)一定能证明I2(g)+H2(g)
 2HI(g)达到平衡状态的是
2HI(g)达到平衡状态的是(2)一定能证明A(s)+2B(g)
 C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是(一)将影响反应速率条件填在空格处。
(1)
| 实例 | 影响反应速率条件 |
| ①食物放在冰箱里能延长保质期 | |
| ②实验室将块状药品研细,再进行反应 | 固体表面积 |
③用 分解制 分解制 时,加入 时,加入 | |
④实验室制备 时,用较浓的硫酸与 时,用较浓的硫酸与 粒反应 粒反应 | 浓度 |
(二)如下图所示,800℃时
 、
、 、
、 三种气体在密闭容器中反应时的浓度变化,分析图象,回答问题:
三种气体在密闭容器中反应时的浓度变化,分析图象,回答问题: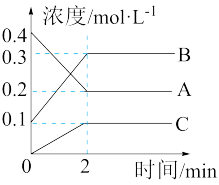
(2)2min内,用C表示的反应速率为
(3)在其他条件下,测得A的反应速率为
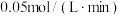 ,此时的反应与800℃时相比,
,此时的反应与800℃时相比,A.比800度时快 B. 比800℃时慢 C. 和800℃时速率一样
用10 mL H2O2制取150 mL O2所需时间(s)
| 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
无催化剂、加热 | 360 | 480 | 540 | 720 |
MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
①上述实验结果体现了
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率的影响:
(2)某温度时,在一个2 L的密闭容器中,M、N、W三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
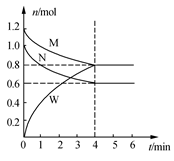
①该反应的化学方程式为
②从反应开始至4 min,N的平均反应速率为
【推荐1】(Ⅰ).下列平衡体系均有颜色。改变条件后,平衡怎样移动?(选填“向左移动”“向右移动”或“不移动”)颜色怎样变化?(选填“变深”“变浅”或“不变”)
(1)FeCl3+3KSCN
 Fe(SCN)3+3KCl:加少许KCl固体:平衡
Fe(SCN)3+3KCl:加少许KCl固体:平衡(2)2NO2
 N2O4 ΔH<0:迅速加压:平衡
N2O4 ΔH<0:迅速加压:平衡(3)2HI
 H2+I2(g) ΔH>0:加压:平衡
H2+I2(g) ΔH>0:加压:平衡(Ⅱ) .对于反应x A(g)+y B(g) p C(g)+q D(g),压强与温度对C的质量分数的影响如图:
p C(g)+q D(g),压强与温度对C的质量分数的影响如图:
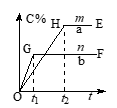
(4)若m、n表示不同温度,则m
(5)若m、n表示不同压强,则m
(6)b曲线的OG段比a曲线的OH段陡的原因是
(7)a曲线的HE段高于b曲线的GF段的原因是

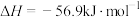 ,请回答下列问题。
,请回答下列问题。(1)将一定量的NO2和N2O4混合气体充入恒容密闭容器中,反应一段时间,能说明该反应达到化学平衡状态的是_______(填字母)。
| A.容器内气体颜色保持不变 |
| B.单位时间内消耗2n mol NO2,同时生成n mol N2O4 |
| C.容器内气体的压强不随时间变化 |
| D.容器内气体质量不随时间变化 |
 向
向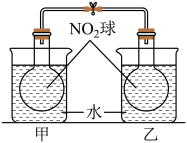
(3)将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。
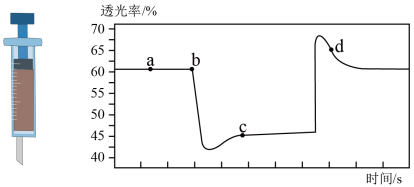
①b点的操作是
②c点与a点相比,c(NO2)
③若不忽略体系温度变化,且没有能量损失,则温度Tb
(1)增加C(s),则平衡
(2)保持温度不变,增大反应容器的容积,则c(CO2)
(3)保持反应容器的容积和温度不变,通入He,则平衡
(4)保持反应容器的容积不变,升高温度,则平衡时c(CO)
II.氢能是一种极具发展潜力的清洁能源。以下反应是目前大规模制取氢气的重要方法之一:
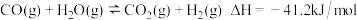
(5)欲提高CO的平衡转化率,理论上可以采取的措施为__________。
| A.增大压强 | B.升高温度 | C.加入催化剂 | D.通入过量水蒸气 |
 CH3OH(g) ΔH=akJ•mol-1),其中X、Y的物质的量与时间的关系如图所示,反应进行1min时三种物质的体积分数均相等。
CH3OH(g) ΔH=akJ•mol-1),其中X、Y的物质的量与时间的关系如图所示,反应进行1min时三种物质的体积分数均相等。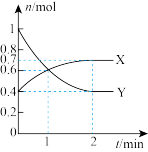
(1)Y为
(2)0~1min时v(CO)为
(3)该温度下,该反应的平衡常数Kc=
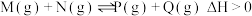 。在某温度下,反应物的起始浓度分别为
。在某温度下,反应物的起始浓度分别为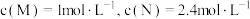 。达到平衡后,
。达到平衡后, 的转化率为
的转化率为 。请回答下列问题:
。请回答下列问题:(1)此时
 的转化率为
的转化率为(2)若温度升高,则
 的转化率
的转化率(3)若反应温度不变,反应物的起始浓度分别为
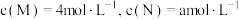 ;达到平衡后,
;达到平衡后,
(4)若反应温度不变,反应物的起始浓度为
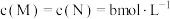 ,达到平衡后,
,达到平衡后, 的转化率为
的转化率为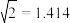 )。
)。
I.在2L密闭容器中,充入10molCO2和32molH2,在催化剂、200°C的条件下发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。部分反应物和产物随时间变化如下图所示:
CH3OH(g)+H2O(g)。部分反应物和产物随时间变化如下图所示:
(1)0~2min末,以H2的浓度变化表示反应的平均速率为
(2)该温度下反应的化学平衡常数为
(3)下列情况能说明该反应达到化学平衡状态的是___________(填字母)。
| A.单位时间内消耗1molCO2,同时生成1molCH3OH |
| B.密闭容器中n(CO2):n(H2O)不发生变化 |
| C.CO2、H2、CH3OH浓度之比为1:3:1的状态 |
| D.密闭容器内混合气体的平均摩尔质量不发生变化 |
II.CO和H2也可合成甲醇:CO(g)+2H2(g)
 CH3OH(g),△H<0
CH3OH(g),△H<0(4)下列措施中能增大反应速率且利于平衡正向移动的是___________
| A.升高反应温度 | B.将CH3OH与反应混合物分离 | C.使用高效催化剂 | D.增大体系压强 |
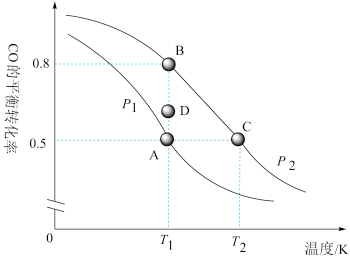
压强p1