(1)常温下将0.2mol/L HCl溶液与0.2mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中由水电离出的c(H+)与0.1mol/LHCl溶液中由水电离出的c(H+)之比为_______
②求出混合溶液中下列算式的精确计算结果(填具体数字):c(Cl-)-c(M+)=____________ mol/L。
(2)常温下若将0.2mol/L MOH溶液与0.1mol/L HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度___________ MCl的水解程度。(填“>”、“<”、或“=”)
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH____________ 。(填“>7”、“<7”、或“无法确定”)
①混合溶液中由水电离出的c(H+)与0.1mol/LHCl溶液中由水电离出的c(H+)之比为
②求出混合溶液中下列算式的精确计算结果(填具体数字):c(Cl-)-c(M+)=
(2)常温下若将0.2mol/L MOH溶液与0.1mol/L HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH
更新时间:2017-12-17 14:24:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下列化合物:①HCl②NaOH③CH3COOH④NH3·H2O⑤CH3COONa⑥NH4Cl。
(1)溶液呈碱性的有___________ (填序号)。
(2)常温下0.05mol/LH2SO4溶液的pH=___________ ;pH=10的CH3COONa溶液中由水电离产生的c(OH-)=___________ mol/L。
(3)用离子方程式解释泡沫灭火器灭火原理___________ 。
(4)将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的pH仍相等m___________ n(填“大于、等于、小于”)。
(5)FeCl3的水溶液呈___________ (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):___________ ;实验室在配制FeCl3的溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以___________ (填“促进”、“抑制”)其水解。
(6)把氯化铝溶液蒸干,灼烧,最后得到的主要固体产物是___________ 。
(1)溶液呈碱性的有
(2)常温下0.05mol/LH2SO4溶液的pH=
(3)用离子方程式解释泡沫灭火器灭火原理
(4)将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的pH仍相等m
(5)FeCl3的水溶液呈
(6)把氯化铝溶液蒸干,灼烧,最后得到的主要固体产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】温度为t℃时,某NaOH稀溶液中c(H+)=10 -amol•L -1,c(OH -)=10 -bmol•L -1;已知:a+b=13,请回答下列问题:
(1)该温度下水的离子积常数Kw=___________ ,t___________ (填“<”、“>”或“=”)25。
(2)该NaOH溶液中NaOH的物质的量浓度为___________ ,该NaOH溶液中由水电离出的c(OH -)为___________ 。
(3)回答下列有关醋酸的问题。
在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示:

①加水量为0时,导电能力也为0,请解释原因:___________ 。
②a、b、c三点醋酸电离程度由大到小的顺序为___________ ;a、b、c三点对应的溶液中,pH最小的是___________ ;a、b、c三点对应的溶液中,水的电离程度最大的是___________ 。
(1)该温度下水的离子积常数Kw=
(2)该NaOH溶液中NaOH的物质的量浓度为
(3)回答下列有关醋酸的问题。
在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示:

①加水量为0时,导电能力也为0,请解释原因:
②a、b、c三点醋酸电离程度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答下列问题:
(1)84消毒液是一种以NaClO为主要成分的高效消毒剂,NaClO溶液呈___________ 性(填“酸”“碱”或“中”),原因可用离子方程式表示为___________ 。
(2)常温下,某柠檬水的pH为3,则其中的c(OH-)为___________ 。
(3)浓度均为0.1mol/L的盐酸、硫酸和醋酸,其中pH最小的是___________ 。
(4)在某温度下,向含有BaSO4固体的BaSO4饱和溶液中加入少量稀硫酸,则c(Ba2+)___________ (填“增大”“减小”或“不变”,下同),Ksp___________ 。
(1)84消毒液是一种以NaClO为主要成分的高效消毒剂,NaClO溶液呈
(2)常温下,某柠檬水的pH为3,则其中的c(OH-)为
(3)浓度均为0.1mol/L的盐酸、硫酸和醋酸,其中pH最小的是
(4)在某温度下,向含有BaSO4固体的BaSO4饱和溶液中加入少量稀硫酸,则c(Ba2+)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.室温下,0.01 mol/ L的盐酸溶液的pH是____ ,0.05 mol/ L的Ba(OH)2溶液的pH是___ ,pH=3的盐酸稀释100倍,所得溶液pH是____ ,pH = 9的NaOH溶液稀释1000倍后溶液中c(OH−)与c(Na+)之比是___ 。
Ⅱ.水的电离平衡曲线如下图所示。

(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从____ 增加到____ 。
(2)100℃的温度下将pH=8的KOH溶液与pH=5的稀H2SO4混合,并保持100℃的恒温,欲使混合溶液pH=7,则KOH溶液与稀H2SO4的体积比是____ 。
Ⅱ.水的电离平衡曲线如下图所示。

(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
(2)100℃的温度下将pH=8的KOH溶液与pH=5的稀H2SO4混合,并保持100℃的恒温,欲使混合溶液pH=7,则KOH溶液与稀H2SO4的体积比是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】a常温下,回答下列关于酸和碱中和反应的问题:
将某一元酸HA 和NaOH溶液等体积混合,分别进行编号①、②、③的实验,实验数据记录事表
请回答:
(1)根据①组实验情况,混合溶液pH=9的原因是_____________ (用离子方程式表示)。
(2)混合溶液①中由水电离出的c (H+)_____ 0.1mol/LNaOH溶液中由水电离出的c(H+)。(填“>”“<”或“=”)
(3)根据①组实验情况,在该溶液中下列关系式正确的是(填序号字母)______ 。
A.c(Na+)+c(H+) =c(OH-) +c(A-)
B.c(Na+) =c(HA) +c(A-)
C.c (HA)+c(H+) =c(OH-)
D.c(Na+) +c(H+) =c(OH-) +c(A-) +c (HA)
(4)②组情况表明,c_________ 0.2mol/L (选填“>”、“<”或“=”)。混合溶液中离子浓度c(A-)____ c(Na+) (选填“>”、“<”或“=”)。
(5)从③组实验结果分析,离子浓度由大到小的顺序是_________________________ 。
将某一元酸HA 和NaOH溶液等体积混合,分别进行编号①、②、③的实验,实验数据记录事表
| 序号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH>9 |
请回答:
(1)根据①组实验情况,混合溶液pH=9的原因是
(2)混合溶液①中由水电离出的c (H+)
(3)根据①组实验情况,在该溶液中下列关系式正确的是(填序号字母)
A.c(Na+)+c(H+) =c(OH-) +c(A-)
B.c(Na+) =c(HA) +c(A-)
C.c (HA)+c(H+) =c(OH-)
D.c(Na+) +c(H+) =c(OH-) +c(A-) +c (HA)
(4)②组情况表明,c
(5)从③组实验结果分析,离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】运用所学知识,解决下列问题。
(1)95 ℃蒸馏水呈___________ (填“酸”、“碱”或“中”)性。
(2)常温下,0.1 mol·L-1 CH3COOH溶液加水稀释10倍,n(H+)___________ ,  的值
的值___________ 。(填 “增大”、“减小”或“不变”)
(3)25℃时,欲使水电离产生的c(H+)=10-13mol·L-1,配制1 L溶液,应向其中加入5.0 mol·L-1的盐酸溶液___________ L或加入NaOH固体___________ g。
(4)25℃时,将0.1 mol/L盐酸和0.06 mol/L Ba(OH)2溶液等体积混合的pH=___________ 。(设混合过程体积变化忽略不计)
(5)25℃时,若测得HR溶液的pH=a,取该溶液10.0 mL,加蒸馏水稀释至100.0 mL,测得pH=b,b-a<1,则HR___________ 是弱酸。(填 “一定”、“一定不”或“不一定”)
(1)95 ℃蒸馏水呈
(2)常温下,0.1 mol·L-1 CH3COOH溶液加水稀释10倍,n(H+)
 的值
的值(3)25℃时,欲使水电离产生的c(H+)=10-13mol·L-1,配制1 L溶液,应向其中加入5.0 mol·L-1的盐酸溶液
(4)25℃时,将0.1 mol/L盐酸和0.06 mol/L Ba(OH)2溶液等体积混合的pH=
(5)25℃时,若测得HR溶液的pH=a,取该溶液10.0 mL,加蒸馏水稀释至100.0 mL,测得pH=b,b-a<1,则HR
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知常温下部分弱电解质的电离平衡常数如下表(已知lg2=0.3):
(1)常温下,0.1mol/L的HClO溶液和0.1mol/L的NaClO溶液等体积混合,判断混合溶液的酸碱性___________ (填“酸性”“碱性”“中性”)。
(2)25℃时,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应后溶液呈中性,用含a的代数式表示NH3·H2O的电离平衡常数Kb___________ 。
(3)CO2可以被NaOH溶液捕获。若所得溶液中c(CO )=c(H2CO3)时,则溶液的pH=
)=c(H2CO3)时,则溶液的pH=______ 。
(4)含H2S的尾气用足量的Na2CO3溶液来吸收,写出离子方程式:___________ 。
(5)已知100℃下,Kw=10-12.将pH11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则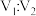 =
=___________ 。
(6)常温下,向0.1mol/LH2S溶液中通入HCl气体或加入NaOH固体,测得c(S2-)与溶液pH的关系如图(忽略溶液体积的变化及H2S的挥发)。请计算:

①当溶液中c(S2-)=1.4×10-19mol/L溶液时,水电离产生的c(H+)___________ mol/L。
②当pH=13时,溶液中c(H2S)+c(HS-)=___________ mol/L。
| 化学式 | H2S | HClO | H2CO3 |
| 电离常数 | K1=9.1×10-8 K2=1.1×10-12 | 4.7×10-8 | K1=4×10-7 K2=5×10-11 |
(1)常温下,0.1mol/L的HClO溶液和0.1mol/L的NaClO溶液等体积混合,判断混合溶液的酸碱性
(2)25℃时,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应后溶液呈中性,用含a的代数式表示NH3·H2O的电离平衡常数Kb
(3)CO2可以被NaOH溶液捕获。若所得溶液中c(CO
 )=c(H2CO3)时,则溶液的pH=
)=c(H2CO3)时,则溶液的pH=(4)含H2S的尾气用足量的Na2CO3溶液来吸收,写出离子方程式:
(5)已知100℃下,Kw=10-12.将pH11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则
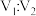 =
=(6)常温下,向0.1mol/LH2S溶液中通入HCl气体或加入NaOH固体,测得c(S2-)与溶液pH的关系如图(忽略溶液体积的变化及H2S的挥发)。请计算:

①当溶液中c(S2-)=1.4×10-19mol/L溶液时,水电离产生的c(H+)
②当pH=13时,溶液中c(H2S)+c(HS-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】常温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
(1)HA为___________ (填“强酸”、“弱酸”或“无法确定”)
(2)x___________ 0.2(填:“<”、“=”、“>”)
(3)实验②反应后的溶液中离子浓度由大到小的顺序为___________
(4)实验①反应后的溶液中c(K+)___________ c(A-)+c(HA) (填:“<”、“=”、“>”)
(5)0.2 mol∙L−1的HA和0.1 mol∙L−1的KOH等体积混合充分反应后所得的溶液中c(HA)___________ c(A-) (填:“<”、“=”、“>”)
| 实验编号 | 起始浓度/ mol∙L−1 | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
(1)HA为
(2)x
(3)实验②反应后的溶液中离子浓度由大到小的顺序为
(4)实验①反应后的溶液中c(K+)
(5)0.2 mol∙L−1的HA和0.1 mol∙L−1的KOH等体积混合充分反应后所得的溶液中c(HA)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】温下,将四种不同的一元酸(用 HA 代表)分别和 NaOH 溶液等体积混合。 两种溶液的物质的量浓度和混合溶液的 pH 如下表所示:
(1)从甲组情况分析,如何判断 HA 是强酸还是弱酸?___________
(2)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是:____________________
(3)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式表示):c(Na+)-c(A-)=______ mol·L-1。
(4)某二元酸(化学式用 H2B 表示)在水中的电离方程式是:H2B=H++HB- HB- H++B2-
H++B2-
在0.1 mol·L-1 的 Na2B 溶液中,下列粒子浓度关系式正确的是________ 。
A.c(B2-)+c(HB-)=0.1 mol·L-1 B.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
C.c(OH-)=c(H+)+c(HB-) D.c(Na+)+c(H+)=c(OH-)+c(HB-)
| 实验 | HA 物质的量 | NaOH 物质的量 | 混合后溶 |
| 编号 | 浓度/(mol·L-1) | 浓度/(mol·L-1) | 液的 pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=11 |
(1)从甲组情况分析,如何判断 HA 是强酸还是弱酸?
(2)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是:
(3)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式表示):c(Na+)-c(A-)=
(4)某二元酸(化学式用 H2B 表示)在水中的电离方程式是:H2B=H++HB- HB-
 H++B2-
H++B2-在0.1 mol·L-1 的 Na2B 溶液中,下列粒子浓度关系式正确的是
A.c(B2-)+c(HB-)=0.1 mol·L-1 B.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
C.c(OH-)=c(H+)+c(HB-) D.c(Na+)+c(H+)=c(OH-)+c(HB-)
您最近一年使用:0次



