醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐(已知:25℃,Ka(CH3COOH)=1.69×10-5)。
(1)醋酸钠溶液呈碱性的原因是_______________ (写出有关的离子方程式)
(2)在CH3COONa溶液中离子浓度由大到小的顺序为_____________________ (用c(Bn+)表示相应离子浓度);
(3)25℃时,0.10mol/L的醋酸溶液的pH约为___________ ( 已知:lg1.3=0.114);
(4)对于醋酸溶液和醋酸钠溶液的下列说法正确的是____________ ;
A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小.
B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解.
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离.
D.醋酸和醋酸钠混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离.
(5)物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合(注:混合前后溶液体积变化忽略不计),混合液中的下列关系式正确的是_______ ;
A.c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B.c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.c(CH3COO-)+c(CH3COOH)=0.1mol/L
(6)常温时,有以下3种溶液,其中pH最小的是____________ ;
A.0.02mol•L-1CH3COOH与0.02mol•L-1NaOH溶液等体积混合液
B.0.03mol•L-1CH3COOH与0.01mol•L-1NaOH溶液等体积混合液
C.pH=2的CH3COOH与pH=12的NaOH溶液等体积混合液
(7)用pH试纸在常温下分别测定0.10mol/L的醋酸钠溶液和0.10mol/L的碳酸钠溶液,则pH(CH3COONa)_______ pH(Na2CO3).(填:“>”、“<”或“=”)
(1)醋酸钠溶液呈碱性的原因是
(2)在CH3COONa溶液中离子浓度由大到小的顺序为
(3)25℃时,0.10mol/L的醋酸溶液的pH约为
(4)对于醋酸溶液和醋酸钠溶液的下列说法正确的是
A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小.
B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解.
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离.
D.醋酸和醋酸钠混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离.
(5)物质的量浓度均为0.1mol/L的CH3COONa和CH3COOH溶液等体积混合(注:混合前后溶液体积变化忽略不计),混合液中的下列关系式正确的是
A.c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B.c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.c(CH3COO-)+c(CH3COOH)=0.1mol/L
(6)常温时,有以下3种溶液,其中pH最小的是
A.0.02mol•L-1CH3COOH与0.02mol•L-1NaOH溶液等体积混合液
B.0.03mol•L-1CH3COOH与0.01mol•L-1NaOH溶液等体积混合液
C.pH=2的CH3COOH与pH=12的NaOH溶液等体积混合液
(7)用pH试纸在常温下分别测定0.10mol/L的醋酸钠溶液和0.10mol/L的碳酸钠溶液,则pH(CH3COONa)
17-18高三上·内蒙古巴彦淖尔·期末 查看更多[8]
内蒙古巴彦淖尔市杭锦后旗奋斗中学2017-2018学年高三第一学期第四次月考(期末)化学试题【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期12月月考化学试题内蒙古呼和浩特市土默特左旗第一中学2019-2020学年高二上学期第二次月考化学试题河南省焦作市沁阳市第一中学2019-2020高二月考考试化学试题(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点25 盐类的水解-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)第三章 第三节 盐类的水解 第2课时 影响盐类水解的因素 水解原理的应用
更新时间:2018-02-07 10:32:02
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】Ⅰ.据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+205.9 kJ·mol-1 ①
CO(g)+3H2(g) ΔH1=+205.9 kJ·mol-1 ①
CO(g)+H2O(g) CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 ②
CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 ②
二氧化碳重整:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH3 ③
2CO(g)+2H2(g) ΔH3 ③
则反应①自发进行的条件是______________ ,ΔH3=______________ kJ·mol-1。
Ⅱ.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g) 2NH3(g)。
2NH3(g)。
(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1 mol、0.3 mol时,平衡后混合物中氨的体积分数(φ)如下图所示。
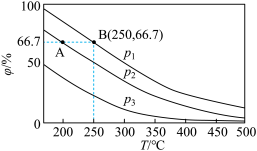
①其中,p1、p2和p3由大到小的顺序是______________________________ ,其原因是__________________________________________________________________ 。
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)________ vB(N2)(填“>”“<”或“=”)。
③若在250 ℃、p1为105 Pa条件下,反应达到平衡时容器的体积为1 L,则该条件下B点N2的分压p(N2)为_____________________ Pa (分压=总压×物质的量分数,保留一位小数)。
Ⅲ.以连二硫酸根(S2O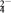 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:

(3)①阴极区的电极反应式为_________________________________ 。
②NO吸收转化后的主要产物为NH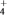 ,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上吸收的NO在标准状况下的体积为________ mL。
Ⅳ、常温下,将a mol·L-1的醋酸与b mol·L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=___________ (用含a和b的代数式表示)。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+205.9 kJ·mol-1 ①
CO(g)+3H2(g) ΔH1=+205.9 kJ·mol-1 ①CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 ②
CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1 ②二氧化碳重整:CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH3 ③
2CO(g)+2H2(g) ΔH3 ③则反应①自发进行的条件是
Ⅱ.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)
 2NH3(g)。
2NH3(g)。(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1 mol、0.3 mol时,平衡后混合物中氨的体积分数(φ)如下图所示。

①其中,p1、p2和p3由大到小的顺序是
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)
③若在250 ℃、p1为105 Pa条件下,反应达到平衡时容器的体积为1 L,则该条件下B点N2的分压p(N2)为
Ⅲ.以连二硫酸根(S2O
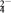 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
(3)①阴极区的电极反应式为
②NO吸收转化后的主要产物为NH
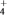 ,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3 mol e-,则此通电过程中理论上吸收的NO在标准状况下的体积为Ⅳ、常温下,将a mol·L-1的醋酸与b mol·L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A==H++HA-、HA- H++A2-
H++A2-
回答下列问题:
(1)Na2A溶液显____________ (填“酸性”“中性”或“碱性”)。理由是____________ (用离子方程式表示)。
(2)在0.1mol·L-1的Na2A溶液中,下列粒子浓度关系式正确的是____________ 。
A.c(A2-)+c(HA-)+c(H2A)=0.1mol·L-1 B.c(Na+)+c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) D.c(Na+)=2c(A2-)+2c(HA-)
(3)已知0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1H2A溶液中氢离子的物质的量浓度可能是____________ 0.11mol·L-1(填“<”“>”或“=”),理由是____________ 。
(4)0.1mol·L-1NaHA溶液中各种离子浓度由大到小的顺序是____________ 。
 H++A2-
H++A2-回答下列问题:
(1)Na2A溶液显
(2)在0.1mol·L-1的Na2A溶液中,下列粒子浓度关系式正确的是
A.c(A2-)+c(HA-)+c(H2A)=0.1mol·L-1 B.c(Na+)+c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) D.c(Na+)=2c(A2-)+2c(HA-)
(3)已知0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1H2A溶液中氢离子的物质的量浓度可能是
(4)0.1mol·L-1NaHA溶液中各种离子浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】甲酸是一种有机弱酸,有望成为理想的氢能储存和运输载体。
(1)常温下,测得 溶液的
溶液的 ,试计算
,试计算
_______ (用科学记数法表示,保留小数点后一位)。
(2)甲酸可通过电解法制备,其原理如图所示:

①电极a应与外接直流电源的_______ 极(填“正”或“负”)相连,生成甲酸的电极反应式为_______ 。
②电极b附近开始阶段发生的反应可能有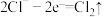 、
、_______ 等(用离子方程式表示)。
(3)某溶液中 含量的测定:取
含量的测定:取 待测溶液置于锥形瓶中,滴入2~3滴指示剂,用
待测溶液置于锥形瓶中,滴入2~3滴指示剂,用 标准溶液滴定(假设滴定时只有
标准溶液滴定(假设滴定时只有 参加反应)。
参加反应)。
①其中第三次读数时滴定管终点的液面位置如图所示,则该次滴定终点的读数为_______  。
。

②若消耗 标准溶液的平均体积为
标准溶液的平均体积为 ,则甲酸的质量浓度为
,则甲酸的质量浓度为_______  。
。
③滴定过程中,若滴定前平视刻度线读数,滴定达到终点时俯视刻度线读数,会使实验结果_______ (“偏大”“偏小”或“无影响”)。
(1)常温下,测得
 溶液的
溶液的 ,试计算
,试计算
(2)甲酸可通过电解法制备,其原理如图所示:

①电极a应与外接直流电源的
②电极b附近开始阶段发生的反应可能有
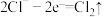 、
、(3)某溶液中
 含量的测定:取
含量的测定:取 待测溶液置于锥形瓶中,滴入2~3滴指示剂,用
待测溶液置于锥形瓶中,滴入2~3滴指示剂,用 标准溶液滴定(假设滴定时只有
标准溶液滴定(假设滴定时只有 参加反应)。
参加反应)。①其中第三次读数时滴定管终点的液面位置如图所示,则该次滴定终点的读数为
 。
。
②若消耗
 标准溶液的平均体积为
标准溶液的平均体积为 ,则甲酸的质量浓度为
,则甲酸的质量浓度为 。
。③滴定过程中,若滴定前平视刻度线读数,滴定达到终点时俯视刻度线读数,会使实验结果
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
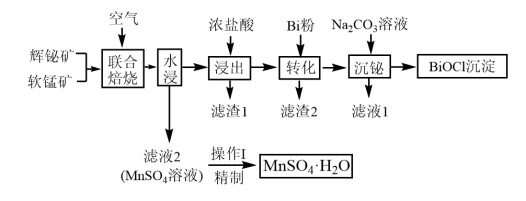
【推荐1】以辉铋矿(主要成分为Bi2S3,含有CuS、FeS2、SiO2杂质)和软锰矿(主要成分为MnO2)为原料联合制备BiOCl和MnSO4•H2O的工艺流程如图:
已知:①金属活动性:Fe>Bi>Cu。
②Bi3+易水解为BiOCl沉淀;常温下,BiOCl存在的pH范围约为2.0~11.0。
③常温下,该工艺中有关金属离子开始沉淀和完全沉淀的pH见表。
(1)“联合焙烧”时Bi2S3、FeS2、CuS分别转化为Bi2O3、Fe2O3、CuO,写出生成MnSO4和Bi2O3的化学方程式:_______ 。
(2)“浸出”时需及时补充浓盐酸调节浸取液的pH≈l.4,其目的是_______ 。
(3)“滤渣1”的主要成分为_______ (填化学式)。
(4)“转化”时加入足量金属Bi的目的是________ (用离子方程式表示)。
(5)为保证BiOCl产品的纯度,理论上“沉铋”时应控制溶液的pH范围为_______ 。
(6)将100kg辉铋矿进行“联合焙烧”,“转化”时消耗2.0kg金属Bi,假设其余各步损失不计,干燥后称量BiOCl产品质量为47.5kg,滴定测得产品中Bi的质量分数为80.0%。辉铋矿中Bi元素的质量分数为_______ %(保留3位有效数字)。
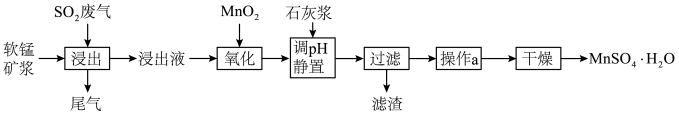
(7)已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。则从“滤液2”中获得较高纯度MnSO4•H2O的“操作I”为控制温度在80~90℃、_______ 、_______ 、用80~90℃蒸馏水洗涤2~3次、真空干燥。

| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe2+ | 6.3 | 8.3 |
| Fe3+ | 1.6 | 3.1 |
②Bi3+易水解为BiOCl沉淀;常温下,BiOCl存在的pH范围约为2.0~11.0。
③常温下,该工艺中有关金属离子开始沉淀和完全沉淀的pH见表。
(1)“联合焙烧”时Bi2S3、FeS2、CuS分别转化为Bi2O3、Fe2O3、CuO,写出生成MnSO4和Bi2O3的化学方程式:
(2)“浸出”时需及时补充浓盐酸调节浸取液的pH≈l.4,其目的是
(3)“滤渣1”的主要成分为
(4)“转化”时加入足量金属Bi的目的是
(5)为保证BiOCl产品的纯度,理论上“沉铋”时应控制溶液的pH范围为
(6)将100kg辉铋矿进行“联合焙烧”,“转化”时消耗2.0kg金属Bi,假设其余各步损失不计,干燥后称量BiOCl产品质量为47.5kg,滴定测得产品中Bi的质量分数为80.0%。辉铋矿中Bi元素的质量分数为
(7)已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。则从“滤液2”中获得较高纯度MnSO4•H2O的“操作I”为控制温度在80~90℃、

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】从铝土矿废料“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中提钪与TiO2的一种工艺流程如图:

已知:①钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。
②该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如表:
请回答以下问题:
(1)Sc元素在元素周期表中的位置:____ 。
(2)试计算“反萃取”时,使Sc3+恰好完全沉淀(浓度为1.0×10-6)的pH=____ (已知:Ksp[Sc(OH)3]=8.00×10-30,lg2=0.30,计算结果保留3位有效数字)。
(3)“反萃取”时若加入的NaOH过量则Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式____ 。
(4)常温下,三价Sc的几种存在形式与F-浓度的对数[1gc(F-)]、pH的关系如图所示。若溶液中c(F-)=5×10-6,“调pH”过程中控制pH=4.0,则调pH后三价Sc的存在形式为____ (填化学式)(已知:lg5=0.7)。

(5)钪的萃取率(E%)与O/A值[萃取剂体积(O)和酸液体积(A)之比]的关系如图,应.选择的合适O/A值为____ 。

(6)向“水相”中加入铁粉的目的是____ 。
(7)“水解”过程中,加水稀释后,TiOSO4水解为TiO2·xH2O的离子方程式为____ 。

已知:①钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。
②该工艺条件下,溶液中相关离子开始沉淀和完全沉淀的pH值如表:
| 离子 | Fe2+ | Fe3+ | Al3+ | TiO2+ |
| 开始沉淀pH | 7.0 | 1.9 | 3.0 | 0.3 |
| 完全沉淀pH | 9.0 | 3.2 | 4.7 | 2.0 |
(1)Sc元素在元素周期表中的位置:
(2)试计算“反萃取”时,使Sc3+恰好完全沉淀(浓度为1.0×10-6)的pH=
(3)“反萃取”时若加入的NaOH过量则Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式
(4)常温下,三价Sc的几种存在形式与F-浓度的对数[1gc(F-)]、pH的关系如图所示。若溶液中c(F-)=5×10-6,“调pH”过程中控制pH=4.0,则调pH后三价Sc的存在形式为

(5)钪的萃取率(E%)与O/A值[萃取剂体积(O)和酸液体积(A)之比]的关系如图,应.选择的合适O/A值为

(6)向“水相”中加入铁粉的目的是
(7)“水解”过程中,加水稀释后,TiOSO4水解为TiO2·xH2O的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】利用低品位软锰矿浆(主要成分是 ,还有少量的
,还有少量的 、
、 等)吸收含
等)吸收含 的废气制备硫酸锰晶体,可实现资源的综合利用和环境治理。
的废气制备硫酸锰晶体,可实现资源的综合利用和环境治理。
已知浸出液的pH<2,有关金属离子形成氢氧化物沉淀时的pH见下表:
(1)用石灰浆调节pH的范围是_______ ;若溶液中的离子浓度为 时可认为该离子已被除去,则
时可认为该离子已被除去,则 的
的
_______ 。
(2)氧化的主要目的是_______ ,反应的离子方程式为_______ 。
(3)用化学平衡原理解释pH≥8.5时 溶解的原因:
溶解的原因:_______ 。
(4)在 隔绝空气脱水时,是否需要加入适量的硫酸?
隔绝空气脱水时,是否需要加入适量的硫酸?_______ (填“是”或“否”),其原因是_______ 。
 ,还有少量的
,还有少量的 、
、 等)吸收含
等)吸收含 的废气制备硫酸锰晶体,可实现资源的综合利用和环境治理。
的废气制备硫酸锰晶体,可实现资源的综合利用和环境治理。
已知浸出液的pH<2,有关金属离子形成氢氧化物沉淀时的pH见下表:
| 离子 |  |  |  |  |
| 开始沉淀时的pH | 7.6 | 2.7 | 3.8 | 8.3 |
| 完全沉淀时的pH | 9.7 | 3.7 | 4.7(≥8.5溶解) | 9.8 |
 时可认为该离子已被除去,则
时可认为该离子已被除去,则 的
的
(2)氧化的主要目的是
(3)用化学平衡原理解释pH≥8.5时
 溶解的原因:
溶解的原因:(4)在
 隔绝空气脱水时,是否需要加入适量的硫酸?
隔绝空气脱水时,是否需要加入适量的硫酸?
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】硫单质及其化合物在工农业生产中有着重要的应用。
(1)已知25℃时:O2(g)+S(s)=SO2(g)△H=-akJ·mol-1
O2(g) +2SO2(g)⇌2SO3(g) △H = -b kJ·mol-1
写出SO3(g)分解生成O2(g)与S(s)的热化学方程式:__________________ 。
(2)研究SO2催化氧化生成SO3的反应,回答下列相关问题:
①甲图是SO2(g)和SO3(g)的浓度随时间的变化情况。反应从开始到平衡时,用O2表示的平均反应速率为__________________ 。
②在一容积可变的密闭容器中充入20 mol SO2(g)和10mol O2(g),O2的平衡转化率随温度(T)、压强(P)的变化如图乙所示。则P1与P2的大小关系是P1______ P2( “>”“ <”或“=”),A、B、C三点的平衡常数大小关系为__________ (用KA、KB、KC和“<”“>”或“=”表示)。
(3)常温下,H2SO3的电离平衡常数Ka1=1.54×10-2,Ka2=1.02×10-7。
①将SO2通入水中反应生成H2SO3。试计算常温下H2SO3⇌2H++SO32-的平衡常数K =_____ 。(结果保留小数点后两位数字)
②浓度均为0. 1 mol • L-1的Na2SO3、NaHSO3混合溶液中,
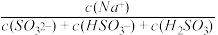 =
=________ 。
(4)往1 L0.2 mol • L-1Na2SO3溶液中加入0.1 mol的CaCl2固体,充分反应后(忽略溶液体积变化),溶液中c(Ca2+)=_________ 。(已知,常温下Ksp(CaSO3)=1.28×l0-9)
(5)用含等物质的量溶质的下列溶液分别吸收SO2,理论吸收量最多的是__________ (填序号)。
A.Na2SO3B.Fe(NO3)3C.Ba(OH)2D.酸性 KMnO4
(1)已知25℃时:O2(g)+S(s)=SO2(g)△H=-akJ·mol-1
O2(g) +2SO2(g)⇌2SO3(g) △H = -b kJ·mol-1
写出SO3(g)分解生成O2(g)与S(s)的热化学方程式:
(2)研究SO2催化氧化生成SO3的反应,回答下列相关问题:
①甲图是SO2(g)和SO3(g)的浓度随时间的变化情况。反应从开始到平衡时,用O2表示的平均反应速率为
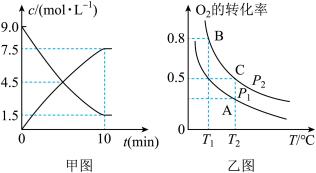
②在一容积可变的密闭容器中充入20 mol SO2(g)和10mol O2(g),O2的平衡转化率随温度(T)、压强(P)的变化如图乙所示。则P1与P2的大小关系是P1
(3)常温下,H2SO3的电离平衡常数Ka1=1.54×10-2,Ka2=1.02×10-7。
①将SO2通入水中反应生成H2SO3。试计算常温下H2SO3⇌2H++SO32-的平衡常数K =
②浓度均为0. 1 mol • L-1的Na2SO3、NaHSO3混合溶液中,
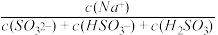 =
=(4)往1 L0.2 mol • L-1Na2SO3溶液中加入0.1 mol的CaCl2固体,充分反应后(忽略溶液体积变化),溶液中c(Ca2+)=
(5)用含等物质的量溶质的下列溶液分别吸收SO2,理论吸收量最多的是
A.Na2SO3B.Fe(NO3)3C.Ba(OH)2D.酸性 KMnO4
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】(І)下表是25℃时某些弱酸的电离平衡常数。
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为___ 。
(2)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是(填“>”、“<”或“=”):CH3COOK___ NaClO,两溶液中:[c(Na+)-c(ClO-)]___ [c(K+)-c(CH3COO-)]。
(3)向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=___ 。
(4)碳酸钠溶液中滴加少量氯水的离子方程式为___ 。
(Ⅱ)H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

(1)写出阳极的电极反应式___ 。
(2)分析产品室可得到H3PO2的原因___ 。
| 化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
| Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
(2)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是(填“>”、“<”或“=”):CH3COOK
(3)向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=
(4)碳酸钠溶液中滴加少量氯水的离子方程式为
(Ⅱ)H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

(1)写出阳极的电极反应式
(2)分析产品室可得到H3PO2的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.葡萄酒中SO2最大使用量为0.25g·L-1,取300.00mL葡萄酒,通过适当的方法使所含SO2全部逸出并用H2O2将其全部氧化为H2SO4,然后用0.0900mol·L-1NaOH标准溶液进行滴定。
①滴定前排气泡时,应选择下图中的___________ (填序号)。

②若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积___________ (填序号)。
A.=10mL B.=40mL C.<10mL D.>40mL
Ⅱ.研究电解质在水溶液中的平衡能了解它的存在形式。
常温下,向100mL0.01mol•L-1HA的溶液中逐滴加入0.02mol•L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。
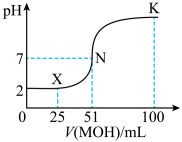
①常温下,0.01mol•L-1HA溶液中由水电离出的c(H+)=___________ mol•L-1
②X点时,溶液中各离子浓度由大到小的顺序是___________ 。
③K点时,溶液中c(H+)+c(M+)–c(OH-)=___________ mol•L-1
①滴定前排气泡时,应选择下图中的

②若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
A.=10mL B.=40mL C.<10mL D.>40mL
Ⅱ.研究电解质在水溶液中的平衡能了解它的存在形式。
常温下,向100mL0.01mol•L-1HA的溶液中逐滴加入0.02mol•L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。

①常温下,0.01mol•L-1HA溶液中由水电离出的c(H+)=
②X点时,溶液中各离子浓度由大到小的顺序是
③K点时,溶液中c(H+)+c(M+)–c(OH-)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】SO2的含量是空气质量日报中一项重要检测指标,也是最近雾霾天气肆虐我国大部分地区的主要原因之一。加大SO2的处理力度,是治理环境污染的当务之急。
I.电化学法处理SO2。
硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如右图所示(电极均为惰性材料):

(1)M极发生的电极反应式为________________ 。
(2)若使该装置的电流强度达到2.0A,理论上每分钟应向负极通入标准状况下气体的体积为________ L(已知:1个e-所带电量为1.6×10-19C)。
Ⅱ.溶液与电化学综合(钠碱循环法)处理SO2。
(3)钠碱循环法中,用Na2SO3溶液作为吸收液来吸收SO2,该反应的离子方程式为______________ 。
(4)吸收液吸收SO2的过程中,pH随n(SO32-)/n(HSO3-)变化关系如右图所示:

①用图中数据和变化规律说明NaHSO3溶液呈酸性的原因________________ 。
②n(SO32-)/n(HSO3-)=1:1时,溶液中离子浓度由大到小的顺序是_____________ 。
(5)当吸收液的pH降至约为6时,需送至电解槽处理,直至得到pH>8的吸收液再循环利用,其电解示意图如下:

①写出阳极发生的电极反应式________________ ;
②当电极上有2 mol电子转移时阴极产物的质量为______________ 。
I.电化学法处理SO2。
硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如右图所示(电极均为惰性材料):

(1)M极发生的电极反应式为
(2)若使该装置的电流强度达到2.0A,理论上每分钟应向负极通入标准状况下气体的体积为
Ⅱ.溶液与电化学综合(钠碱循环法)处理SO2。
(3)钠碱循环法中,用Na2SO3溶液作为吸收液来吸收SO2,该反应的离子方程式为
(4)吸收液吸收SO2的过程中,pH随n(SO32-)/n(HSO3-)变化关系如右图所示:

①用图中数据和变化规律说明NaHSO3溶液呈酸性的原因
②n(SO32-)/n(HSO3-)=1:1时,溶液中离子浓度由大到小的顺序是
(5)当吸收液的pH降至约为6时,需送至电解槽处理,直至得到pH>8的吸收液再循环利用,其电解示意图如下:

①写出阳极发生的电极反应式
②当电极上有2 mol电子转移时阴极产物的质量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】高炉炼铁的基本反应之一如下: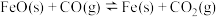 ,1100℃时,某密闭容器中发生该反应。
,1100℃时,某密闭容器中发生该反应。
(1)能说明该反应已达平衡状态的是___________
(2)若平衡后,保持温度不变,加入FeO后, 将
将___________ (填“增大”、“减小”或“不变”)。1100℃时,K=0.263,测得高炉中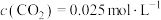 、
、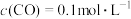 ,判断该反应是否处于平衡状态
,判断该反应是否处于平衡状态___________ (填“是”、“否”),此时,化学反应速率是
___________ 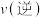 (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。
(3)反应的平衡常数K与温度T(单位:K)之间的关系如图所示。
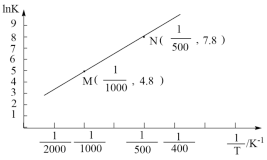
温度升高,化学平衡移动后达到新的平衡,高炉内 和CO的体积比
和CO的体积比___________ (填“增大”、“减小”或“不变”),K___________ (填“增大”、“减小”或“不变”)。指出两条提高CO的平衡转化率的措施___________ 。
(4)某实验小组在实验室模拟上述反应。一定温度下,在2L盛有FeO粉末的恒容密闭容器中通入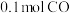 ,5min时生成
,5min时生成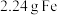 。0~5min内用CO的浓度变化表示的平均反应速率是
。0~5min内用CO的浓度变化表示的平均反应速率是___________ 。若将此时反应体系中的混合气体通入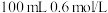 的NaOH溶液中,所得溶液中离子浓度由大到小的顺序是
的NaOH溶液中,所得溶液中离子浓度由大到小的顺序是___________ 。
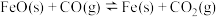 ,1100℃时,某密闭容器中发生该反应。
,1100℃时,某密闭容器中发生该反应。(1)能说明该反应已达平衡状态的是___________
| A.容器内固体质量保持不变 | B.容器中气体压强保持不变 |
C.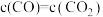 | D.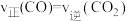 |
 将
将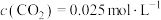 、
、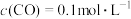 ,判断该反应是否处于平衡状态
,判断该反应是否处于平衡状态
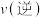 (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。(3)反应的平衡常数K与温度T(单位:K)之间的关系如图所示。

温度升高,化学平衡移动后达到新的平衡,高炉内
 和CO的体积比
和CO的体积比(4)某实验小组在实验室模拟上述反应。一定温度下,在2L盛有FeO粉末的恒容密闭容器中通入
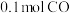 ,5min时生成
,5min时生成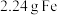 。0~5min内用CO的浓度变化表示的平均反应速率是
。0~5min内用CO的浓度变化表示的平均反应速率是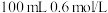 的NaOH溶液中,所得溶液中离子浓度由大到小的顺序是
的NaOH溶液中,所得溶液中离子浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】请根据要求回答下列问题。
(1)1 mol·L-1 Na2CO3溶液的pH_______ (填“>”“<”或“=”, 下同)0.1 mol·L-1Na2CO3溶液的pH;1 mol·L-1 Na2CO3溶液的水解程度_______ 0. 1 mol·L-1Na2CO3溶液的水解程度。
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则pH=9的NaOH溶液与pH=4的H2SO4溶液的体积之比为_______ 。
(3)X、Y、Z、 W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种。下表是常温下浓度均为0.01mol/L的X、Y、Z、W溶液的pH。将X、Y、Z各1 mol同时溶于水中得到混合溶液,则混合溶液中各离子的浓度由大到小的顺序为_______ 。
(1)1 mol·L-1 Na2CO3溶液的pH
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则pH=9的NaOH溶液与pH=4的H2SO4溶液的体积之比为
(3)X、Y、Z、 W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种。下表是常温下浓度均为0.01mol/L的X、Y、Z、W溶液的pH。将X、Y、Z各1 mol同时溶于水中得到混合溶液,则混合溶液中各离子的浓度由大到小的顺序为
| 0.01mol/L的溶液 | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
您最近一年使用:0次



