常温下,用pH=m的盐酸滴定20mLpH=n的MOH溶液,且m+n=14,混合溶液的pH与盐酸体积(V)的关系如图所示。下列说法正确的是

| A.Kb(MOH)的数量级为10-11 |
| B.由c点可算得m=14/3 |
| C.b点溶液呈中性,此时c(Cl-)=c(M+) |
| D.a点:c(Cl-)>c(M+)>c(OH-)>c(H+) |
更新时间:2018-05-10 16:38:57
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
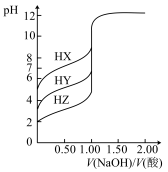
【推荐1】常温下,用 的NaOH溶液分别滴定浓度均为
的NaOH溶液分别滴定浓度均为 的三种一元酸HX、HY、HZ,滴定曲线如图所示。下列说法中正确的是
的三种一元酸HX、HY、HZ,滴定曲线如图所示。下列说法中正确的是
 的NaOH溶液分别滴定浓度均为
的NaOH溶液分别滴定浓度均为 的三种一元酸HX、HY、HZ,滴定曲线如图所示。下列说法中正确的是
的三种一元酸HX、HY、HZ,滴定曲线如图所示。下列说法中正确的是
| A.相同条件下,电离平衡常数越大的酸,滴定突变越不明显 |
B.常温下, 的HZ溶液 的HZ溶液 |
C. 时, 时,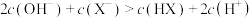 |
| D.滴定HY时,选用甲基橙作指示剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】实验室测定反应 的平衡常数K的过程为:
的平衡常数K的过程为:
①一定温度下,将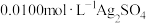 溶液与
溶液与 溶液
溶液 等体积混合,产生灰黑色沉淀;
等体积混合,产生灰黑色沉淀;
②待步骤①中反应达到平衡时,取v mL上层清液,用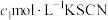 标准溶液滴定
标准溶液滴定 ,至出现稳定的浅红色时消耗KSCN标准溶液
,至出现稳定的浅红色时消耗KSCN标准溶液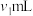 。
。
资料: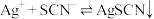 (白色)
(白色) 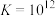 ,
,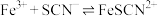 (红色)
(红色) 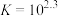
下列说法正确的是
 的平衡常数K的过程为:
的平衡常数K的过程为:①一定温度下,将
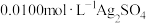 溶液与
溶液与 溶液
溶液 等体积混合,产生灰黑色沉淀;
等体积混合,产生灰黑色沉淀;②待步骤①中反应达到平衡时,取v mL上层清液,用
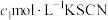 标准溶液滴定
标准溶液滴定 ,至出现稳定的浅红色时消耗KSCN标准溶液
,至出现稳定的浅红色时消耗KSCN标准溶液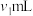 。
。资料:
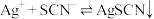 (白色)
(白色) 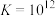 ,
,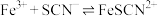 (红色)
(红色) 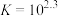
下列说法正确的是
A. 溶液可替换为 溶液可替换为 溶液 溶液 |
| B.过程①中产生的灰黑色沉淀为Fe或Ag元素的氧化物 |
C.可用KCl标准溶液代替KSCN的标准溶液滴定 |
D.步骤②中不待溶液澄清,直接用浊液做滴定实验测定 ,则所测K值偏小 ,则所测K值偏小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】我国硒含量居世界首位,H2SeO3为二元弱酸溶液,25°C时,用0.1mol·L-1 NaOH溶液滴定20mL 0.1mol·L-1 H2SeO3溶液的滴定曲线如图所示(已知:25°C时,pKa=-lgKa,H2SeO3的pKa1=1.34,pKa2=7.34)

下列说法正确的是

下列说法正确的是
| A.a点对应消耗NaOH溶液的体积为10mL |
B.b点溶液中:c(H2SeO3)>c(SeO ) ) |
C.c点溶液中:c(Na+)+c(H+)=3c(HSeO )+c(OH-) )+c(OH-) |
| D.水的电离程度:a>b>c>d |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下,向20mL0.lmol•L-1(CH3)2NH•H2O(一水合二甲胺)溶液中滴加0.1mol•L-1盐酸,滴定曲线如图甲所示,含C微粒的物质的量分数σ随pH变化如图乙所示。下列说法错误的是( )
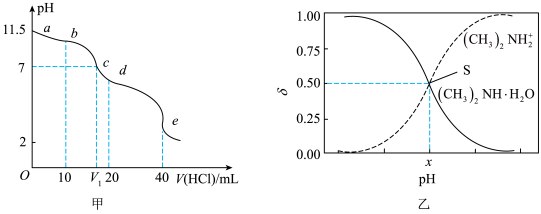

| A.e点时,溶液中c(Cl-)=2c[(CH3)2NH•H2O]+2c[(CH3)2NH2+] |
| B.S点对应溶液的pH约为11.5 |
| C.常温下(CH3)2NH•H2O的电离常数为1×10-4 |
| D.d点时,溶液中c(H+)=c(OH-)+c[(CH3)2NH•H2O] |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】常温下,向1 L 0.05 mol/L  溶液(不考虑空气的影响)中缓慢通入0.05 mol
溶液(不考虑空气的影响)中缓慢通入0.05 mol ,充分混合,完全,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入
,充分混合,完全,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入 的物质的量之间的变化曲线如图所示。已知:常温下,
的物质的量之间的变化曲线如图所示。已知:常温下, ,
, 。下列说法错误的是
。下列说法错误的是
 溶液(不考虑空气的影响)中缓慢通入0.05 mol
溶液(不考虑空气的影响)中缓慢通入0.05 mol ,充分混合,完全,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入
,充分混合,完全,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入 的物质的量之间的变化曲线如图所示。已知:常温下,
的物质的量之间的变化曲线如图所示。已知:常温下, ,
, 。下列说法错误的是
。下列说法错误的是
| A.a点溶液pH约为10 |
| B.水的电离程度:b>d |
C.c点溶液中,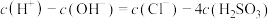 |
D.若将 换成 换成 ,其他不变,当通入0.05 mol ,其他不变,当通入0.05 mol  时,溶液中的浓度大小有: 时,溶液中的浓度大小有: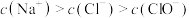 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,用 NaOH溶液滴定NH4HSO4溶液 ,混合溶液的相对导电能力变化曲线如图所示,已知: Kb(NH3• H2O) =10-5,下列叙述正确的是


A.X→Y 过程中发生反应的离子方程式为: +OH-= NH3• H2O +OH-= NH3• H2O |
B.Y点满足:c( ) +c(Na+) =2c( ) +c(Na+) =2c( ) ) |
| C.水的电离程度:X>Y>Z |
| D.若Z点溶液pH=1l,则此时溶液中氨水浓度约为0.1 mol•L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,电解质溶液中的下列关系式不正确的是
A.已知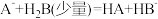 ,则结合H+的能力:HB-<A-<B2- ,则结合H+的能力:HB-<A-<B2- |
| B.在0.1mol·L-1的氨水中滴加0.1mol·L-1盐酸,恰好完全中和时溶液的pH=7 |
C.将c mol·L-1的醋酸溶液与0.02 mol·L-1NaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示CH3COOH的电离常数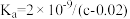 |
D.测得0.1 mol·L-1NaHSO3溶液的pH约为3.5,说明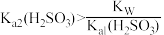 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】25℃下部分弱酸的电离常数如表。下列有关说法不正确的是
| 弱酸 | HCOOH | HClO | H2S |
| 电离平衡常数(Ka) | Ka=1.0×10-4 | Ka=2.0×10-8 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| A.若 HCOONa和 HCOOH的混合溶液的pH=3,则c( HCOOH)/c(HCOO-)=10 |
| B.相同pH的 HCOONa和NaClO溶液中离子总浓度前者大 |
| C.等浓度等体积的Na2S和 HCOOH混合后:c(Na+)=2c(HCOO-)+2c( HCOOH) |
D.向NaClO溶液中通入H2S发生的反应为ClO-+H2S HS-+HClO HS-+HClO |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】室温下,等物质的量的 与强碱
与强碱 混合,得到
混合,得到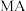 悬浊液,静置,取上层清液,通入
悬浊液,静置,取上层清液,通入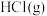 ,混合溶液中
,混合溶液中 与
与 的关系如图。已知:
的关系如图。已知: 、
、 。下列说法错误的是
。下列说法错误的是

 与强碱
与强碱 混合,得到
混合,得到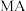 悬浊液,静置,取上层清液,通入
悬浊液,静置,取上层清液,通入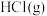 ,混合溶液中
,混合溶液中 与
与 的关系如图。已知:
的关系如图。已知: 、
、 。下列说法错误的是
。下列说法错误的是
A. 时, 时, |
B.a→b的溶液中 将逐渐增大 将逐渐增大 |
C.上层清液中 |
D. 时, 时, |
您最近一年使用:0次



