已知: Kb(NH3·H2O)=1.76×10-5。25℃时,分别向浓度均为0.1mol/L,体积均为20mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的c水(H+)与加入氨水的体积变化关系如图所示。下列说法正确的是
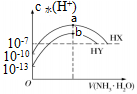

| A.HX的电离方程式为HX==H++X- |
| B.b 点时溶液中c(NH4+)=c(Y-)>c(H+)=c(OH-) |
| C.其中一种酸的电离度为0.1% |
| D.a点溶液呈中性 |
更新时间:2018-05-04 21:17:21
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】25℃时,重水(D2O)的离子积为 1.6×10ˉ15,也可用与 pH 一样的定义来规定其酸碱度:pD=-lgc(D+),下列叙述正确的是(均为 25℃条件下)
| A.重水和水两种液体,D2O 的电离度大于 H2O |
| B.在 100mL0.25mol·Lˉ1DCl 重水溶液中,加入 50mL0.2mol·Lˉ1NaOD 重水溶液,反应后溶液的 pD=1 |
| C.0.01 mol·Lˉ1NaOD 重水溶液,其 pD=12 |
| D.NH4Cl 溶于 D2O 中生成的一水合氨和水合氢离子的化学式为 NH3·D2O 和 HD2O+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】设NA为阿伏加德罗常数的值,下列说法正确的
| A.一定量的Na2O2溶于足量水,生成1.6gO2时转移电子的数目为0.2NA |
| B.在1.8gH2O与2.24LO2中含有的分子数相同,均为0.1NA |
| C.在1mol由C2H4和C3H6的混合物中,含C-H键的数目一定为5NA |
| D.在常温下,1LpH=10的Na2CO3溶液中含H+的数目一定为10-10NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】 时,向
时,向 二元弱酸(简写成
二元弱酸(简写成 )溶液中加入
)溶液中加入 固体或通入
固体或通入 气体,调节溶液
气体,调节溶液 ,混合溶液的
,混合溶液的 与
与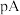 或
或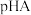 或
或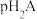 的关系如图所示(忽略溶液体积变化和
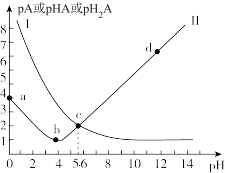
的关系如图所示(忽略溶液体积变化和 的挥发)。下列有关叙述错误的是(已知:
的挥发)。下列有关叙述错误的是(已知: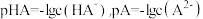 )
)
 时,向
时,向 二元弱酸(简写成
二元弱酸(简写成 )溶液中加入
)溶液中加入 固体或通入
固体或通入 气体,调节溶液
气体,调节溶液 ,混合溶液的
,混合溶液的 与
与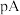 或
或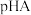 或
或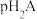 的关系如图所示(忽略溶液体积变化和
的关系如图所示(忽略溶液体积变化和 的挥发)。下列有关叙述错误的是(已知:
的挥发)。下列有关叙述错误的是(已知: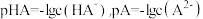 )
)
A.曲线Ⅰ、Ⅱ分别代表的微粒为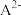 和 和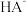 |
B.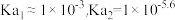 |
| C.从a点到c点,水的电离程度先增大后减小 |
D.b点有关微粒浓度大小关系为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】25 °C时,Ka(HClO)=4.0×10-8。下 列说法正确的是
| A.25°C时,往pH=3的HClO溶液中加少量NaClO固体,HClO的电离程度和水电离出的c(H+ )均减小 |
| B.将浓度均为0.1mol·L-1的NaClO和NaOH溶液加热,两种溶液的pH均变大 |
| C.相同温度下,等pH的HCOONa和NaClO溶液中存在:c(HCOO- )>c(ClO- ) |
| D.25 °C时,pH=7的NaClO和HClO混合溶液中存在:c(HClO)<c(ClO- )=c(Na+ ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】根据下表数据(数据均为常温下所测数据),判断下列叙述正确的是( )


| A.在等浓度的NaClO、 NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) |
| B.在等浓度的NaClO、NaHCO3混合溶液中:c(OH-)>c(HClO)>c(H2CO3) |
| C.少量CO2通入NaClO溶液中反应的离子方程式为:CO2+H2O+2ClO—=CO32—+2HClO |
| D.等温等浓度的NaClO溶液和NaHCO3溶液,前者导电能力强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】t℃时,将0.200mol·L-1的某一元酸HA与0.200mol·L-1的NaOH溶液等体积混合,充分反应后所得溶液中部分离子浓度如下表。下列说法中正确的是
| 微粒 | H+ | Na+ | A- |
| 浓度(mol/L)-1 | 2.50×10-10 | 0.100 | 9.92×10-2 |
| A.所得溶液中:c(Na+)>c(A-)>c(HA)>c(OH-) |
| B.t℃时,水的离子积Kw=1.0×10-13 |
| C.t℃时,一元酸HA的电离常数K=3.10×10-7 |
| D.t℃时,0.100mol·L-1NaA溶液中A-的水解率为0.80% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,以酚酞为指示剂,用0.1000mol·L−1的NaOH溶液滴定20.00mL0.1000mol·L−1的二元酸H2A溶液。溶液中pH、含A微粒分布系数δ(物质的量分数)随滴加NaOH溶液体积VNaOH的变化关系如图所示

| A.H2A在水中电离的方程式为:H2A⇌H++HA-,HA-⇌H++A2- |
| B.当VNaOH溶液=20.00mL时,溶液中离子浓度大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| C.常温下,HA-的电离平衡常数数量级为10-5 |
| D.当VNaOH溶液=30.00mL时,c(HA-)+c(H+)=c(A2-)+c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,已知Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11。某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述正确的是
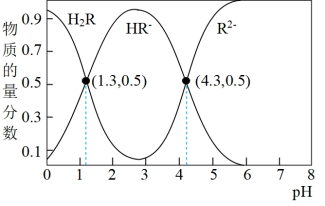

A.反应H2R+R2- 2HR-的平衡常数K=1000 2HR-的平衡常数K=1000 |
B.向Na2CO3溶液中加入少量H2R溶液,发生的反应是:CO +H2R=CO2↑+H2O+R2- +H2R=CO2↑+H2O+R2- |
| C.等体积、等浓度的NaOH溶液与H2R溶液混合后,溶液中:(R2-)<c(H2R) |
| D.在pH=4的溶液中:3c(R2-)>c(Na+)+c(H+)-c(OH-) |
您最近一年使用:0次

 时,下图表示起始浓度为
时,下图表示起始浓度为 的
的 溶液中各含碳粒子物质的量分数与
溶液中各含碳粒子物质的量分数与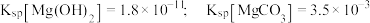 。下列说法错误的是
。下列说法错误的是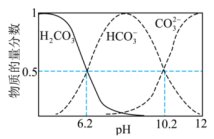
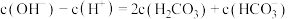
 时,溶液中
时,溶液中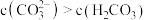
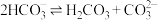 的平衡常数
的平衡常数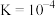
 时,向溶液中加入足量
时,向溶液中加入足量 溶液,溶液中会产生两种沉淀
溶液,溶液中会产生两种沉淀

