已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol/L的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
| A.当加入氨水的体积为10 mL时,c(NH4+)=c(CH3COO-) |
| B.c(NH4+)/c(NH3·H2O)先增大再减小 |
| C.水的电离程度始终增大 |
| D.c(CH3COOH)与c(CH3COO-)之和始终保持不变 |
更新时间:2019-02-20 13:20:42
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】已知水的电离方程式:H2O⇌ H++OH-。下列叙述中,正确的是
| A.升高温度,KW增大,pH不变 |
| B.向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低 |
| C.向水中加入少量硫酸氢钠固体,平衡向逆反应方向移动,c(H+)增大,KW不变 |
| D.向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,水的电离达到平衡:H2O ⇌H++OH-。下列叙述正确的是
| A.向水中加入少量金属 Na,平衡正向移动,c(OH-)增大 |
| B.向水中加入少量 CH3COOH,平衡逆向移动,KW 变小 |
| C.向水中加入少量 NaHSO4 或 NaHCO3 固体,平衡均正向移动,水的电离程度增大 |
| D.向水中加入少量 CH3COONH4 固体,溶液呈中性,水的电离平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法正确的是
A.常温下,将1mLpH=1的H2SO4溶液加水稀释到100mL,稀释后的溶液中 =109 =109 |
| B.常温下,pH=13的Ba(OH)2溶液aL与pH=3的H2SO4溶液bL混合后溶液呈中性(混合后溶液体积变化忽略不计),则a∶b=1∶100 |
C.常温下,设pH=5的H2SO4溶液中由水电离出的H+浓度为c1,pH=5的Al2(SO4)3溶液中由水电离出的H+浓度为c2,则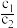 =10-5 =10-5 |
| D.某温度时,测得0.01mol·L-1的NaOH溶液的pH为11,则该温度低于25℃ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列推断或表述正确的是 ( )
| A.分别将体积各为1L的1mol/L NaCI溶液和1mol/L的NaF溶液加水稀释至100L,两溶液离子总数相等 |
| B.将pH =a的醋酸溶液稀释100倍,稀释液pH=b,则b=a+2 |
| C.0.2mol/L的盐酸与0.05mol/L的Ba( OH)2溶液等体积混合,混合液pH =1 |
| D.向1L,0.3mol/L的NaOH溶液缓缓通入CO2气体,至溶液质量增加8.8g,则溶液中:2c(Na+)==3[c(HCO3-)+c(CO32-)+c(H2CO3)] |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
A.常温下,pH=4的 溶液中,由水电离的 溶液中,由水电离的 |
B.将pH=2的HCl溶液和pH=4的 溶液等体积混合,所得溶液pH=3 溶液等体积混合,所得溶液pH=3 |
C.0.1mol/L氨水和0.1mol/L  溶液等体积混合后所得溶液pH>7,则 溶液等体积混合后所得溶液pH>7,则 |
D.室温下,用pH试纸测定某 溶液的pH约为6,则 溶液的pH约为6,则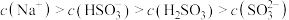 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/c(HCO )的值保持增大
)的值保持增大
②浓度为0.1mol/L的Na2CO3溶液:c(Na+)=c(CO )+c(HCO
)+c(HCO )+c(H2CO3)
)+c(H2CO3)
③在0.1mol/L氨水中滴加0.1mol/L盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=10-amol/L
④向0.1mol/L (NH4)2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO )、c(NH
)、c(NH )均增大
)均增大
⑤在Na2S稀溶液中,c(OH-)=c(H+)+2c(H2S)+c(HS-)
①NaHCO3溶液加水稀释,c(Na+)/c(HCO
 )的值保持增大
)的值保持增大②浓度为0.1mol/L的Na2CO3溶液:c(Na+)=c(CO
 )+c(HCO
)+c(HCO )+c(H2CO3)
)+c(H2CO3)③在0.1mol/L氨水中滴加0.1mol/L盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=10-amol/L
④向0.1mol/L (NH4)2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO
 )、c(NH
)、c(NH )均增大
)均增大⑤在Na2S稀溶液中,c(OH-)=c(H+)+2c(H2S)+c(HS-)
| A.①④ | B.②④ | C.①③ | D.②⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】NA为阿伏加德罗常数的值,下列说法正确的是
A.4.4g C2H4O中含有 键的数目为0.6NA 键的数目为0.6NA |
| B.3molNO2与H2O完全反应时转移电子的数目为4NA |
| C.常温下,1LpH=6.5的H2O2溶液中由水电离产生H+的数目为10-7.5NA |
D.常温下,1L0.1mol/LK2Cr2O7溶液中 的数目为0.1NA 的数目为0.1NA |
您最近一年使用:0次


 的
的 溶液或醋酸中,由水电离出的
溶液或醋酸中,由水电离出的 均为
均为
 的醋酸和
的醋酸和 的NaOH溶液等体积混合后,
的NaOH溶液等体积混合后,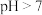
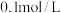
 溶液和
溶液和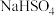 溶液等体积混合,溶液中
溶液等体积混合,溶液中


