砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________ 。
(2)根据元素周期律,原子半径Ga_____________ As,第一电离能Ga____________ As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________ ,其中As的杂化轨道类型为_________ 。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是__________ 。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________ ,Ga与As以________ 键键合。Ga和As的摩尔质量分别为MGag·mol-1和MAs g·mol-1,原子半径分别为rGapm和rAspm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________ 。

(1)写出基态As原子的核外电子排布式
(2)根据元素周期律,原子半径Ga
(3)AsCl3分子的立体构型为
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为

2016·全国·高考真题 查看更多[21]
湖南省郴州市永兴县第一中学2021-2022学年高三下学期期中考试化学试题广西河池市高级中学2021-2022学年高三上学期第三次月考化学试题福建省永安市第三中学2021届高三9月月考化学试题广西壮族自治区田阳高中2019-2020学年高二下学期6月月考理科综合化学试题湖北省武汉市华中师范大学第一附属中学2020届高三2月份网络教学质量监测理综化学试题2020届高中化学第一轮复习第十二章《物质结构与性质》测试卷2016年全国普通高等学校招生统一考试化学(全国3卷参考版)【全国百强校】江西省南昌市第十中学2019届高三上学期期末考试理科综合化学试题【全国百强校】四川省棠湖中学2019届高三上学期第三次月考理综-化学试题吉林省实验中学2018届高三上学期第五次月考(一模)理科综合化学试题【全国校级联考】四川省眉山一中办学共同体2019届高三9月月考化学试题【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高二下学期期中考试化学试题吉林省实验中学2018高三一模理综化学试题贵州省遵义航天高级中学2018届高三第二次模拟(10月)理科综合化学试题河南省南阳市第一中学2018届高三实验班第一次考试化学试题2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷2016年全国普通高等学校招生统一考试化学(新课标3卷精编版)四川省绵阳中学实验学校2017届高三5月模拟理综化学试题新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题四川省眉山中学2016-2017学年高二下学期期中考试理综化学试题
更新时间:2016-12-09 15:43:51
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
请回答下列问题:
(1)写出下列元素符号:A______ , B_______ ,C________ ,D__________ 。
(2)写出C元素在周期表的位置_________ ,E2+价电子的轨道表示式______________ ,B元素能量最高的电子为____ 轨道上的电子,其轨道呈______ 形。
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物中σ键有______ 个,π键有______ 个。(阿伏伽德罗常数的值用NA表示)
(4)B、C、D的简单离子的半径由大到小的顺序为________ (用离子符号表示)。
(5)写出C的核外有18个电子的氢化物的电子式_____________ 。
| 元素 | 相关信息 |
| A | 基态原子的价电子排布式为nSnnPn |
| B | 元素原子的核外p电子数比s电子数少1个 |
| C | 最外层电子数是电子层数的3倍 |
| D | 简单离子是第三周期元素中离子半径最小的 |
| E | 价电子层中的未成对电子数为4 |
(1)写出下列元素符号:A
(2)写出C元素在周期表的位置
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物中σ键有
(4)B、C、D的简单离子的半径由大到小的顺序为
(5)写出C的核外有18个电子的氢化物的电子式
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铜被称为细菌病毒的“杀手”,研究表明新冠病毒在铜表面存活时间仅为4小时。回答下列问题:
(1)铜元素在周期表中的位置___________ ,基态铜离子核外能量最高的电子所处电子层符号为___________ 。
(2)铜能与类卤素 反应生成
反应生成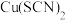 ,
,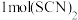 分子含有
分子含有 键的数目为
键的数目为___________ ;写出一种与 互为等电子体的分子的电子式为
互为等电子体的分子的电子式为___________ 。
(3)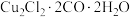 是一种配合物,其结构如图所示:
是一种配合物,其结构如图所示:
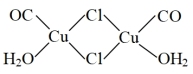
①该配合物中亚铜离子的配位数为___________ 。
②该配合物中, 作配体时配位原子是C而不是O的原因是
作配体时配位原子是C而不是O的原因是___________ 。
(4) 晶胞中
晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,其侧视图如图2新示(阿伏加德罗常数的值为
所构成的四面体中心,其侧视图如图2新示(阿伏加德罗常数的值为 )。
)。
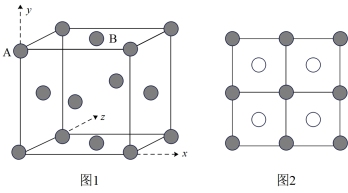
 的配位数为
的配位数为___________ ,若 晶胞的密度为
晶胞的密度为 ,则
,则 和
和 之间的最短距离为
之间的最短距离为___________  。
。
(1)铜元素在周期表中的位置
(2)铜能与类卤素
 反应生成
反应生成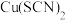 ,
,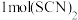 分子含有
分子含有 键的数目为
键的数目为 互为等电子体的分子的电子式为
互为等电子体的分子的电子式为(3)
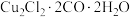 是一种配合物,其结构如图所示:
是一种配合物,其结构如图所示:
①该配合物中亚铜离子的配位数为
②该配合物中,
 作配体时配位原子是C而不是O的原因是
作配体时配位原子是C而不是O的原因是(4)
 晶胞中
晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,其侧视图如图2新示(阿伏加德罗常数的值为
所构成的四面体中心,其侧视图如图2新示(阿伏加德罗常数的值为 )。
)。
 的配位数为
的配位数为 晶胞的密度为
晶胞的密度为 ,则
,则 和
和 之间的最短距离为
之间的最短距离为 。
。
您最近半年使用:0次
【推荐3】Ⅰ.变化观和平衡观视角认识物质
(1)工业上在Cu-ZnO催化下利用CO2发生如下反应Ⅰ生产甲醇,同时伴有反应Ⅱ发生。
Ⅰ.

Ⅱ.

①已知:298K时,相关物质的相对能量如图1,反应Ⅰ的 为
为_________ 。
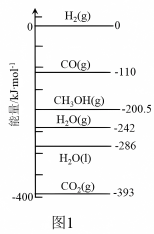
②不同条件下,按照n(CO2):n(H2)=1:3投料,CO2的平衡转化率如图2所示。压强p1、p2、p3由大到小的顺序是___________ 。压强为p1时,温度高于300℃之后,随着温度升高CO2平衡转化率增大的原因 ___________ 。

(2)能说明反应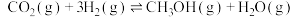 ,已达平衡状态的是 ___________
,已达平衡状态的是 ___________ 填字母
填字母 。
。
Ⅱ.从微粒结构视角认识物质
(3)基态Fe2+的核外电子排布式为_______ ;第四周期元素中,基态原子未成对电子数与Co相等的有 ___________  填元素符号
填元素符号 。
。
(4)利用配合物的特征颜色可检验补铁药片中的Fe3+和Fe2+,部分配合物的结构如下:

①取等量碾碎的药片放入两支试管中,试管1加盐酸溶解,试管2加等体积蒸馏水溶解。分别滴加KSCN溶液,发现试管1溶液变红,试管2溶液不变色。依据图示信息,解释SCN-检验Fe3+须在酸性条件下进行的原因_______ 。
②邻二氮菲中N原子的价层孤电子对占据_______ 。 填标号
填标号 。
。
A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
(1)工业上在Cu-ZnO催化下利用CO2发生如下反应Ⅰ生产甲醇,同时伴有反应Ⅱ发生。
Ⅰ.


Ⅱ.


①已知:298K时,相关物质的相对能量如图1,反应Ⅰ的
 为
为
②不同条件下,按照n(CO2):n(H2)=1:3投料,CO2的平衡转化率如图2所示。压强p1、p2、p3由大到小的顺序是

(2)能说明反应
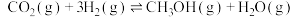 ,已达平衡状态的是 ___________
,已达平衡状态的是 ___________ 填字母
填字母 。
。A.单位时间内生成1mol  的同时消耗了1mol 的同时消耗了1mol  |
| B.在恒温恒容的容器中,混合气体的密度保持不变 |
| C.在绝热恒容的容器中,反应的平衡常数不再变化 |
| D.在恒温恒压的容器中,气体的平均摩尔质量不再变化 |
Ⅱ.从微粒结构视角认识物质
(3)基态Fe2+的核外电子排布式为
 填元素符号
填元素符号 。
。(4)利用配合物的特征颜色可检验补铁药片中的Fe3+和Fe2+,部分配合物的结构如下:

①取等量碾碎的药片放入两支试管中,试管1加盐酸溶解,试管2加等体积蒸馏水溶解。分别滴加KSCN溶液,发现试管1溶液变红,试管2溶液不变色。依据图示信息,解释SCN-检验Fe3+须在酸性条件下进行的原因
②邻二氮菲中N原子的价层孤电子对占据
 填标号
填标号 。
。A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】含 、
、 元素的物质在生产生活中有重要的用途。回答下列问题:
元素的物质在生产生活中有重要的用途。回答下列问题:
(1)基态 核外电子排布式为
核外电子排布式为________ 。
(2) 分子的立体构型为
分子的立体构型为________ 。
(3)某个 (Ⅱ)有机配合物的结构如图所示:
(Ⅱ)有机配合物的结构如图所示:

①该分子中N原子的杂化方式为________ 、________ 。
②请在图中用“ ”标出
”标出 的配位键
的配位键______ 。
(4)Ge,As,Se元素处于同一周期,三种元素原子的第一电离能由大到小的顺序为________ 。
(5) 的酸性强于
的酸性强于 的原因是
的原因是________ , 的键角小于
的键角小于 的原因是
的原因是________ 。
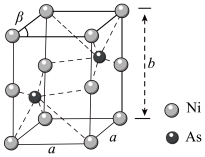
(6)如图为Ni和As形成的某种晶体的六方晶胞图,该化合物的化学式为________ ,Ni原子占据的空隙类型为________ 。已知晶胞参数分别为apm、apm、bpm和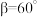 ,则该晶胞的密度为
,则该晶胞的密度为________  (设阿伏加 德罗常数的值为NA)
(设阿伏加 德罗常数的值为NA)
 、
、 元素的物质在生产生活中有重要的用途。回答下列问题:
元素的物质在生产生活中有重要的用途。回答下列问题:(1)基态
 核外电子排布式为
核外电子排布式为(2)
 分子的立体构型为
分子的立体构型为(3)某个
 (Ⅱ)有机配合物的结构如图所示:
(Ⅱ)有机配合物的结构如图所示:
①该分子中N原子的杂化方式为
②请在图中用“
 ”标出
”标出 的配位键
的配位键(4)Ge,As,Se元素处于同一周期,三种元素原子的第一电离能由大到小的顺序为
(5)
 的酸性强于
的酸性强于 的原因是
的原因是 的键角小于
的键角小于 的原因是
的原因是(6)如图为Ni和As形成的某种晶体的六方晶胞图,该化合物的化学式为
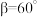 ,则该晶胞的密度为
,则该晶胞的密度为 (设阿伏加 德罗常数的值为NA)
(设阿伏加 德罗常数的值为NA)
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的核外电子排布为该同学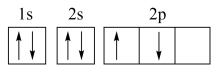 所画的电子排布图违背了
所画的电子排布图违背了___________ 。
(2)B元素的电负性____________ (填“大于”“小于”或“等于”)C元素的电负性。
(3)D元素第二次电离能飞跃数据将发生在失去第____________ 个电子时。
(4)E基态原子中能量最高的电子,其电子云在空间有____________ 个伸展方向。
(5)基态F2+和F3+中未成对电子数之比为___________ 。
(6)和元素F为同一周期的第VIIB元素G能形成G2+,气态G2+再失去1个电子比气态F2+再失去1个电子难,对此你的解释是___________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素基态原子p轨道有两个未成对电子 |
| D原子的第一至第四电离能分别是:I1=738kJ·mol-1;I2=1451kJ·mol-1;I3=7733kJ·mol-1;I4=10540kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F基态原子中未成对电子数和该元素所在的周期数相等 |
 所画的电子排布图违背了
所画的电子排布图违背了(2)B元素的电负性_
(3)D元素第二次电离能飞跃数据将发生在失去第_
(4)E基态原子中能量最高的电子,其电子云在空间有_
(5)基态F2+和F3+中未成对电子数之比为
(6)和元素F为同一周期的第VIIB元素G能形成G2+,气态G2+再失去1个电子比气态F2+再失去1个电子难,对此你的解释是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、V、M、W为五种短周期元素,其中X是短周期元素中金属性最强的元素;Y与X同周期,是同周期简单离子中半径最小的;Z原子基态时2p原子轨道上有3个未成对的电子;V原子的核外电子排布式为1s22s22p63s2;M处于第三周期,其单质为淡黄色固体;W的一种同位素原子无中子。回答下列问题:
(1)M与W形成的分子是___ (填“极性分子”或“非极性分子”);与该分子互为等电子体的一种阴离子为(写化学式)___ 。
(2)元素X、Y、V第一电离能由小到大的顺序是___ (用元素符号表示)。
(3)ZW3气体易溶于水的原因是___ 。(写两点)
(4)M8是___ 晶体,该晶体中微粒间的作用力为___ ;
(5)X的最高价氧化物的水化物和Y的最高价氧化物相互反应的离子方程式___ 。
(1)M与W形成的分子是
(2)元素X、Y、V第一电离能由小到大的顺序是
(3)ZW3气体易溶于水的原因是
(4)M8是
(5)X的最高价氧化物的水化物和Y的最高价氧化物相互反应的离子方程式
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铬、镍等过渡元素的单质、化合物在工业上有广泛的应用。
(1)基态镍原子核外共有______ 种不同的能量的电子,3d能级上的未成对电子数为______ 。
(2)Cu和Cr位于同一周期。
①向CuSO4溶液中逐滴加入氨水,可得深蓝色晶体[Cu(NH3)4]SO4·H2O,其中心离子是______ (填元素符号),配体是______ ,SO 的几何构型为
的几何构型为______ 。
②Cr元素所在周期中金属原子第一电离能最大的是______ (填元素符号,下同)。
③Cr元素所在周期中原子电负性最大的是______ (不考虑零族元素)。
(3)过渡金属单质及其化合物是有机合成反应的重要催化剂。
例如: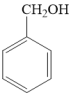

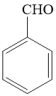 。
。
①苯甲醇分子中的碳原子的杂化类型分别是______ 、______ 。
②苯甲醇、苯甲醛的沸点依次为206℃、179℃,造成二者沸点差异的主要原因是______ 。
(1)基态镍原子核外共有
(2)Cu和Cr位于同一周期。
①向CuSO4溶液中逐滴加入氨水,可得深蓝色晶体[Cu(NH3)4]SO4·H2O,其中心离子是
 的几何构型为
的几何构型为②Cr元素所在周期中金属原子第一电离能最大的是
③Cr元素所在周期中原子电负性最大的是
(3)过渡金属单质及其化合物是有机合成反应的重要催化剂。
例如:


 。
。①苯甲醇分子中的碳原子的杂化类型分别是
②苯甲醇、苯甲醛的沸点依次为206℃、179℃,造成二者沸点差异的主要原因是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】黑火药是我国古代的四大发明之一。黑火药爆炸时发生的反应为:2KNO3+S+3C=K2S+N2↑+3CO2↑。回答下列问题:
(1)基态钾原子的核外电子排布式为____________ ,第一电离能:K______ (填“>”或“<”)Na。
(2)NO3-的空间构型为_____________ 。
(3)固态硫易溶于CS2,熔点为112℃,沸点为444.8℃。其分子结构为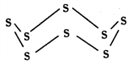 ,S8中硫原子的杂化轨道类型是
,S8中硫原子的杂化轨道类型是____________ ,S8分子中至多有________ 个硫原子处于同一平面。
(4)N2分子中σ键与π键的个数比为________ ,N2的沸点比CO的沸点____ (填“高”或“低”)。
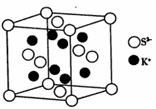
(5)K2S的晶胞结构如图所示。其中K+的配位数为_______ ,S2-的配位数为____ ;若晶胞中距离最近的两个S2-核间距为a cm,则K2S晶体的密度为____ g·cm-3(列出计算式,不必计算出结果)。
(1)基态钾原子的核外电子排布式为
(2)NO3-的空间构型为
(3)固态硫易溶于CS2,熔点为112℃,沸点为444.8℃。其分子结构为
 ,S8中硫原子的杂化轨道类型是
,S8中硫原子的杂化轨道类型是(4)N2分子中σ键与π键的个数比为
(5)K2S的晶胞结构如图所示。其中K+的配位数为

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】短周期元素D、E、X、Y、Z原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为________ ;Z的核外电子排布式是________ ;
(2)D的最高价氧化物与E的一种氧化物为等电子体,写出E的氧化物的化学式________ ;
(3)D和Y形成的化合物,其分子的空间构型为________ ;D原子的轨道杂化方式是________ ;
(4)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是________ 。
(1)Y的最高价氧化物的化学式为
(2)D的最高价氧化物与E的一种氧化物为等电子体,写出E的氧化物的化学式
(3)D和Y形成的化合物,其分子的空间构型为
(4)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氢、碳、氮、氧、铁、铜等元素及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
(1)写出基态铜原子的价电子排布式___ 。
(2)实验室用KSCN溶液、检验Fe3+。C、N、O的电负性由大到小的顺序为___ (用元素符号表示),一定条件下,SCN-与MnO2反应可得到(SCN)2,试写出(SCN)2的结构式___ 。
(3)FeCl3的熔点为306℃,沸点为315℃FeCl3的晶体类型是__ 。FeSO4常作补铁剂,SO42-的立体构型是__ 。
(4)CH3OH分子中O原子的杂化方式为___ ,键角:H-C-H___ H-O-C。(填“<”、“>”、“=”)CH3OH能与H2O以任意比互溶的原因是___ 。
(5)已知C60分子结构和C60晶胞示意图(如图I、图Ⅱ所示):
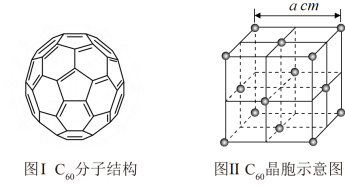
则一个C60分子中含有σ键的个数为__ ,与每个C60分子距离最近且相等的C60分子有__ 个,C60晶体的密度的表达式为__ g·cm-3。
(1)写出基态铜原子的价电子排布式
(2)实验室用KSCN溶液、检验Fe3+。C、N、O的电负性由大到小的顺序为
(3)FeCl3的熔点为306℃,沸点为315℃FeCl3的晶体类型是
(4)CH3OH分子中O原子的杂化方式为
(5)已知C60分子结构和C60晶胞示意图(如图I、图Ⅱ所示):

则一个C60分子中含有σ键的个数为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
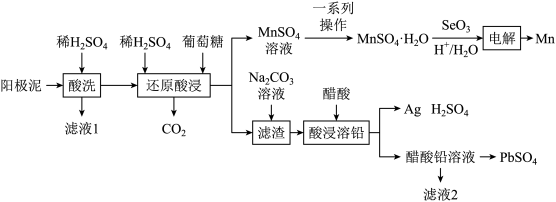
【推荐2】一种回收锌电解阳极泥(主要成分为 、
、 和ZnO,还有少量锰铅氧化物
和ZnO,还有少量锰铅氧化物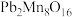 和Ag)中金属元素锌、锰、铅和银的工艺如图所示。回答下列问题:
和Ag)中金属元素锌、锰、铅和银的工艺如图所示。回答下列问题:
已知: 易溶于水,不溶于乙醇。
易溶于水,不溶于乙醇。
(1)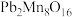 中Pb的化合价为+2价,Mn的化合价有+2价和+4价,则氧化物中+2价和+4价Mn的个数比为
中Pb的化合价为+2价,Mn的化合价有+2价和+4价,则氧化物中+2价和+4价Mn的个数比为___________ 。
(2)“还原酸浸”过程中主要反应的化学方程式为___________ 。
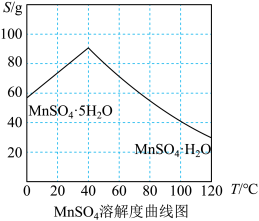
(3)结合 溶解度曲线图分析,由
溶解度曲线图分析,由 溶液制得
溶液制得 晶体的“一系列操作”是
晶体的“一系列操作”是___________ 、___________ ,用___________ (填物质的名称)洗涤、干燥。
(4)“电解”时,加入 与水反应生成二元弱酸
与水反应生成二元弱酸 ,在阴极放电生成Se单质,有利于
,在阴极放电生成Se单质,有利于 电还原沉积。则
电还原沉积。则 放电的电极反应式为
放电的电极反应式为___________ 。
(5)通过计算说明可用 溶液将“滤渣”中的
溶液将“滤渣”中的 转化为
转化为 的原因
的原因___________ 。[已知:25℃时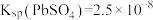 ,
,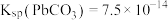 ]
]
(6)关于流程中有关物质的说法正确的是___________(填标号)。
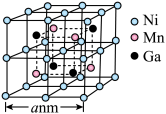
(7)锰、镍、镓的某种磁性形状记忆型合金的晶胞结构如图所示。 表示阿伏加德罗常数的值。该晶体的密度为
表示阿伏加德罗常数的值。该晶体的密度为___________  (列出计算式即可)。
(列出计算式即可)。
 、
、 和ZnO,还有少量锰铅氧化物
和ZnO,还有少量锰铅氧化物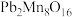 和Ag)中金属元素锌、锰、铅和银的工艺如图所示。回答下列问题:
和Ag)中金属元素锌、锰、铅和银的工艺如图所示。回答下列问题:
已知:
 易溶于水,不溶于乙醇。
易溶于水,不溶于乙醇。(1)
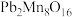 中Pb的化合价为+2价,Mn的化合价有+2价和+4价,则氧化物中+2价和+4价Mn的个数比为
中Pb的化合价为+2价,Mn的化合价有+2价和+4价,则氧化物中+2价和+4价Mn的个数比为(2)“还原酸浸”过程中主要反应的化学方程式为
(3)结合
 溶解度曲线图分析,由
溶解度曲线图分析,由 溶液制得
溶液制得 晶体的“一系列操作”是
晶体的“一系列操作”是
(4)“电解”时,加入
 与水反应生成二元弱酸
与水反应生成二元弱酸 ,在阴极放电生成Se单质,有利于
,在阴极放电生成Se单质,有利于 电还原沉积。则
电还原沉积。则 放电的电极反应式为
放电的电极反应式为(5)通过计算说明可用
 溶液将“滤渣”中的
溶液将“滤渣”中的 转化为
转化为 的原因
的原因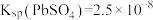 ,
,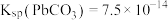 ]
](6)关于流程中有关物质的说法正确的是___________(填标号)。
| A.葡萄糖溶于水,葡萄糖分子能与水分子形成氢键4dS{s |
B.Ag和Cu是同族元素且相邻,Ag的价电子轨道表示式为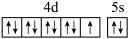 |
C. 与 与 均属于分子晶体, 均属于分子晶体, 为非极性分子,其空间构型为直线形 为非极性分子,其空间构型为直线形 |
| D.流程中的“滤液2”可循环利用 |
 表示阿伏加德罗常数的值。该晶体的密度为
表示阿伏加德罗常数的值。该晶体的密度为 (列出计算式即可)。
(列出计算式即可)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】C、N化合物对人类生存环境有重要影响。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为_________ 。
(2)C、N、O三种元素的第一电离能由小到大的顺序为_________ 。
(3)键角:NH3__________ (填“>“<”或“=”)H2O;NH3的VSEPR模型为_________ 。
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为_________ 。
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为_________ (填元素符号),原因是_________ 。
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。_________ 。
②2号原子的坐标为_________ 。
③该晶体的密度为__________ g/cm3。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为
(2)C、N、O三种元素的第一电离能由小到大的顺序为
(3)键角:NH3
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。
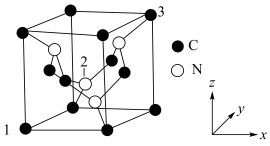
②2号原子的坐标为
③该晶体的密度为
您最近半年使用:0次



