滴定分数是指滴定过程中标准溶液与待测溶液中溶质的物质的量之比。用0.10 mol·L-1 NaOH溶液滴定0.10 mol·L1 H2C2O4(草酸)溶液的滴定曲线如图所示。下列说法不正确的是
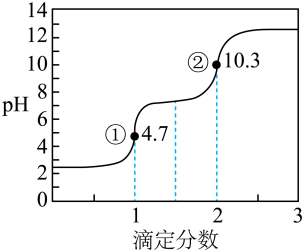

| A.H2C2O4属于二元弱酸 |
| B.若用NaOH标准溶液滴定NaHC2O4溶液,可用酚酞作指示剂 |
| C.图中①处:c(H2C2O4)+c(H+)=c(OH-) |
| D.图中②处:c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+) |
更新时间:2019-06-10 16:18:27
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列图示与对应的叙述相符的是
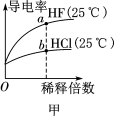


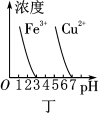




| A.由图甲可知,a点Kw的数值比b点Kw的数值大 |
| B.图乙表示在相同的密闭容器中,不同温度下的反应,该反应的ΔH>0 |
| C.图丙表示0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 等浓度醋酸溶液的滴定曲线 |
| D.根据图丁,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列图示与对应的叙述相符的是
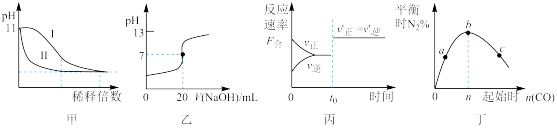

| A.图甲表示常温下稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水 |
| B.图乙表示常温下,0.1000mol∙L-1NaOH 溶液滴定20.00mL0.1000mol∙L-1醋酸溶液的滴定曲线 |
C.图丙表示某可逆反应的反应速率随时间的变化,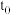 时刻改变的条件一定是使用了催化剂 时刻改变的条件一定是使用了催化剂 |
D.图丁表示反应4CO(g)+2NO2(g) N2(g)+4CO2(g),在其他条件不变的情况下改变起始CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c>b>a N2(g)+4CO2(g),在其他条件不变的情况下改变起始CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c>b>a |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某兴趣小组依据以下方案将KI、Na2S2O3和淀粉溶液混合后,再加入K2S2O8溶液,探究反应条件对反应速率的影响。已知:S2O +2I-=I2+2SO
+2I-=I2+2SO (慢),2S2O
(慢),2S2O +I2=2I-+2SO
+I2=2I-+2SO (快)。下列说法不正确的是
(快)。下列说法不正确的是
 +2I-=I2+2SO
+2I-=I2+2SO (慢),2S2O
(慢),2S2O +I2=2I-+2SO
+I2=2I-+2SO (快)。下列说法不正确的是
(快)。下列说法不正确的是| 实验序号 | 体积/mL | |||
| K2S2O8溶液 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| 1 | 10.0 | 4.0 | 4.0 | 2.0 |
| 2 | 8.0 | 4.0 | 4.0 | 2.0 |
| A.将KI、Na2S2O3和淀粉溶液混合后,加入K2S2O8溶液,溶液不会立即变蓝 |
| B.当溶液中的Na2S2O3完全耗尽,溶液将由无色变为蓝色 |
| C.依据上述方案,通过颜色变化出现的快慢,可以说明反应物浓度对速率的影响 |
| D.为了确保能观察到颜色变化,Na2S2O3和K2S2O8初始物质的量之比应小于2 |
您最近一年使用:0次
【推荐1】某温度下,向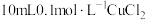 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
溶液,滴加过程中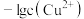 与
与 溶液体积的关系如图所示。
溶液体积的关系如图所示。

已知: 。下列有关说法正确的是
。下列有关说法正确的是
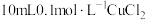 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
溶液,滴加过程中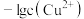 与
与 溶液体积的关系如图所示。
溶液体积的关系如图所示。
已知:
 。下列有关说法正确的是
。下列有关说法正确的是A. 溶液中: 溶液中: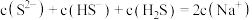 |
B.向 溶液中滴加 溶液中滴加 的 的 溶液,图中的b点向下平移 溶液,图中的b点向下平移 |
C.该温度下, |
| D.b、c点对应的溶液中,水的电离程度更大的为b点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温时,改变饱和氯水的pH,得到部分含氯微粒的物质的量分数与pH的关系如图所示。下列叙述不正确的是( )


A.该温度下, 的电离常数 的电离常数 的对值 的对值 |
B.氯水中的 、 、 、HClO均能与KI发生反应 、HClO均能与KI发生反应 |
C. 的氯水中, 的氯水中, |
D.已知常温下反应 的 的 ,当pH增大时,K减小 ,当pH增大时,K减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用中和滴定法可以测定精制磷酸中H3PO4的质量分数:25℃下,取ag精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用b mol∙L−1NaOH溶液滴定,溶液的pH与NaOH溶液体积的关系如图所示:

下列说法错误的是

下列说法错误的是
A.从m点到n点反应的离子方程式为H2PO +OH-=HPO +OH-=HPO +H2O +H2O |
| B.m、n两点溶液中由水电离的H+浓度均大于1.0×10−7 mol∙L−1 |
C.m、n两点之间的某一点会存在关系:2c(Na+)=3[c(H2PO )+c(HPO )+c(HPO )+c(PO )+c(PO )+c(H3PO4)] )+c(H3PO4)] |
D.精制磷酸中H3PO4的质量分数是 % % |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】25℃时CH3COOH的 、HF的
、HF的 ,下列说法正确的是
,下列说法正确的是
 、HF的
、HF的 ,下列说法正确的是
,下列说法正确的是A.分别测定某HF溶液、醋酸溶液的pH,前者小于后者,可以证明HF的 |
B.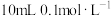 的HF溶液中加入 的HF溶液中加入 的NaOH溶液,溶液中水的电离程度与纯水相同,V(NaOH)可能小于或大于10mL 的NaOH溶液,溶液中水的电离程度与纯水相同,V(NaOH)可能小于或大于10mL |
C.向 的HF溶液中加入 的HF溶液中加入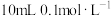 的NaOH溶液充分反应,所得溶液中 的NaOH溶液充分反应,所得溶液中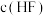  |
D.将 的HF溶液与 的HF溶液与 的醋酸混合,HF的电离度增大 的醋酸混合,HF的电离度增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,某二元弱碱M(OH)2的水溶液中含有M(OH)2、M(OH)+、M2+,它们的分布系数δ随溶液pH的变化曲线如图所示。Kb2为M(OH)2的第二步电离平衡常数,下列说法错误的是


| A.Kb2=1×10-5.5 |
| B.曲线Ⅱ代表的微粒为M(OH)+ |
| C.m、n、p三点对应的水溶液中,m点水的电离程度最大 |
| D.0.1 mol/LM(OH)Cl溶液中c(Cl-)>c([M(OH)2]>c(M2+)>c(OH-)>c(H+) |
您最近一年使用:0次

 和
和 ,原理如下图所示。已知:25℃时,
,原理如下图所示。已知:25℃时, 的
的 ,
, 的
的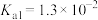 ,
, ,下列说法正确的是
,下列说法正确的是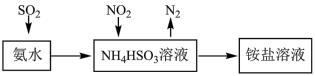
 :
: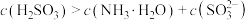


 ;
;



