接触法制硫酸工艺中,其主反应如下:
2SO2(g) + O2(g) 2SO3(g)
2SO3(g)  H=-197 kJ/mol
H=-197 kJ/mol
下列说法正确的是
2SO2(g) + O2(g)
 2SO3(g)
2SO3(g)  H=-197 kJ/mol
H=-197 kJ/mol下列说法正确的是
| A.因为反应放热,所以该反应不需要加热即能快速反应 |
| B.增大O2的浓度可以提高反应速率和SO2的转化率 |
| C.反应450℃时的平衡常数小于500℃时的平衡常数 |
| D.恒温下缩小容器容积,使Q > K |
18-19高二下·北京海淀·期中 查看更多[8]
更新时间:2019-06-13 08:50:30
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列有关平衡常数的说法正确的是( )
| A.改变条件,反应物的转化率增大,平衡常数也一定增大 |
B. 的平衡常数表达式为 的平衡常数表达式为 |
| C.对于给定的可逆反应,温度一定时,其正、逆反应的平衡常数相等 |
D. 的平衡常数表达式为 的平衡常数表达式为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知下列反应:O2(g)+C(s) CO2(g) K1;2C(s)+O2(g)
CO2(g) K1;2C(s)+O2(g) 2CO(g) K2; 则反应2CO(g)+O2(g)
2CO(g) K2; 则反应2CO(g)+O2(g) 2CO2(g)的平衡常数为
2CO2(g)的平衡常数为
 CO2(g) K1;2C(s)+O2(g)
CO2(g) K1;2C(s)+O2(g) 2CO(g) K2; 则反应2CO(g)+O2(g)
2CO(g) K2; 则反应2CO(g)+O2(g) 2CO2(g)的平衡常数为
2CO2(g)的平衡常数为A.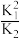 | B.2K1-K2 | C.K12×K2 | D.2K1+K2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】氯化亚铜,化学式CuCl或Cu2Cl2。为白色立方结晶或白色粉末,微溶于水,溶于浓盐酸生成氯化亚铜酸(HCuCl2强酸),溶于氨水生成氯化二氨合亚铜,不溶于乙醇。
实验室制备氯化亚铜∶
方法1∶CuCl2溶于浓盐酸,加入铜屑并加热,生成HCuCl2溶液,加水稀释可得CuCl沉淀;
方法2∶向含有铜丝、氯化铵、盐酸的溶液中加入硝酸作催化剂,通入氧气并加热,将反应得到的NH4[CuCl2]用大量的水稀释可得CuCl沉淀。
工业制法∶向CuSO4和NaCl的混合溶液中加入Fe粉或通入SO2,充分反应后再用大量的水稀释,过滤、酒精洗涤、真空干燥。
下列说法不正确的是
实验室制备氯化亚铜∶
方法1∶CuCl2溶于浓盐酸,加入铜屑并加热,生成HCuCl2溶液,加水稀释可得CuCl沉淀;
方法2∶向含有铜丝、氯化铵、盐酸的溶液中加入硝酸作催化剂,通入氧气并加热,将反应得到的NH4[CuCl2]用大量的水稀释可得CuCl沉淀。
工业制法∶向CuSO4和NaCl的混合溶液中加入Fe粉或通入SO2,充分反应后再用大量的水稀释,过滤、酒精洗涤、真空干燥。
下列说法不正确的是
| A.方法2中生成NH4[CuCl2],1mol[CuCl2]-含σ键数2mol |
| B.方法2中制备1molCuCl,参加反应氧气的体积为5.6L |
C.[CuCl2]-(aq) CuCl(s)+Cl-(aq),加水稀释,有利于CuCl沉淀生成 CuCl(s)+Cl-(aq),加水稀释,有利于CuCl沉淀生成 |
| D.用酒精洗涤CuCl沉淀,真空干燥可有效防止CuCl被空气中氧气氧化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】汽车尾气中NO产生的反应为
 。一定条件下,等物质的量
。一定条件下,等物质的量 和
和 在恒容密闭容器中反应,曲线a表示该反应在温度T下
在恒容密闭容器中反应,曲线a表示该反应在温度T下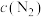 随时间(t)的变化,曲线b表示该反应在某一起始条件改变时
随时间(t)的变化,曲线b表示该反应在某一起始条件改变时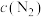 随时间(t)的变化。下列叙述不正确的是
随时间(t)的变化。下列叙述不正确的是


 。一定条件下,等物质的量
。一定条件下,等物质的量 和
和 在恒容密闭容器中反应,曲线a表示该反应在温度T下
在恒容密闭容器中反应,曲线a表示该反应在温度T下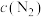 随时间(t)的变化,曲线b表示该反应在某一起始条件改变时
随时间(t)的变化,曲线b表示该反应在某一起始条件改变时 随时间(t)的变化。下列叙述不正确的是
随时间(t)的变化。下列叙述不正确的是
A.温度T下、0-40s内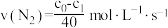 |
B.M点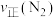 小于N点 小于N点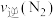 |
| C.曲线b对应的条件改变可能是充入氧气 |
D.若曲线b对应的条件改变是升高温度,则 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列事实中,能用勒夏特列原理解释的是
| A.H2(g)、I2(g)、HI(g)平衡混合气加压后颜色变深 |
| B.使用催化剂可加快SO2转化为SO3的速率 |
| C.500℃左右比室温更有利于氨的合成 |
| D.工业合成氨时,采用迅速冷却的方法,将气态氨变为液氨后及时从混合物中分离出去,以提高NH3的产量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】丁烷催化脱氢制备丁烯的主反应为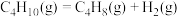
 ,副反应为
,副反应为 裂解生成
裂解生成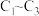 (表示碳原子数为1~3的烷烃或烯烃)。将
(表示碳原子数为1~3的烷烃或烯烃)。将 与
与 的混合气体以定流速通过填充有催化剂的反应器,
的混合气体以定流速通过填充有催化剂的反应器, 的产率、
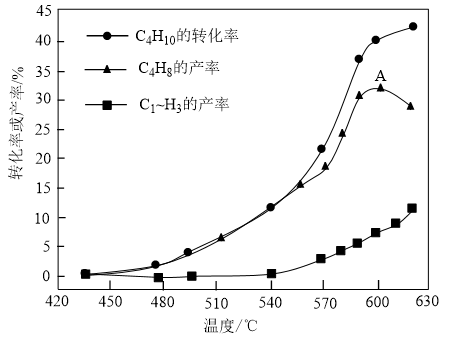
的产率、 的转化率与温度的关系如图所示。下列说法不正确的是
的转化率与温度的关系如图所示。下列说法不正确的是
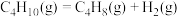
 ,副反应为
,副反应为 裂解生成
裂解生成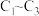 (表示碳原子数为1~3的烷烃或烯烃)。将
(表示碳原子数为1~3的烷烃或烯烃)。将 与
与 的混合气体以定流速通过填充有催化剂的反应器,
的混合气体以定流速通过填充有催化剂的反应器, 的产率、
的产率、 的转化率与温度的关系如图所示。下列说法不正确的是
的转化率与温度的关系如图所示。下列说法不正确的是
A.435℃时 产率低的原因可能是此温度下催化剂活性较低,反应速率较慢 产率低的原因可能是此温度下催化剂活性较低,反应速率较慢 |
B.600℃以后, 的产率下降原因可能是 的产率下降原因可能是 发生裂解反应生成 发生裂解反应生成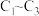 |
C.图中表示 产率的曲线中,A点时主反应不一定达到平衡状态 产率的曲线中,A点时主反应不一定达到平衡状态 |
| D.提高丁烷脱氢制备丁烯转化率的研究方向为寻找低温时具有较高活性的催化剂 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】在某催化剂作用下,乙炔选择性加成反应C2H2(g)+H2(g)⇌C2H4(g) ΔH<0。速率方程为v正=k正c(C2H2)c(H2),v逆=k逆c(C2H4)(k正、k逆为速率常数,只与温度、催化剂有关)。一定温度下,在2L恒容密闭容器中充入1molC2H2(g)和1molH2(g),只发生上述反应。测得C2H4的物质的量如下表所示:
下列说法错误的是
| t/min | 0 | 5 | 10 | 15 | 20 |
| n/mol | 0 | 0.3 | 0.5 | 0.6 | 0.6 |
| A.0~10min内,v(H2)=0.025mol・L-1・min-1 |
| B.升高温度,k正增大的倍数小于k逆增大的倍数 |
| C.净反应速率(v正-v逆)由大到小最终等于0 |
| D.在上述条件下,15min时2k逆=15k正 |
您最近一年使用:0次
【推荐1】化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是
| 选项 | 操作或做法 | 目的 |
| A | 向酒精溶液中加入生石灰,过滤 | 制备无水乙醇 |
| B | 将盐酸与NaHCO3混合后产生的气体直接通入苯酚钠溶液 | 验证酸性:碳酸>苯酚 |
| C | 向NaOH溶液中滴加几滴BaCl2溶液 | 验证NaOH溶液是否变质 |
| D | 缩小H2(g)+Br2 (g) 2HBr(g)的平衡体系的容器容积 2HBr(g)的平衡体系的容器容积 | 探究压强对平衡移动的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知:由CO2制备甲烷的反应为CO2(g)+4H2(g) CH4(g)+2H2O(g)△H<0。一定温度下,在一容积恒定的密闭容器中充入1mol CO2(g)和4molH2(g)发生上述反应,反应达到平衡后,若要同时增大正反应速率和H2平衡转化率,下列措施合理的是
CH4(g)+2H2O(g)△H<0。一定温度下,在一容积恒定的密闭容器中充入1mol CO2(g)和4molH2(g)发生上述反应,反应达到平衡后,若要同时增大正反应速率和H2平衡转化率,下列措施合理的是
 CH4(g)+2H2O(g)△H<0。一定温度下,在一容积恒定的密闭容器中充入1mol CO2(g)和4molH2(g)发生上述反应,反应达到平衡后,若要同时增大正反应速率和H2平衡转化率,下列措施合理的是
CH4(g)+2H2O(g)△H<0。一定温度下,在一容积恒定的密闭容器中充入1mol CO2(g)和4molH2(g)发生上述反应,反应达到平衡后,若要同时增大正反应速率和H2平衡转化率,下列措施合理的是| A.通入一定量的氦气,增大压强 |
| B.将产物分离出来 |
| C.再充入1molCO2(g)和4molH2(g) |
| D.适当降低温度 |
您最近一年使用:0次

 ,已知
,已知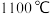 时
时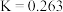 。下列说法错误的是
。下列说法错误的是
 ,反应速率会变大
,反应速率会变大 ,此时v正大于v逆
,此时v正大于v逆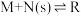 达到平衡后,无论加压或降温,M的转化率都增大,则下列结论正确的是
达到平衡后,无论加压或降温,M的转化率都增大,则下列结论正确的是

