电解质溶液的电导率越大,导电能力越强。用0.100mol/L的NaOH溶液滴定0.100mol/L浓度均为0.100mol/L的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是( )
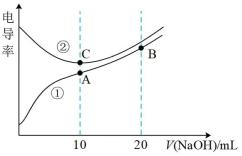

| A.曲线①代表滴定CH3COOH溶液的曲线 |
| B.A、C两点对应溶液均呈中性 |
| C.B点溶液中:c(Na+)>c(OH-)>c(CH3COO-) |
| D.A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.050mol/L |
更新时间:2019-06-21 19:00:15
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】25℃时,将浓度均为0.1mol/L、体积分别为Va和Vb的HX溶液与NH3·H2O溶液按不同体积比混合,保持Va+Vb=100mL (溶液体积有简单叠加),Va、Vb与混合液的pH的关系如图所示。下列说法不正确的是
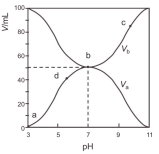

| A.Ka(HX)的值与Kb(NH3·H2O)的值相等 |
B.c、d两点,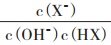 值相等 值相等 |
| C.a→d点过程中,存在c (X-) =c (NH4+) |
| D.b点,c(NH4+)+c (HX) = 0.05mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验方案的设计,不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 测定未知NaOH溶液的浓度 | 向20.00mL待测NaOH溶液中加入甲基橙指示剂,用0.1mol·L-1醋酸标准溶液滴定,记下指示剂变色时耗酸量并计算 |
| B | 验证牺牲阳极的阴极保护法 | 用导线连接Zn和Fe,浸入酸化的NaCl溶液中,用胶头滴管从Fe电极区域取少量溶液于试管,滴入两滴铁氰化钾溶液 |
| C | 验证草酸电离吸热 | 将0.1mol·L-1草酸溶液加热,并用传感器监测pH变化 |
| D | 比较AgCl和AgBr的Ksp大小 | 分别向等体积AgCl和AgBr饱和溶液中加入足量AgNO3溶液,比较产生沉淀的物质的量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
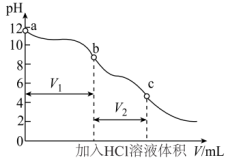
【推荐3】可用酚酞和甲基橙双指示剂法测定部分变质的烧碱中 的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
 的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
| A.指示剂的添加顺序为先加酚酞,后加甲基橙 |
B.b点时溶液中的溶质主要为NaCl和 |
C.若 ,则a点溶液中存在 ,则a点溶液中存在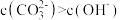 |
D.原固体混合物中碳酸钠的质量分数表示为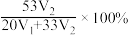 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】缓冲溶液是指pH值在一定的范围内不因稀释或外加少量的酸或碱而发生显著变化的溶液。常温下,已知某浓度相等的 和
和 的缓冲溶液显酸性。下列说法正确的是
的缓冲溶液显酸性。下列说法正确的是
 和
和 的缓冲溶液显酸性。下列说法正确的是
的缓冲溶液显酸性。下列说法正确的是| A.等浓度的盐酸和氯化钠混合溶液也能组成缓冲溶液 |
B.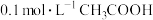 和 和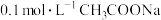 组成的缓冲溶液,比 组成的缓冲溶液,比 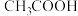 和 和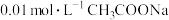 组成的缓冲溶液酸性更强 组成的缓冲溶液酸性更强 |
C.加水稀释该缓冲溶液,由水电离的 减小 减小 |
D.该缓冲溶液中存在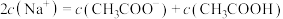 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,向10 mL 0.10mol·L−1YOH溶液中逐渐滴加0.20mol·L−1HX溶液,混合溶液的pH变化如图所示(温度和体积变化忽略不计)。下列结论错误的是
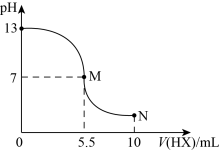

| A.HX为一元弱酸,YOH为一元强碱 |
| B.M点对应溶液中水的电离程度大于N点溶液中水的电离程度 |
| C.室温时,pH=a的YX溶液中水电离出的c(OH−)=l.0×10−(14-a) mol·L−1 |
| D.N点对应溶液中粒子浓度:c(HX)>c(X−)>c(Y+)>c(H+)>c(OH−) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】25 ℃时,在10 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液20 mL,溶液中含碳微粒的物质的量随溶液pH的变化如图所示。下列说法错误的是( )
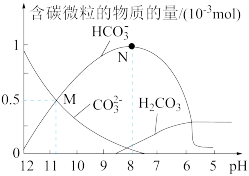

| A.HCl溶液滴加一半时,溶液pH>7 |
| B.H2CO3的Ka1的数量级为10-6 |
| C.pH=8时,溶液中NaHCO3的物质的量浓度为0.1 mol·L-1 |
D.在M点:c(Na+)>c(CO )=c(HCO )=c(HCO )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】设 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.  溶液中含有的 溶液中含有的 数目为 数目为 |
B.标准状况下,22.4L  通入足量水中,所得溶液中 通入足量水中,所得溶液中 、HClO、 、HClO、 的个数和为 的个数和为 |
C.0.1mol  加入沸水中完全反应生成胶体的粒子数为0.1 加入沸水中完全反应生成胶体的粒子数为0.1 |
D.过氧化钠与水反应,生成0.1mol氧气时,转移的电子数为0.2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】按一定的速率用0.10mol·L-1NaOH溶液滴定10.0mL0.10 mol·L-1H2A溶液,溶液pH和温度随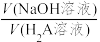 的变化曲线如图所示。下列说法
的变化曲线如图所示。下列说法不正确 的是
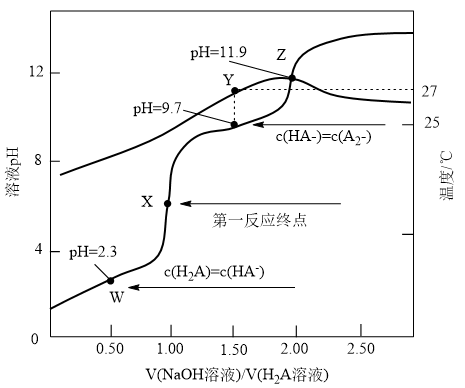
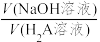 的变化曲线如图所示。下列说法
的变化曲线如图所示。下列说法
| A.从W至Z点,水的电离程度和KW逐渐增大 |
B.当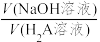 =1时c(Na+)=c(H2A)+c(HA-)+c(A2-) =1时c(Na+)=c(H2A)+c(HA-)+c(A2-) |
C.27℃,H2A的电离常数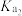 =10-9.7 =10-9.7 |
| D.可用酚酞作为第二反应终点的指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知H2A的电离常数分别用Ka1、Ka2表示,水的离子积常数为KW。25 ℃时,向1 L 0.01 mol·L-1 H2A溶液中滴加NaOH溶液,溶液中c(H2A)、c(HA-)、c(A2-)、c(OH-)、c(H+)的负对数值(-lg c)与pH的关系如图所示。下列说法正确的是
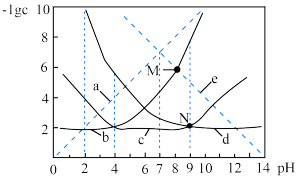

| A.pH=10时,n(HA-)=9.1×10-4 mol |
B.0.01 mol·L-1 NaHA溶液中:c(H+)≈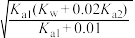 mol·L-1 mol·L-1 |
| C.M点溶液中n(Na+)+n(H+)-n(A2-)=0.02 mol |
| D.随溶液pH增大,c(H2A)·c(A2-)先减小后增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】 时,苯酚
时,苯酚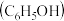 的
的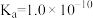 ,下列说法正确的是
,下列说法正确的是
 时,苯酚
时,苯酚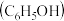 的
的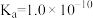 ,下列说法正确的是
,下列说法正确的是A.相同温度下,等 的 的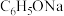 和 和 溶液中, 溶液中, |
B.将浓度均为 的 的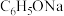 和 和 溶液加热,两种溶液的 溶液加热,两种溶液的 均变大 均变大 |
C. 时, 时, 溶液与 溶液与 溶液混合,测得 溶液混合,测得 ,则此时溶液中 ,则此时溶液中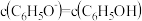 |
D. 时, 时, 的 的 溶液中加少量 溶液中加少量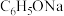 固体,水的电离程度变小 固体,水的电离程度变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验操作、所得现象及结论均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将2mol•L-1KI溶液与1mol•L-1FeCl3溶液等体积混合 | 充分反应后,滴加几滴KSCN溶液,溶液变红 | Fe3+与I-的反应为可逆反应 |
| B | 常温下将Ba(OH)2•8H2O晶体与NH4Cl晶体在烧杯中搅拌混合 | 烧杯壁变凉 | 该反应熵变△S<0 |
| C | 向饱和食盐水中先通入足量CO2,再通入NH3 | 有固体析出 | 可用于侯氏制碱法中NaHCO3的制备 |
| D | 用pH试纸分别测量等物质的量浓度的NH4HCO3溶液和NaClO溶液的pH | NaClO溶液的pH较大 | 电离常数:Ka1(H2CO3)>Ka(HClO) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



