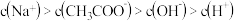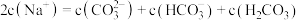关于小苏打水溶液的表述正确的是( )
A.存在的电离平衡为HCO3-+H2O H2CO3+OH- H2CO3+OH- |
| B.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| C.HCO3-的电离程度大于HCO3-的水解程度 |
| D.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
更新时间:2019-07-03 10:38:17
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某小组同学进行了以下3个实验:
下列说法正确的是
| 实验1 | 实验2 | 实验3 | |
| 操作 | 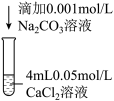 |  | 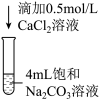 |
| 现象 | 无沉淀及气体产生 | 有沉淀及气体产生 | 现象a |
A.实验1中发生了反应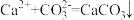 |
B.实验2中 促进了 促进了 的电离平衡 的电离平衡 |
| C.实验3中现象a可能是:有沉淀及气体产生 |
D.推测:可用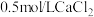 溶液鉴别浓度均为 溶液鉴别浓度均为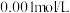 的 的 溶液和 溶液和 溶液 溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关化学用语表达正确的是
| A.铅蓄电池放电时负极反应式:Pb-2e-=Pb2+ |
B.H2CO3的电离方程式:H2CO3 2H++CO 2H++CO |
C.HS-的水解方程式:HS-+H2O H3O++S2- H3O++S2- |
D.AgCl的溶解平衡表达式:AgCl(s)  Ag+(aq)+Cl-(aq) Ag+(aq)+Cl-(aq) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在一定条件下发生下列反应,其中属于盐类水解反应的是
A.NH +2H2O +2H2O  NH3·H2O+H3O+ NH3·H2O+H3O+ |
B.HCO + H2O + H2O  H3O+ + CO H3O+ + CO |
C.NH3 +H2O NH NH +OH- +OH- |
D.Cl2+H2O H++Cl–+HClO H++Cl–+HClO |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式书写正确的是
A.熔融状态下硫酸氢钾的电离方程式: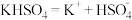 |
B.NaHS水解: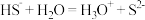 |
C. 溶于氢碘酸: 溶于氢碘酸: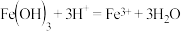 |
D.碳酸电离: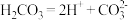 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知25℃时有关弱酸的电离平衡常数见下表:
则下列有关说法正确的是
弱酸化学式 | HA | H2B |
电离平衡常数 (25℃) | Ka=1.7×10-6 | Ka1=1.3×10-3 Ka2=5.6×10-8 |
则下列有关说法正确的是
| A.等物质的量浓度的各溶液pH关系为:pH(Na2B)>pH(NaHB)>pH(NaA) |
| B.将a mol·L-1的HA溶液与a mol·L-1的NaA溶液等体积混合,混合液中:c(Na+)>c(A-) |
| C.向Na2B溶液中加入足量的HA溶液发生反应的离子方程式为:B2+2HA==2A- +H2B |
| D.NaHB溶液中部分微粒浓度的大小为:c(Na+)>c(HB-)>c(B-)>c(H2B) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】分析化学中将“滴定分数”定义为:所加滴定剂与被滴定组分的物质的量之比。甲基橙的变色范围是3.1~4.4。常温下以0.10 mol·L-1的NaOH溶液为滴定剂滴定0.10 mol·L-1一元酸HA溶液,并绘制出如图所示的滴定曲线。下列叙述正确的是
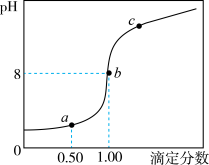

| A.HA的电离方程式为:HA= H++A- |
| B.该酸碱中和滴定过程可选甲基橙作指示剂 |
| C.a点溶液满足:c(HA) + 2c(H+)=c(A-)+ 2c(OH-) |
| D.从a点到c点,溶液中水的电离程度一直增大 |
您最近一年使用:0次



 +H2O
+H2O +D2O⇌NH3·D2O+H+
+D2O⇌NH3·D2O+H+ +H2O⇌H3O++CO
+H2O⇌H3O++CO
 溶液中:
溶液中:
 的下列溶液:①
的下列溶液:①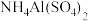 、②
、② 、③
、③ ,其中
,其中 由大到小的顺序是:①>②>③
由大到小的顺序是:①>②>③ 时,将
时,将 的
的 溶液与
溶液与 的
的 溶液等体积混合后:
溶液等体积混合后: