工业上用以下流程从铜沉淀渣中回收铜、硒、碲等物质。沉淀渣中除含有铜 、硒
、硒 、碲
、碲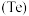 外,还含有少量稀贵金属,主要物质为
外,还含有少量稀贵金属,主要物质为 、
、 和
和 。
。
(1)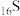 、
、 、
、 为同主族元素,其中
为同主族元素,其中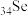 在元素周期表中的位置
在元素周期表中的位置____ 。
其中铜、硒、碲的主要回收流程如图:
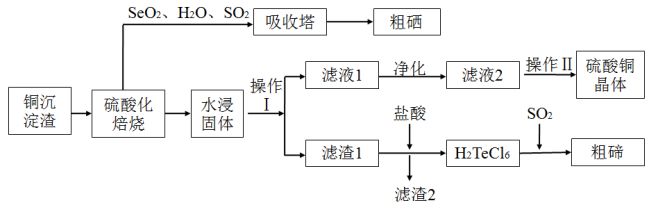
(2)经过硫酸化焙烧 ,铜、硒化铜和碲化铜转变为硫酸铜。
①写出 硫酸化焙烧的化学方程式
硫酸化焙烧的化学方程式____ 。
②“水浸固体”过程中补充少量氯化钠固体,可减少固体中的银(硫酸银)进入浸出液中,结合化学用语,从平衡移动原理角度解释其原因___ 。
③滤液2经过____ 、_____ 、过滤、洗涤、干燥可以得到硫酸铜晶体。
(3)所得粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示。蒸馏操作中控制的最佳温度是____ (填序号)。
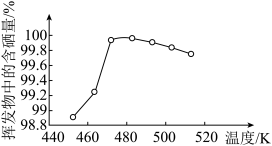
a.455℃ b.462℃ c.475℃ d.515℃
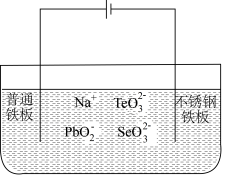
(4)目前碲化镉薄膜太阳能行业发展迅速,被认为是最有发展前景的太阳能技术之一。用如下装置可以完成碲的电解精炼。研究发现在低的电流密度、碱性条件下,随着 浓度的增加,促进了
浓度的增加,促进了 的沉积。写出
的沉积。写出 的沉积的电极反应式为
的沉积的电极反应式为____ 。
 、硒
、硒 、碲
、碲 外,还含有少量稀贵金属,主要物质为
外,还含有少量稀贵金属,主要物质为 、
、 和
和 。
。(1)
 、
、 、
、 为同主族元素,其中
为同主族元素,其中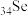 在元素周期表中的位置
在元素周期表中的位置其中铜、硒、碲的主要回收流程如图:

(2)经过
①写出
 硫酸化焙烧的化学方程式
硫酸化焙烧的化学方程式②“水浸固体”过程中补充少量氯化钠固体,可减少固体中的银(硫酸银)进入浸出液中,结合化学用语,从平衡移动原理角度解释其原因
③滤液2经过
(3)所得粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示。蒸馏操作中控制的最佳温度是

a.455℃ b.462℃ c.475℃ d.515℃
(4)目前碲化镉薄膜太阳能行业发展迅速,被认为是最有发展前景的太阳能技术之一。用如下装置可以完成碲的电解精炼。研究发现在低的电流密度、碱性条件下,随着
 浓度的增加,促进了
浓度的增加,促进了 的沉积。写出
的沉积。写出 的沉积的电极反应式为
的沉积的电极反应式为
更新时间:2019-09-27 22:33:47
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某小组利用“氯气氧化法”制备溴酸钠( ),并测定产品纯度。
),并测定产品纯度。
Ⅰ、制备
________________________________________ 。
(2)向装置Ⅲ通 前,先打开电热磁力搅拌器,升温至50~60℃,滴入适量液溴,然后打开
前,先打开电热磁力搅拌器,升温至50~60℃,滴入适量液溴,然后打开 、
、 ,通入
,通入 至pH传感器显示接近中性,关闭
至pH传感器显示接近中性,关闭 、
、 。装置Ⅲ中发生反应的总化学方程式为
。装置Ⅲ中发生反应的总化学方程式为________________ 。反应结束后,为避免Ⅰ中残留的 污染空气,在拆卸装置前应进行的操作是
污染空气,在拆卸装置前应进行的操作是________________________ 。
Ⅱ、 的分离提纯
的分离提纯
(3)溴酸钠和氯化钠的溶解度曲线如图所示。将装置Ⅲ中所得混合液趁热过滤,将滤液________________ 、过滤、洗涤、干燥,得到 粗产品。
粗产品。 产品纯度
产品纯度
步骤1:取 粗产品溶于蒸馏水配制成
粗产品溶于蒸馏水配制成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入适量稀硫酸和过量
溶液于锥形瓶中,加入适量稀硫酸和过量 溶液,再用
溶液,再用
 ,标准溶液滴定,平均消耗
,标准溶液滴定,平均消耗 标准溶液的体积为
标准溶液的体积为 。
。
(已知 、
、 ,杂质不反应)
,杂质不反应)
步骤2:另取 蒸馏水做空白实验,消耗
蒸馏水做空白实验,消耗
 标准溶液。(空白实验的目的是减小滴定过程中空气及溶解氧氧化
标准溶液。(空白实验的目的是减小滴定过程中空气及溶解氧氧化 带来的影响)
带来的影响)
(4)产品纯度为________________________ (用含m,c, ,
, 的代数式表示)。
的代数式表示)。
 ),并测定产品纯度。
),并测定产品纯度。Ⅰ、制备

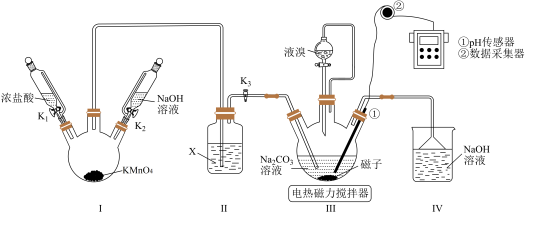
(2)向装置Ⅲ通
 前,先打开电热磁力搅拌器,升温至50~60℃,滴入适量液溴,然后打开
前,先打开电热磁力搅拌器,升温至50~60℃,滴入适量液溴,然后打开 、
、 ,通入
,通入 至pH传感器显示接近中性,关闭
至pH传感器显示接近中性,关闭 、
、 。装置Ⅲ中发生反应的总化学方程式为
。装置Ⅲ中发生反应的总化学方程式为 污染空气,在拆卸装置前应进行的操作是
污染空气,在拆卸装置前应进行的操作是Ⅱ、
 的分离提纯
的分离提纯(3)溴酸钠和氯化钠的溶解度曲线如图所示。将装置Ⅲ中所得混合液趁热过滤,将滤液
 粗产品。
粗产品。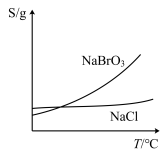
 产品纯度
产品纯度步骤1:取
 粗产品溶于蒸馏水配制成
粗产品溶于蒸馏水配制成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入适量稀硫酸和过量
溶液于锥形瓶中,加入适量稀硫酸和过量 溶液,再用
溶液,再用
 ,标准溶液滴定,平均消耗
,标准溶液滴定,平均消耗 标准溶液的体积为
标准溶液的体积为 。
。(已知
 、
、 ,杂质不反应)
,杂质不反应)步骤2:另取
 蒸馏水做空白实验,消耗
蒸馏水做空白实验,消耗
 标准溶液。(空白实验的目的是减小滴定过程中空气及溶解氧氧化
标准溶液。(空白实验的目的是减小滴定过程中空气及溶解氧氧化 带来的影响)
带来的影响)(4)产品纯度为
 ,
, 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】利用某化上污泥(主要成分为Cu2Te、Cr2O3以及少量的Au)资源化利用的工艺流程如图所示。
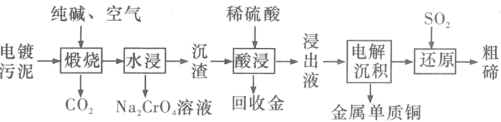
回答下列问题:
(1)52Te在元素周期表中位于___________ 族,Cu2Te的名称为___________ 。
(2)煅烧时,生成TeO2和Na2CrO4的化学反应方程式分别为:___________ 、___________ 。
(3)浸出液中的阳离子有H+、TeO2+和___________ (填化学符号)。
(4)“还原”时的离子反应方程式为___________ ,为降低成本,提高原料的利用率。可采取的措施是___________ 。
(5) 在溶液中可转化为
在溶液中可转化为 :2
:2 +2H+
+2H+
 +H2O。常温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中达到平衡时,c(
+H2O。常温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中达到平衡时,c( )随c(H+)的变化如图所示。
)随c(H+)的变化如图所示。
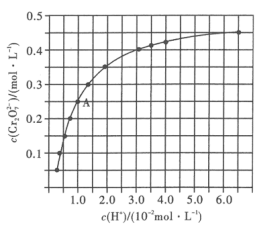
根据A点数据,计算出该转化反应的平衡常数K=___________ 。

回答下列问题:
(1)52Te在元素周期表中位于
(2)煅烧时,生成TeO2和Na2CrO4的化学反应方程式分别为:
(3)浸出液中的阳离子有H+、TeO2+和
(4)“还原”时的离子反应方程式为
(5)
 在溶液中可转化为
在溶液中可转化为 :2
:2 +2H+
+2H+
 +H2O。常温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中达到平衡时,c(
+H2O。常温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中达到平衡时,c( )随c(H+)的变化如图所示。
)随c(H+)的变化如图所示。
根据A点数据,计算出该转化反应的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上制取硝酸铵的流程图如图,请回答下列问题:_______ 。
(2)在合成硝酸的吸收塔中通入空气的目的是:_______ 。
(3)在合成氨的设备(合成塔)中,设置热交换器的目的是:_______ 。
(4)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH=2NaNO2+H2O
NH3还原法:NH3+NO2=N2+H2O
①配平NH3还原法的化学方程式_______ 。
②以上两种方法中,符合绿色化学的是_______ 。
③某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的百分比含量:_______ 。

(2)在合成硝酸的吸收塔中通入空气的目的是:
(3)在合成氨的设备(合成塔)中,设置热交换器的目的是:
(4)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH=2NaNO2+H2O
NH3还原法:NH3+NO2=N2+H2O
①配平NH3还原法的化学方程式
②以上两种方法中,符合绿色化学的是
③某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的百分比含量:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】CuCl广泛应用于化工和印染等行业。某研究小组用粗铜(含杂质Fe) 为原料制备CuCl2·2H2O晶体,再用CuCl2·2H2O晶体制备CuCl。
(1)制备CuCl2·2H2O晶体:
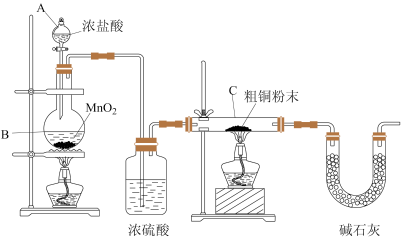
① B装置中发生反应的化学方程式是_________________
② 装置C中粗铜粉末(含杂质Fe)与气体充分反应时的生成物是______________
③ 反应完成后,将C中的固体用稀盐酸完全溶解,再调节pH值除杂,经一系列操作便可获得CuCl2·2H2O晶体。溶解C中生成物固体时,有时会加入少量双氧水,目的是__________
(2)制取CuCl,为了制取CuCl采用如图所示装置进行实验(夹持仪器略):
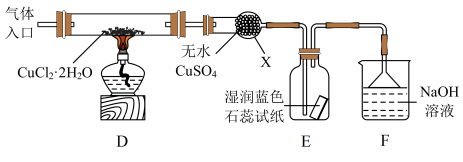
已知:
④仪器X的名称是__________
⑤实验操作的先后顺序是a→__________________________ →e(填操作的编号)。
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
⑥装置F中NaOH溶液的作用是___________________ 。
⑦ 反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质。请分析产生CuCl2杂质的原因是__________________________
(1)制备CuCl2·2H2O晶体:

① B装置中发生反应的化学方程式是
② 装置C中粗铜粉末(含杂质Fe)与气体充分反应时的生成物是
③ 反应完成后,将C中的固体用稀盐酸完全溶解,再调节pH值除杂,经一系列操作便可获得CuCl2·2H2O晶体。溶解C中生成物固体时,有时会加入少量双氧水,目的是
(2)制取CuCl,为了制取CuCl采用如图所示装置进行实验(夹持仪器略):

已知:

④仪器X的名称是
⑤实验操作的先后顺序是a→
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
⑥装置F中NaOH溶液的作用是
⑦ 反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质。请分析产生CuCl2杂质的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某铜矿石的主要成分为Cu2O,还含有少量Al2O3、Fe2O3、SiO2。工业上用该矿石获取铜和胆矾的操作流程如下:
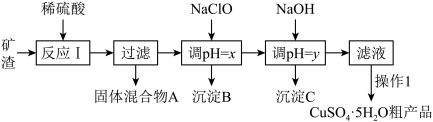
已知:①Cu2O+2H+=Cu+Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)实际生产中将矿石粉碎为矿渣的目的是___________ 。
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为___________ 。
(3)反应Ⅰ完成后的滤液中铁元素的存在形式为___________ (填离子符号),检验该离子常用的试剂为___________ ,生成该离子的离子方程式为___________ 。
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围___________ 。
(6)操作1主要包括:蒸发浓缩、冷却结晶、过滤、 冷水洗涤得到CuSO4·5H2O。如何洗涤CuSO4·5H2O粗品___________ 。

已知:①Cu2O+2H+=Cu+Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 5.4 | 4.0 | 2.7 | 5.8 |
| 沉淀完全的pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)实际生产中将矿石粉碎为矿渣的目的是
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为
(3)反应Ⅰ完成后的滤液中铁元素的存在形式为
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围
(6)操作1主要包括:蒸发浓缩、冷却结晶、过滤、 冷水洗涤得到CuSO4·5H2O。如何洗涤CuSO4·5H2O粗品
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1) 可用作有机合成的催化剂。
可用作有机合成的催化剂。 是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。
是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。
次磷酸 是一种强还原剂,将它加入
是一种强还原剂,将它加入 水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生
水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生 。写出生成CuH的化学方程式:
。写出生成CuH的化学方程式:___________ 。
(2)某同学利用如下图所示装置,测定高炉煤气中CO、 、
、 和
和 的百分组成。
的百分组成。
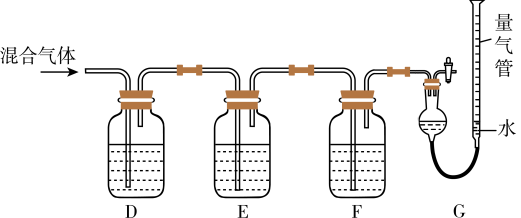
已知:i. 的盐酸溶液能吸收CO形成
的盐酸溶液能吸收CO形成 。
。
ii.保险粉 和KOH的混合溶液能吸收氧气。
和KOH的混合溶液能吸收氧气。
请回答以下问题:
①G中测出的是___________ (填物质的化学式)的体积。
②F洗气瓶中宜盛放的试剂是___________ 。
(3)工业上可以在酸性介质中用 氧化浸出黄铜矿
氧化浸出黄铜矿 。
。
① 反应后转化为
反应后转化为 、
、 、
、 。将
。将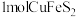 完全转化,理论上所需
完全转化,理论上所需 的物质的量为
的物质的量为___________ 。
②浸出过程中发现, 的反应实际用量远大于理论用量,原因是
的反应实际用量远大于理论用量,原因是___________ 。
③若浸出过程中,溶液中含有少量 ,则会析出黄钠铁矾
,则会析出黄钠铁矾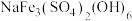 沉淀。写出
沉淀。写出 转化为黄钠铁矾沉淀的离子方程式:
转化为黄钠铁矾沉淀的离子方程式:___________ 。
(1)
 可用作有机合成的催化剂。
可用作有机合成的催化剂。 是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。
是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。次磷酸
 是一种强还原剂,将它加入
是一种强还原剂,将它加入 水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生
水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生 。写出生成CuH的化学方程式:
。写出生成CuH的化学方程式:(2)某同学利用如下图所示装置,测定高炉煤气中CO、
 、
、 和
和 的百分组成。
的百分组成。
已知:i.
 的盐酸溶液能吸收CO形成
的盐酸溶液能吸收CO形成 。
。ii.保险粉
 和KOH的混合溶液能吸收氧气。
和KOH的混合溶液能吸收氧气。请回答以下问题:
①G中测出的是
②F洗气瓶中宜盛放的试剂是
(3)工业上可以在酸性介质中用
 氧化浸出黄铜矿
氧化浸出黄铜矿 。
。①
 反应后转化为
反应后转化为 、
、 、
、 。将
。将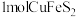 完全转化,理论上所需
完全转化,理论上所需 的物质的量为
的物质的量为②浸出过程中发现,
 的反应实际用量远大于理论用量,原因是
的反应实际用量远大于理论用量,原因是③若浸出过程中,溶液中含有少量
 ,则会析出黄钠铁矾
,则会析出黄钠铁矾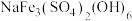 沉淀。写出
沉淀。写出 转化为黄钠铁矾沉淀的离子方程式:
转化为黄钠铁矾沉淀的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】雾霾中含有多种污染物,包括氮氧化物 、CO、
、CO、 等。它们可以通过化学反应得到一定的消除或转化。
等。它们可以通过化学反应得到一定的消除或转化。
 氮硫的氧化物的转化:
氮硫的氧化物的转化: 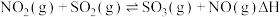
已知: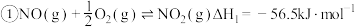
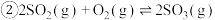
 ,则
,则
_______  。
。
一定条件下,将 与
与 以一定比例置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有
以一定比例置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有_______ 。
a.混合气体的密度不变 b.混合气体的颜色保持不变
c.SO3和NO的体积比保持不变 d.反应速率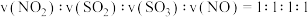
 碳氧化物的转化:
碳氧化物的转化:
 可用于合成甲醇,反应方程式为:
可用于合成甲醇,反应方程式为: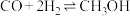 ,在一恒温恒容密闭容器中充入
,在一恒温恒容密闭容器中充入 和
和 进行上述反应。测得CO和
进行上述反应。测得CO和 浓度随时间变化如图1所示。
浓度随时间变化如图1所示。

则 内,氢气的反应速率为
内,氢气的反应速率为____ 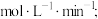 第
第 后,保持温度不变,向该密闭容器中再充入
后,保持温度不变,向该密闭容器中再充入 和
和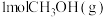 ,则平衡
,则平衡_______  填“正向”、“逆向”或“不”
填“正向”、“逆向”或“不” 移动。
移动。
 通过电解CO制备
通过电解CO制备 ,电解液为碳酸钠溶液,工作原理如图2所示,写出阴极的电极反应式
,电解液为碳酸钠溶液,工作原理如图2所示,写出阴极的电极反应式_____ 。若以甲醇燃料电池作为电源,则生成标准状况下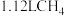 需要消耗
需要消耗 的质量为
的质量为_______ 。
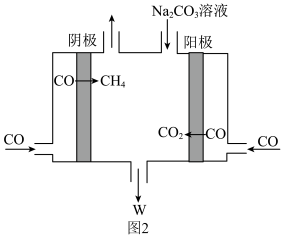
 硫氧化物的转化:硫的氧化物与一定量氨气、空气反应,可生成硫酸铵。硫酸铵水溶液呈酸性的原因是
硫氧化物的转化:硫的氧化物与一定量氨气、空气反应,可生成硫酸铵。硫酸铵水溶液呈酸性的原因是________________  用离子方程式表示
用离子方程式表示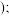 室温时,向
室温时,向 溶液中滴入NaOH溶液至溶液呈中性,则所得溶液中微粒浓度大小关系:
溶液中滴入NaOH溶液至溶液呈中性,则所得溶液中微粒浓度大小关系:
____  填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。
 、CO、
、CO、 等。它们可以通过化学反应得到一定的消除或转化。
等。它们可以通过化学反应得到一定的消除或转化。 氮硫的氧化物的转化:
氮硫的氧化物的转化: 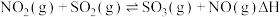
已知:
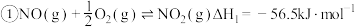
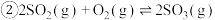
 ,则
,则
 。
。一定条件下,将
 与
与 以一定比例置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有
以一定比例置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有a.混合气体的密度不变 b.混合气体的颜色保持不变
c.SO3和NO的体积比保持不变 d.反应速率
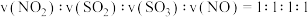
 碳氧化物的转化:
碳氧化物的转化: 可用于合成甲醇,反应方程式为:
可用于合成甲醇,反应方程式为: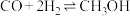 ,在一恒温恒容密闭容器中充入
,在一恒温恒容密闭容器中充入 和
和 进行上述反应。测得CO和
进行上述反应。测得CO和 浓度随时间变化如图1所示。
浓度随时间变化如图1所示。
则
 内,氢气的反应速率为
内,氢气的反应速率为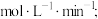 第
第 后,保持温度不变,向该密闭容器中再充入
后,保持温度不变,向该密闭容器中再充入 和
和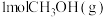 ,则平衡
,则平衡 填“正向”、“逆向”或“不”
填“正向”、“逆向”或“不” 移动。
移动。 通过电解CO制备
通过电解CO制备 ,电解液为碳酸钠溶液,工作原理如图2所示,写出阴极的电极反应式
,电解液为碳酸钠溶液,工作原理如图2所示,写出阴极的电极反应式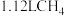 需要消耗
需要消耗 的质量为
的质量为
 硫氧化物的转化:硫的氧化物与一定量氨气、空气反应,可生成硫酸铵。硫酸铵水溶液呈酸性的原因是
硫氧化物的转化:硫的氧化物与一定量氨气、空气反应,可生成硫酸铵。硫酸铵水溶液呈酸性的原因是 用离子方程式表示
用离子方程式表示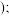 室温时,向
室温时,向 溶液中滴入NaOH溶液至溶液呈中性,则所得溶液中微粒浓度大小关系:
溶液中滴入NaOH溶液至溶液呈中性,则所得溶液中微粒浓度大小关系:
 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】习近平主席在第七十五届联合国大会一般性辩论会上表示,中国将提高国家自主贡献力度,采取更加有力的政策和措施,二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。CO2可通过反应转化为重要的化工原料。
(1)工业上常用“碳捕捉”技术来“捕捉”空气中的二氧化碳,再把捕捉的二氧化碳提取出来,经化学反应使之变成甲醇(CH3OH)和水,其流程如图所示( 部分反应条件和物质未标出):

①将Y加入X溶液后发生反应的化学方程式为_______ ;_______ 。
②合成塔内的反应条件为300℃,200kPa和催化剂,用CO2来生产燃料甲醇的某些化学键的键能数据如下表:
写出该反应的热化学方程式:_______ 。
③甲醇与CO可以生成醋酸,常温下将a mol·L-1的醋酸与b mol·L-1Ba(OH)2溶液以2:1体积比混合,混合溶液中2c(Ba2+)=c(CH3COO- ),则醋酸的电离平衡常数为_______ (忽略混合过程中溶液体积的变化,用含a和b的代数式表示)。
(2)CO2可制取二甲醚,热化学方程为2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) =-125kJ/mol。往一容积为2L的恒容密闭容器中通入2mol CO2和6mol H2,一定温度下发生该反应,起始总压为P0,20min时达到化学平衡状态,测得CH3OCH3的物质的量分数为12. 5%。
=-125kJ/mol。往一容积为2L的恒容密闭容器中通入2mol CO2和6mol H2,一定温度下发生该反应,起始总压为P0,20min时达到化学平衡状态,测得CH3OCH3的物质的量分数为12. 5%。
①达到化学平衡状态时,下列有关叙述正确的是_______ (填序号)。
a.容器内气体压强不再发生改变
b.正、逆反应速率相等且均为零
c.向容器内再通入1mol CO2和3mol H2,重新达平衡后CH3OCH3体积分数增大
d.向容器内通入少量氦气,则平衡向正反应方向移动
②0~20min内,用H2表示的平均反应速率v( H2)=_______ ,该温度下, 反应的平衡常数Kp=_______ (用含P0的式子表达,用平衡分压代替平衡浓度计算,分压=总压x物质的量分数)。
③升高温度,二甲醚的平衡产率_______ (填“增大”“减小”或“不变”)。
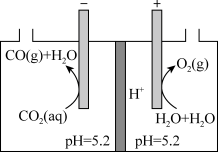
(3)科学家研究将CO2转化为可利用的再生能源是一种理想选择,可用如图所示电化学法进行CO2转化。写出通入CO2一极的电极反应式:_______ 。
(1)工业上常用“碳捕捉”技术来“捕捉”空气中的二氧化碳,再把捕捉的二氧化碳提取出来,经化学反应使之变成甲醇(CH3OH)和水,其流程如图所示( 部分反应条件和物质未标出):

①将Y加入X溶液后发生反应的化学方程式为
②合成塔内的反应条件为300℃,200kPa和催化剂,用CO2来生产燃料甲醇的某些化学键的键能数据如下表:
| 化学键 | C-C | C-H | H-H | C-O | C=O | H-O |
| 键能/kJ·mol-1 | 348 | 413 | 436 | 358 | 750 | 463 |
③甲醇与CO可以生成醋酸,常温下将a mol·L-1的醋酸与b mol·L-1Ba(OH)2溶液以2:1体积比混合,混合溶液中2c(Ba2+)=c(CH3COO- ),则醋酸的电离平衡常数为
(2)CO2可制取二甲醚,热化学方程为2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)
 =-125kJ/mol。往一容积为2L的恒容密闭容器中通入2mol CO2和6mol H2,一定温度下发生该反应,起始总压为P0,20min时达到化学平衡状态,测得CH3OCH3的物质的量分数为12. 5%。
=-125kJ/mol。往一容积为2L的恒容密闭容器中通入2mol CO2和6mol H2,一定温度下发生该反应,起始总压为P0,20min时达到化学平衡状态,测得CH3OCH3的物质的量分数为12. 5%。①达到化学平衡状态时,下列有关叙述正确的是
a.容器内气体压强不再发生改变
b.正、逆反应速率相等且均为零
c.向容器内再通入1mol CO2和3mol H2,重新达平衡后CH3OCH3体积分数增大
d.向容器内通入少量氦气,则平衡向正反应方向移动
②0~20min内,用H2表示的平均反应速率v( H2)=
③升高温度,二甲醚的平衡产率
(3)科学家研究将CO2转化为可利用的再生能源是一种理想选择,可用如图所示电化学法进行CO2转化。写出通入CO2一极的电极反应式:

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】在水体中部分含氮有机物循环如图1所示.
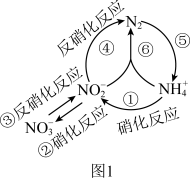

(1)图中属于氮的固定的是____ (填序号).
(2)图中①②的转化是在亚硝化细菌和硝化细菌作用下进行的,已知:
2NH4+(aq)+3O2═2NO2﹣(aq)+4H+(aq)+2H2O(l)△H1=﹣556.8kJ/mol
2NO2﹣(aq)+O2(g)=2NO3﹣(aq);△H2=﹣145.2kJ•mol﹣1
则反应NH4+(aq)+2O2(g)=NO3﹣(aq)+2H+(aq)+H2O(1)△H3=____ kJ•mol﹣1
(3)某科研机构研究通过化学反硝化的方法除脱水体中过量的NO3﹣,他们在图示的三颈烧瓶中(装置如图2)中,加入NO3﹣起始浓度为45mg•L﹣1的水样、自制的纳米铁粉,起始时pH=2.5,控制水浴温度为25℃、搅拌速率为500转/分,实验中每间隔一定时间从取样口检测水体中NO3﹣、NO2﹣及pH(NH4+、N2未检测)的相关数据(如图3).
①实验室可通过反应Fe(H2O)62++2BH4﹣=Fe↓+2H3BO3+7H2↑制备纳米铁粉,每生成1molFe转移电子总的物质的量为____ .
②向三颈烧瓶中通入N2的目的是____ .
③开始反应0~20min,pH快速升高到约6.2,原因之一是___________ ;NO3﹣还原为NH4+及少量在20~250min时,加入缓冲溶液维持pH6.2左右,NO3﹣主要还原为NH4+,Fe转化为Fe(OH)2,该反应的离子方程式为___
(4)一种可以降低水体中NO3﹣含量的方法是:在废水中加入食盐后用特殊电极进行电解反硝化脱除,原理可用图4简要说明.
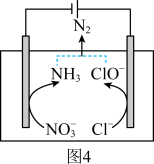
①电解时,阴极的电极反应式为_____ .
②溶液中逸出N2的离子方程式为_____ .


(1)图中属于氮的固定的是
(2)图中①②的转化是在亚硝化细菌和硝化细菌作用下进行的,已知:
2NH4+(aq)+3O2═2NO2﹣(aq)+4H+(aq)+2H2O(l)△H1=﹣556.8kJ/mol
2NO2﹣(aq)+O2(g)=2NO3﹣(aq);△H2=﹣145.2kJ•mol﹣1
则反应NH4+(aq)+2O2(g)=NO3﹣(aq)+2H+(aq)+H2O(1)△H3=
(3)某科研机构研究通过化学反硝化的方法除脱水体中过量的NO3﹣,他们在图示的三颈烧瓶中(装置如图2)中,加入NO3﹣起始浓度为45mg•L﹣1的水样、自制的纳米铁粉,起始时pH=2.5,控制水浴温度为25℃、搅拌速率为500转/分,实验中每间隔一定时间从取样口检测水体中NO3﹣、NO2﹣及pH(NH4+、N2未检测)的相关数据(如图3).
①实验室可通过反应Fe(H2O)62++2BH4﹣=Fe↓+2H3BO3+7H2↑制备纳米铁粉,每生成1molFe转移电子总的物质的量为
②向三颈烧瓶中通入N2的目的是
③开始反应0~20min,pH快速升高到约6.2,原因之一是
(4)一种可以降低水体中NO3﹣含量的方法是:在废水中加入食盐后用特殊电极进行电解反硝化脱除,原理可用图4简要说明.

①电解时,阴极的电极反应式为
②溶液中逸出N2的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】乙酰苯胺是染料和合成樟脑等的中间体,传统制备多为乙酸和苯温度计胺脱水缩合而成。反应原理为:CH3COOH+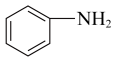

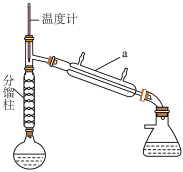
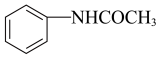 +H2O,装置如图所示。在圆底烧瓶中加入9.00g(0.15mol)乙酸、4.65g(0.05mol)苯胺、0.14g锌粉,小火加热圆底烧瓶,保持温度计读数在105℃左右,生成的水(含少量乙酸)被蒸出分离,反应约1.5h,产率为58.0%。
+H2O,装置如图所示。在圆底烧瓶中加入9.00g(0.15mol)乙酸、4.65g(0.05mol)苯胺、0.14g锌粉,小火加热圆底烧瓶,保持温度计读数在105℃左右,生成的水(含少量乙酸)被蒸出分离,反应约1.5h,产率为58.0%。
已知:苯胺在空气中极易被氧化而变为黄色;各物质的性质见下表。
回答下列问题:
(1)仪器a的名称是___________ ,分馏柱的作用是___________ 。
(2)加入锌粉的目的是___________ 。
(3)加入乙酸较苯胺多,其目的是___________ 。
(4)实际操作中保持温度在105℃左右,不能过高与过低的原因是___________ 。
(5)反应完成后,经冷却结晶、抽滤、重结晶制得产物。可以用重结晶方法提纯乙酰苯胺的原因是___________ 。
(6)实验改进:将Zn替换为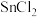 ,多次实验结果如下表。
,多次实验结果如下表。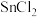 的最佳用量为
的最佳用量为___________ mmol;能用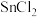 替代锌粉的证据是
替代锌粉的证据是___________ (任答1点)。


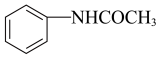 +H2O,装置如图所示。在圆底烧瓶中加入9.00g(0.15mol)乙酸、4.65g(0.05mol)苯胺、0.14g锌粉,小火加热圆底烧瓶,保持温度计读数在105℃左右,生成的水(含少量乙酸)被蒸出分离,反应约1.5h,产率为58.0%。
+H2O,装置如图所示。在圆底烧瓶中加入9.00g(0.15mol)乙酸、4.65g(0.05mol)苯胺、0.14g锌粉,小火加热圆底烧瓶,保持温度计读数在105℃左右,生成的水(含少量乙酸)被蒸出分离,反应约1.5h,产率为58.0%。
已知:苯胺在空气中极易被氧化而变为黄色;各物质的性质见下表。
| 药品 | 性状 | 熔点(℃) | 沸点(℃) | 乙酰苯胺的溶解度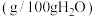 | ||||
| 苯胺 | 无色液体 | 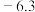 | 184.4 | 20℃ | 50℃ | 80℃ | 100℃ | |
| 乙酰苯胺 | 白色结晶 | 114.3 | 304 | 0.46 | 0.84 | 3.45 | 5.55 | |
| 乙酸 | 无色液体 | 16.6 | 117.9 | |||||
(1)仪器a的名称是
(2)加入锌粉的目的是
(3)加入乙酸较苯胺多,其目的是
(4)实际操作中保持温度在105℃左右,不能过高与过低的原因是
(5)反应完成后,经冷却结晶、抽滤、重结晶制得产物。可以用重结晶方法提纯乙酰苯胺的原因是
(6)实验改进:将Zn替换为
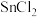 ,多次实验结果如下表。
,多次实验结果如下表。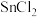 的最佳用量为
的最佳用量为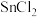 替代锌粉的证据是
替代锌粉的证据是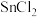 物质的量/mmol 物质的量/mmol | 0 | 0.80 | 1.6 | 2.5 | 3.3 | 4.1 |
| 粗产物颜色 | 黄 | 淡黄 | 淡黄 | 微黄 | 白 | 白 |
| 产率/% | 47.0 | 52.7 | 52.7 | 56.1 | 58.3 | 53.1 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】I.铈及其化合物在工业生产中应用广泛。以某玻璃废料(主要成分为 、
、 、
、 、FeO等)为原料制备
、FeO等)为原料制备 和
和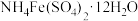 (硫酸铁铵晶体)。其流程如下(已知
(硫酸铁铵晶体)。其流程如下(已知 既不溶于稀硫酸,也不溶于氢氧化钠溶液):
既不溶于稀硫酸,也不溶于氢氧化钠溶液):
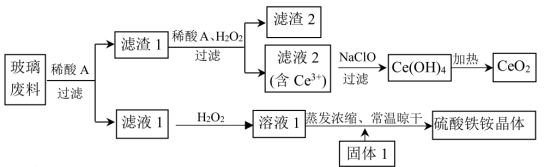
回答下列问题:
(1)浸取玻璃废料选用的“稀酸A”为___________ (填“稀硫酸”或“稀盐酸”)。
(2)向滤渣1中加入 的目的是
的目的是___________ (用离子方程式表示)。为了提高溶解“滤渣1”的速率,常采用加热措施,但温度高于 时溶解速率减慢,其主要原因是
时溶解速率减慢,其主要原因是___________ 。
(3)为了少引入杂质,所选用固体1的化学式为___________ 。
(4)制备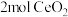 需要NaClO的质量为
需要NaClO的质量为___________ 。
II.NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下图所示:
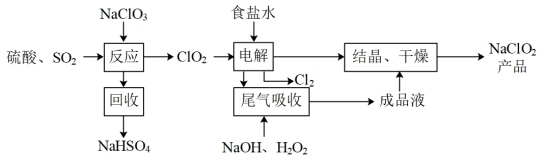
(5)写出“反应”步骤中生成ClO2的化学方程式:___________ 。
(6)“尾气吸收”是吸收电解过程排出的少量ClO2。写出此吸收反应的化学方程式:______ 。
 、
、 、
、 、FeO等)为原料制备
、FeO等)为原料制备 和
和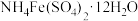 (硫酸铁铵晶体)。其流程如下(已知
(硫酸铁铵晶体)。其流程如下(已知 既不溶于稀硫酸,也不溶于氢氧化钠溶液):
既不溶于稀硫酸,也不溶于氢氧化钠溶液):
回答下列问题:
(1)浸取玻璃废料选用的“稀酸A”为
(2)向滤渣1中加入
 的目的是
的目的是 时溶解速率减慢,其主要原因是
时溶解速率减慢,其主要原因是(3)为了少引入杂质,所选用固体1的化学式为
(4)制备
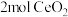 需要NaClO的质量为
需要NaClO的质量为II.NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下图所示:

(5)写出“反应”步骤中生成ClO2的化学方程式:
(6)“尾气吸收”是吸收电解过程排出的少量ClO2。写出此吸收反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】软锰矿主要成分为 ,含少量
,含少量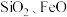 和
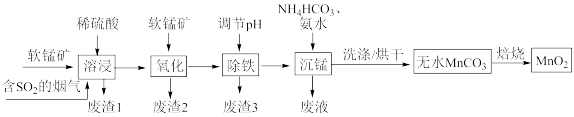
和 等杂质,以软锰矿为主要原料吸收脱除工业含硫烟气中的
等杂质,以软锰矿为主要原料吸收脱除工业含硫烟气中的 ,制备纯净
,制备纯净 的工艺流程如图。
的工艺流程如图。
已知:常温下,不同金属离子生成氢氧化物沉淀的 如下表:
如下表:
回答下列问题:
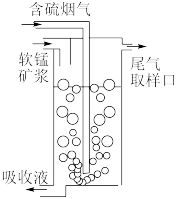
(1)“溶浸”所用吸收塔如图所示,描述有利于提高吸收效率的设计之一:_______ 。
(2)调节溶液的 前,加入软锰矿的作用是
前,加入软锰矿的作用是_______ 。
(3)“调节 ”时可选用的试剂为
”时可选用的试剂为_______ (填化学式)。调节 ,充分反应后生成的沉淀为
,充分反应后生成的沉淀为_______ 。
(4)“沉锰”过程中再次加入氨水的目的是_______ (从化学平衡移动的角度解释)。“沉锰”过程宜在较低温度下进行,可能原因是_______ (写1条即可)。
 ,含少量
,含少量 和
和 等杂质,以软锰矿为主要原料吸收脱除工业含硫烟气中的
等杂质,以软锰矿为主要原料吸收脱除工业含硫烟气中的 ,制备纯净
,制备纯净 的工艺流程如图。
的工艺流程如图。
已知:常温下,不同金属离子生成氢氧化物沉淀的
 如下表:
如下表:| 离子 |  |  |  |
开始沉淀时 | 1.8 | 7.7 | 7.8 |
完全沉淀时 | 3.2 | 9.7 | 9.8 |

(1)“溶浸”所用吸收塔如图所示,描述有利于提高吸收效率的设计之一:
(2)调节溶液的
 前,加入软锰矿的作用是
前,加入软锰矿的作用是(3)“调节
 ”时可选用的试剂为
”时可选用的试剂为 ,充分反应后生成的沉淀为
,充分反应后生成的沉淀为(4)“沉锰”过程中再次加入氨水的目的是
您最近一年使用:0次



