10 ℃加热NaHCO3饱和溶液,测得该溶液的pH发生如下的变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该水解反应的离子方程式为______________ 。
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度________ (填“大于”或“小于”)NaHCO3,该分解反应的化学方程式为____ 。
(3)丙同学认为甲、乙的判断都不充分。丙认为:
①只要在加热煮沸的溶液中加入足量的试剂BaCl2溶液,若产生沉淀,则乙判断正确。原因是____________ (写出反应的离子方程式)。能不能选用Ba(OH)2溶液?______ (答“能”或“不能”)。
②将加热后的溶液冷却到10 ℃,若溶液的pH________ (填“大于”“小于”或“等于”)8.3,则________ (填“甲”或“乙”)判断正确。
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50 ℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该水解反应的离子方程式为
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
(3)丙同学认为甲、乙的判断都不充分。丙认为:
①只要在加热煮沸的溶液中加入足量的试剂BaCl2溶液,若产生沉淀,则乙判断正确。原因是
②将加热后的溶液冷却到10 ℃,若溶液的pH
更新时间:2019-11-12 11:37:33
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】聚合硫酸铁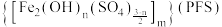 是一种应用广泛的水处理剂。制备方法如下:
是一种应用广泛的水处理剂。制备方法如下:
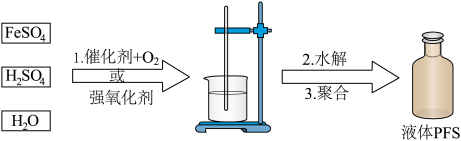
(1)氧化可采用催化氧化或直接氧化。
①以 为氧化剂,
为氧化剂, 作催化剂,需控温55℃,反应4h。氧化的化学方程式为
作催化剂,需控温55℃,反应4h。氧化的化学方程式为_______ 。
②以 为氧化剂,需控温40-70℃,反应1-3h。检验氧化反应已经发生的方法是
为氧化剂,需控温40-70℃,反应1-3h。检验氧化反应已经发生的方法是_______ 。
③以NaClO作为氧化剂,比方法② 用量大,反应中生成少量污染性气体。原因是
用量大,反应中生成少量污染性气体。原因是_______ 。
(2)水解-聚合过程中部分反应过程如下:

①水解-聚合过程中pH变化趋势是_______ 。
②聚合的原理是_______ 。
③聚合硫酸铁净水效果好的原因是_______ 。
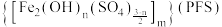 是一种应用广泛的水处理剂。制备方法如下:
是一种应用广泛的水处理剂。制备方法如下:
(1)氧化可采用催化氧化或直接氧化。
①以
 为氧化剂,
为氧化剂, 作催化剂,需控温55℃,反应4h。氧化的化学方程式为
作催化剂,需控温55℃,反应4h。氧化的化学方程式为②以
 为氧化剂,需控温40-70℃,反应1-3h。检验氧化反应已经发生的方法是
为氧化剂,需控温40-70℃,反应1-3h。检验氧化反应已经发生的方法是③以NaClO作为氧化剂,比方法②
 用量大,反应中生成少量污染性气体。原因是
用量大,反应中生成少量污染性气体。原因是(2)水解-聚合过程中部分反应过程如下:

①水解-聚合过程中pH变化趋势是
②聚合的原理是
③聚合硫酸铁净水效果好的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.Na2O2具有很强的氧化性,其与FeCl2溶液能发生反应:Na2O2+FeCl2+H2O→Fe(OH)3↓+FeCl3+NaCl(未配平)。
(1)已知FeCl2的化学计量数为6,配平上述化学方程式,并标出电子转移的方向和数目:_______ 。该反应中氧化产物是_______ 。
Ⅱ.碳酸氢钠俗称“小苏打”,在生活、生产中用途广泛。
(2)泡沫灭火器中主要成分是NaHCO3溶液和Al2(SO4)3 溶液,二者混合后发生相互促进的水解反应生成 Al(OH)3和CO2进行灭火,写出该反应的化学方程式:_______ 。
(3)向NaHCO3溶液中加入少许Ba(OH)2固体,忽略溶液体积变化,溶液中c(CO )的变化是
)的变化是_______ (填“增大”“减小”或“不变”)。
(4)NaHCO3是氨碱法和联合制碱法制纯碱的中间产物,在滤出小苏打后,母液提取氯化铵有两种方法:①通入氨,冷却、加食盐,过滤;②不通入氨,冷却、加食盐,过滤。这两种方法中,_______ (填“①”或“②”)析出的氯化铵纯度更高。
(1)已知FeCl2的化学计量数为6,配平上述化学方程式,并标出电子转移的方向和数目:
Ⅱ.碳酸氢钠俗称“小苏打”,在生活、生产中用途广泛。
(2)泡沫灭火器中主要成分是NaHCO3溶液和Al2(SO4)3 溶液,二者混合后发生相互促进的水解反应生成 Al(OH)3和CO2进行灭火,写出该反应的化学方程式:
(3)向NaHCO3溶液中加入少许Ba(OH)2固体,忽略溶液体积变化,溶液中c(CO
 )的变化是
)的变化是(4)NaHCO3是氨碱法和联合制碱法制纯碱的中间产物,在滤出小苏打后,母液提取氯化铵有两种方法:①通入氨,冷却、加食盐,过滤;②不通入氨,冷却、加食盐,过滤。这两种方法中,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铁、铜及其化合物在日常生活及工业生产中用途非常广泛。
I.FeCl3是常用的金属蚀刻剂和净水剂。
(1)FeCl3净水的原理是___ (用离子方程式及语言表示)。
(2)FeCl3在溶液中分三步水解:Fe3++H2O Fe(OH)2++H+ K1;Fe(OH)2++H2O
Fe(OH)2++H+ K1;Fe(OH)2++H2O Fe(OH)
Fe(OH) +H+ K2;Fe(OH)
+H+ K2;Fe(OH) +H2O
+H2O Fe(OH)3+H+ K3。以上水解反应的平衡常数K1、K2、K3由大到小的顺序是
Fe(OH)3+H+ K3。以上水解反应的平衡常数K1、K2、K3由大到小的顺序是___ 。
(3)配制FeCl3溶液时,常将FeCl3晶体溶于浓盐酸中,使用时加蒸馏水稀释至指定浓度。某同学误将FeCl3直接放入自来水中(含有Mg2+、Ca2+、HCO 、Cl-等杂质离子),看到红褐色沉淀和大量气泡,试解释出现该现象的原因
、Cl-等杂质离子),看到红褐色沉淀和大量气泡,试解释出现该现象的原因___ (用离子方程式表示)。
II.CuCl2常用作电镀添加剂、催化剂及饲料添加剂。
(4)①25℃时Fe(OH)2、Fe(OH)3、Cu(OH)2的Ksp如表所示,计算当溶液中Fe2+、Cu2+浓度均为0.1mol/L时,Fe(OH)2沉淀完全及Cu(OH)2开始沉淀时的pH值(已知lg2=0.3,离子浓度小于1.0×10-5mol/L视为沉淀完全)。
②为了除去CuCl2溶液中含有的少量FeCl2,可以用氧化剂将FeCl2氧化为FeCl3,调控溶液pH___ (填范围),将FeCl3转化为Fe(OH)3除去。
I.FeCl3是常用的金属蚀刻剂和净水剂。
(1)FeCl3净水的原理是
(2)FeCl3在溶液中分三步水解:Fe3++H2O
 Fe(OH)2++H+ K1;Fe(OH)2++H2O
Fe(OH)2++H+ K1;Fe(OH)2++H2O Fe(OH)
Fe(OH) +H+ K2;Fe(OH)
+H+ K2;Fe(OH) +H2O
+H2O Fe(OH)3+H+ K3。以上水解反应的平衡常数K1、K2、K3由大到小的顺序是
Fe(OH)3+H+ K3。以上水解反应的平衡常数K1、K2、K3由大到小的顺序是(3)配制FeCl3溶液时,常将FeCl3晶体溶于浓盐酸中,使用时加蒸馏水稀释至指定浓度。某同学误将FeCl3直接放入自来水中(含有Mg2+、Ca2+、HCO
 、Cl-等杂质离子),看到红褐色沉淀和大量气泡,试解释出现该现象的原因
、Cl-等杂质离子),看到红褐色沉淀和大量气泡,试解释出现该现象的原因II.CuCl2常用作电镀添加剂、催化剂及饲料添加剂。
(4)①25℃时Fe(OH)2、Fe(OH)3、Cu(OH)2的Ksp如表所示,计算当溶液中Fe2+、Cu2+浓度均为0.1mol/L时,Fe(OH)2沉淀完全及Cu(OH)2开始沉淀时的pH值(已知lg2=0.3,离子浓度小于1.0×10-5mol/L视为沉淀完全)。
| 分子式 | Ksp | 开始沉淀时的pH | 沉淀完全时的pH |
| Fe(OH)2 | 4.0×10-17 | 6.3 | a= |
| Fe(OH)3 | 2.79×10-39 | 1.5 | 2.8 |
| Cu(OH)2 | 1.6×10-20 | b= | 6.6 |
②为了除去CuCl2溶液中含有的少量FeCl2,可以用氧化剂将FeCl2氧化为FeCl3,调控溶液pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列方程式的书写
(1) 溶液显碱性的离子方程式
溶液显碱性的离子方程式_______
(2)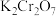 溶液中存在的化学平衡的离子方程式
溶液中存在的化学平衡的离子方程式_______
(3)硫代硫酸钠溶液与稀硫酸反应的化学方程式_______
(4)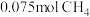 在常温常压下完全燃烧放出66kJ的热量,写出
在常温常压下完全燃烧放出66kJ的热量,写出 燃烧热的热化学方程式
燃烧热的热化学方程式_______ 。
(1)
 溶液显碱性的离子方程式
溶液显碱性的离子方程式(2)
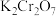 溶液中存在的化学平衡的离子方程式
溶液中存在的化学平衡的离子方程式(3)硫代硫酸钠溶液与稀硫酸反应的化学方程式
(4)
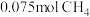 在常温常压下完全燃烧放出66kJ的热量,写出
在常温常压下完全燃烧放出66kJ的热量,写出 燃烧热的热化学方程式
燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】填写下列空白:
(1)FeCl3水溶液呈_______ 性,原因是(用离子方程式表示)_______ 。为了防止发生水解,可以加入少量的_______ 。
(2)把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______ 。
(1)FeCl3水溶液呈
(2)把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】10℃时,常压下加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为__________________________________________ 。乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度____________ (填“大于”或“小于”)NaHCO3。
(2)丙同学认为甲、乙的判断都不充分。丙认为:只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙同学判断正确。试剂X是______________ 。
A. Ba(OH)2溶液 B. BaCl2溶液 C. NaOH溶液 D. 澄清的石灰水
(3)将加热后的溶液冷却到10℃,若溶液的pH_______ (填“高于”、“低于”或“等于”)8.3,则甲同学判断正确。
(4)查阅资料,发现NaHCO3的分解温度为150℃,丙断言_______ (填“甲”或“乙”)判断是错误的,理由是_________________________________________________________________ 。
(5)将amol/L的Na2CO3溶液与bmol/L的NaHCO3溶液等体积混合,所得溶液中粒子浓度间的关系及相关判断不正确 的是_________ 。
A. c(Na+)+ c(H+)>c(CO32-)+c(HCO3-)+c(OH-)
B.c(Na+)>c(CO32-)+ c(HCO3-)+c(H2CO3)
C.若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则一定a<b
D.若c(CO32-)+2c(OH-)=2c(H+)+ c(HCO3-)+ 3c(H2CO3),则可确定a=b
(6)已知25℃时,Ksp [CaCO3]=2.8×10﹣9,Ksp [MgCO3]=6.8×10﹣6。该温度下向物质的量浓度均为0.02mol·L﹣1的MgCl2和CaCl2混合溶液中逐滴加入Na2CO3溶液,当CaCO3和MgCO3两种沉淀共存时,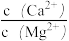 =
=_______________ (保留2位有效数字)。
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为
(2)丙同学认为甲、乙的判断都不充分。丙认为:只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙同学判断正确。试剂X是
A. Ba(OH)2溶液 B. BaCl2溶液 C. NaOH溶液 D. 澄清的石灰水
(3)将加热后的溶液冷却到10℃,若溶液的pH
(4)查阅资料,发现NaHCO3的分解温度为150℃,丙断言
(5)将amol/L的Na2CO3溶液与bmol/L的NaHCO3溶液等体积混合,所得溶液中粒子浓度间的关系及相关判断
A. c(Na+)+ c(H+)>c(CO32-)+c(HCO3-)+c(OH-)
B.c(Na+)>c(CO32-)+ c(HCO3-)+c(H2CO3)
C.若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则一定a<b
D.若c(CO32-)+2c(OH-)=2c(H+)+ c(HCO3-)+ 3c(H2CO3),则可确定a=b
(6)已知25℃时,Ksp [CaCO3]=2.8×10﹣9,Ksp [MgCO3]=6.8×10﹣6。该温度下向物质的量浓度均为0.02mol·L﹣1的MgCl2和CaCl2混合溶液中逐滴加入Na2CO3溶液,当CaCO3和MgCO3两种沉淀共存时,
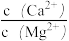 =
=
您最近一年使用:0次



