面对目前世界范围内的能源危机,甲醇作为一种较好的可再生能源,具有广泛的应用前景。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g)⇌CH3OH(g) ΔH1= -90 kJ·mol-1
②CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH2= -41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:_______________________ 。
(2)在容积为VL的容器中充入amol CO与2amol H2,在催化剂作用下反应生成甲醇,平衡时的转化率与温度、压强的关系如图所示。
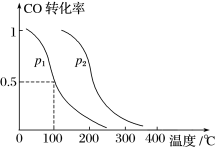
①p1________ p2(填“大于”、“小于”或“等于”);
②在温度、体积不变的情况下,再增加amol CO与2amol H2,达到新平衡时,CO的转化率________ (填“增大”、“减小”或“不变”),平衡常数_____ (填“增大”、“减小”或“不变”)。
(3)已知在T℃时,CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,则该反应________ (填“已经”或“没有”)达到平衡,此时刻υ正 ______ υ逆 (填“>”、“<”或“=”)。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g)⇌CH3OH(g) ΔH1= -90 kJ·mol-1
②CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH2= -41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:
(2)在容积为VL的容器中充入amol CO与2amol H2,在催化剂作用下反应生成甲醇,平衡时的转化率与温度、压强的关系如图所示。

①p1
②在温度、体积不变的情况下,再增加amol CO与2amol H2,达到新平衡时,CO的转化率
(3)已知在T℃时,CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,则该反应
更新时间:2019-11-24 18:22:36
|
相似题推荐
解答题-原理综合题
|
容易
(0.94)
名校
【推荐1】2020年世界环境日的宣传主题为“关爱自然,刻不容缓”。防治大气污染、水体污染等是世界各国保护环境的最重要课题。
(1)将CH4催化重整为可用的化学品,对改善环境意义重大。
①某科研团队利用Ni-CaO-Fe3O4三元催化剂在850℃下“超干重整”CH4和CO2。
已知:反应ICH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH=+247kJ/mol
2CO(g)+2H2(g) ΔH=+247kJ/mol
反应ⅡCO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41kJ/mol
CO2(g)+H2(g) ΔH=-41kJ/mol
则反应ⅢCH4(g)+3CO2(g) 4CO(g)+2H2O(g) ΔH=
4CO(g)+2H2O(g) ΔH=___________ 。
②在容积为1L的刚性容器中进行“合成气催化重整”,反应的化学方程式为:CH4(g)+CO2(g) 2CO(g)+2H2(g),当投料n(CH4):n(CO2)=1.0时,CO2的平衡转化率(ɑ)与温度(T),初始压强(p)的关系如图(1)所示。压强p1
2CO(g)+2H2(g),当投料n(CH4):n(CO2)=1.0时,CO2的平衡转化率(ɑ)与温度(T),初始压强(p)的关系如图(1)所示。压强p1___________ (填”>“=”或“<”下同)p2;当温度为T3、压强为p1时,a点时的v正___________ v逆;起始时向容器中加入1molCH4、同时加2molN2(N2不参与反应)、在温度为T6,初始压强为p2时反应,该反应的K=___________ 。
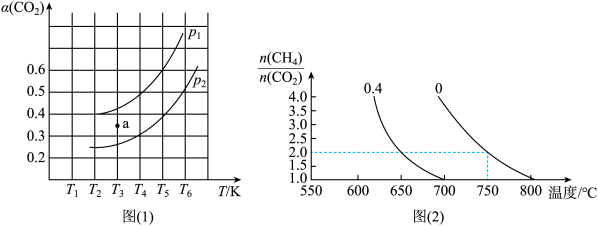
③“合成气催化重整”过程中有副产物碳生成,碳的积累会严重影响催化剂的活性。某研究小组计算和模拟实验表明积碳量(催化剂表面碳的质量与催化剂的质量之比)与投料比、温度的关系如图(2)当投料比n(CH4):n(CO2)=2.0时,要使积碳量最小,应调节温度为___________ ℃。
(2)氮氧化物是造成大气污染的主要物质,研究氮氧化物的反应机理更有助于消除大气污染。NH3催化还原NO是重要的烟气脱硝技术,研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图所示。
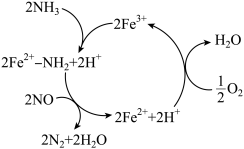
写出脱硝过程的总反应的化学方程式:___________
(1)将CH4催化重整为可用的化学品,对改善环境意义重大。
①某科研团队利用Ni-CaO-Fe3O4三元催化剂在850℃下“超干重整”CH4和CO2。
已知:反应ICH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH=+247kJ/mol
2CO(g)+2H2(g) ΔH=+247kJ/mol反应ⅡCO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-41kJ/mol
CO2(g)+H2(g) ΔH=-41kJ/mol则反应ⅢCH4(g)+3CO2(g)
 4CO(g)+2H2O(g) ΔH=
4CO(g)+2H2O(g) ΔH=②在容积为1L的刚性容器中进行“合成气催化重整”,反应的化学方程式为:CH4(g)+CO2(g)
 2CO(g)+2H2(g),当投料n(CH4):n(CO2)=1.0时,CO2的平衡转化率(ɑ)与温度(T),初始压强(p)的关系如图(1)所示。压强p1
2CO(g)+2H2(g),当投料n(CH4):n(CO2)=1.0时,CO2的平衡转化率(ɑ)与温度(T),初始压强(p)的关系如图(1)所示。压强p1
③“合成气催化重整”过程中有副产物碳生成,碳的积累会严重影响催化剂的活性。某研究小组计算和模拟实验表明积碳量(催化剂表面碳的质量与催化剂的质量之比)与投料比、温度的关系如图(2)当投料比n(CH4):n(CO2)=2.0时,要使积碳量最小,应调节温度为
(2)氮氧化物是造成大气污染的主要物质,研究氮氧化物的反应机理更有助于消除大气污染。NH3催化还原NO是重要的烟气脱硝技术,研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图所示。

写出脱硝过程的总反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐2】建设“美丽中国”首先要做好环境保护与治理。氮氧化物(NOx)是严重的大气污染物,其主要来源有汽车尾气和硝酸工厂等。氮氧化物(NOx)能引起雾霾、光化学烟雾、酸雨等环境问题。某科研机构设计了如下转化氮氧化物的几种方案。请回答下列问题:
方案I.NH3—SCR法是工业上消除氮氧化物的常用方法。该法是利用氨的还原性,在一定条件下,将烟气中的NOx直接还原为N2,主要反应原理为:4NH3+4NO+O2 4N2+6H2O。
4N2+6H2O。
(1)已知有下列热化学方程式(a、b、c均大于0):
①4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(1)△H=-akJ/mol
4N2(g)+6H2O(1)△H=-akJ/mol
②N2(g)+O2(g) 2NO(g)△H=+bkJ/mol
2NO(g)△H=+bkJ/mol
③H2O(g) H2O(1)△H=-ckJ/mol
H2O(1)△H=-ckJ/mol
则氨气与氧气反应生成NO和气态水的热化学方程式为___ 。
方案Ⅱ:利用CO在催化剂条件下还原NO2:2NO2(g)+4CO(g) N2(g)+4CO2(g)∆H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2molNO2(g)和3molCO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:
N2(g)+4CO2(g)∆H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2molNO2(g)和3molCO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:

(2)①T1___ T2(填“>”或“<”);△H___ 0(填“>”或“<”),判定的依据是___ ;
②T1温度时,该反应的平衡常数K=___ (列出数字表达式即可);
③乙容器中,平衡时NO2的转化率为___ 。
方案Ⅲ:采用原电池原理的方法消除氮氧化物的污染,其工作原理如图所示:
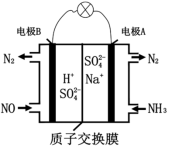
(3)该电池的负极为___ 电极(填“A”或“B”)。负极发生的电极反应式为:___ 。
方案I.NH3—SCR法是工业上消除氮氧化物的常用方法。该法是利用氨的还原性,在一定条件下,将烟气中的NOx直接还原为N2,主要反应原理为:4NH3+4NO+O2
 4N2+6H2O。
4N2+6H2O。(1)已知有下列热化学方程式(a、b、c均大于0):
①4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(1)△H=-akJ/mol
4N2(g)+6H2O(1)△H=-akJ/mol②N2(g)+O2(g)
 2NO(g)△H=+bkJ/mol
2NO(g)△H=+bkJ/mol③H2O(g)
 H2O(1)△H=-ckJ/mol
H2O(1)△H=-ckJ/mol则氨气与氧气反应生成NO和气态水的热化学方程式为
方案Ⅱ:利用CO在催化剂条件下还原NO2:2NO2(g)+4CO(g)
 N2(g)+4CO2(g)∆H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2molNO2(g)和3molCO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:
N2(g)+4CO2(g)∆H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2molNO2(g)和3molCO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:
(2)①T1
②T1温度时,该反应的平衡常数K=
③乙容器中,平衡时NO2的转化率为
方案Ⅲ:采用原电池原理的方法消除氮氧化物的污染,其工作原理如图所示:

(3)该电池的负极为
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐3】回答下列问题。
(1)一定条件下,在 密闭容器中充入
密闭容器中充入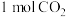 和
和 ,发生反应:
,发生反应: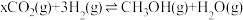 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
___________ ; 内
内 的平均反应速率
的平均反应速率
___________ 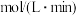 ,平衡时
,平衡时 的转化率为
的转化率为___________ 。
(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
(3)工业上常以水煤气( 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: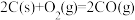
 ;
;
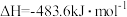 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为___________ 。
(1)一定条件下,在
 密闭容器中充入
密闭容器中充入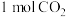 和
和 ,发生反应:
,发生反应: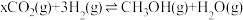 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。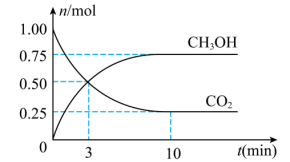

 内
内 的平均反应速率
的平均反应速率
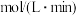 ,平衡时
,平衡时 的转化率为
的转化率为(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
| A.降低温度 | B.增加 的量 的量 | C.使用催化剂 | D.及时分离出甲醇 |
 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: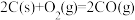
 ;
;
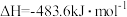 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
名校
解题方法
【推荐1】硫、氮的氧化物治理是当前化学研究的热点。回答下列问题:
(1)烟气脱硫过程涉及的反应如下:
Ca(ClO)2 (aq)+ H2SO4 (aq) CaSO4(s) +2HClO(aq) △H =a kJ·mol-1;
CaSO4(s) +2HClO(aq) △H =a kJ·mol-1;
SO2(g)+ H2O(l) + HClO(aq) H2SO4(aq) + HCl(aq) △H =b kJ·mol-1。
H2SO4(aq) + HCl(aq) △H =b kJ·mol-1。
则脱硫反应:Ca(ClO)2(aq) + 2SO2(g) + 2H2O(l) CaSO4 (s)+ H2SO4(aq) +2HCl(aq)的△H=
CaSO4 (s)+ H2SO4(aq) +2HCl(aq)的△H=_______ (用含 a、b的代数式表示)kJ·mol-1。
(2)一定温度下,向一个2 L的恒容密闭容器中充入0.4 mol NO2 ,发生反应:2NO2(g) N2O4(g) △H<0,测得不同时间时容器中NO2的浓度如下表所示。
N2O4(g) △H<0,测得不同时间时容器中NO2的浓度如下表所示。
①在0~3 min时间段内,N2O4的平均反应速率为_______ ,NO2的平衡转化率为_______ 。
②该温度下,反应的平衡常数K=_______ L·mol-1。
(1)烟气脱硫过程涉及的反应如下:
Ca(ClO)2 (aq)+ H2SO4 (aq)
 CaSO4(s) +2HClO(aq) △H =a kJ·mol-1;
CaSO4(s) +2HClO(aq) △H =a kJ·mol-1;SO2(g)+ H2O(l) + HClO(aq)
 H2SO4(aq) + HCl(aq) △H =b kJ·mol-1。
H2SO4(aq) + HCl(aq) △H =b kJ·mol-1。则脱硫反应:Ca(ClO)2(aq) + 2SO2(g) + 2H2O(l)
 CaSO4 (s)+ H2SO4(aq) +2HCl(aq)的△H=
CaSO4 (s)+ H2SO4(aq) +2HCl(aq)的△H=(2)一定温度下,向一个2 L的恒容密闭容器中充入0.4 mol NO2 ,发生反应:2NO2(g)
 N2O4(g) △H<0,测得不同时间时容器中NO2的浓度如下表所示。
N2O4(g) △H<0,测得不同时间时容器中NO2的浓度如下表所示。| 时间/min | 0 | 1 | 2 | 3 | 4 |
| c(NO2)/(mol·L-1) | 0.2 | 0.15 | 0.12 | 0.11 | 0.11 |
②该温度下,反应的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
名校
【推荐2】甲醇水蒸气催化重整反应是生产氢能的有效方法之一:CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)。已知Kp表示用分压表示平衡常数,气体分压=气体物质的量分数×总压。此反应机理可以整合为以下途径:
甲醇分解(I):CH3OH(g)⇌CO(g)+2H2(g) △H1(kJ/mol)
水煤气变换(II):CO(g)+H2O(g)⇌CO2(g)+H2(g) △H2(kJ/mol)
甲醇分解(I)、水煤气变换(II)的反应平衡常数Kp与温度关系见表:
①△HI__ 0,△HII__ 0(填“>”或“<”)
②398K时,反应CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)的Kp=___ (kpa)2。
甲醇分解(I):CH3OH(g)⇌CO(g)+2H2(g) △H1(kJ/mol)
水煤气变换(II):CO(g)+H2O(g)⇌CO2(g)+H2(g) △H2(kJ/mol)
甲醇分解(I)、水煤气变换(II)的反应平衡常数Kp与温度关系见表:
| 温度T | 398K | 498K | 598K | 698K | 798K | 898K |
| 甲醇分解Kp(I)/kpa | 0.50 | 185.8 | 9939.5 | 1.8×105 | 1.6×106 | 9.3×106 |
| 水煤气变换Kp(II) | 1577 | 137.5 | 28.14 | 9.339 | 4.180 | 2.276 |
②398K时,反应CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)的Kp=
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐3】建设“美丽中国”首先要做好环境保护与治理。氮氧化物(NOx)是严重的大气污染物,其主要来源有汽车尾气和硝酸工厂等。氮氧化物(NOx)能引起雾霾、光化学烟雾、酸雨等环境问题。某科研机构设计了如下转化氮氧化物的几种方案。请回答下列问题:
方案I.NH3—SCR法是工业上消除氮氧化物的常用方法。该法是利用氨的还原性,在一定条件下,将烟气中的NOx直接还原为N2,主要反应原理为:4NH3+4NO+O2 4N2+6H2O。
4N2+6H2O。
(1)已知有下列热化学方程式(a、b、c均大于0):
①4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(1)△H=-akJ/mol
4N2(g)+6H2O(1)△H=-akJ/mol
②N2(g)+O2(g) 2NO(g)△H=+bkJ/mol
2NO(g)△H=+bkJ/mol
③H2O(g) H2O(1)△H=-ckJ/mol
H2O(1)△H=-ckJ/mol
则氨气与氧气反应生成NO和气态水的热化学方程式为___ 。
方案Ⅱ:利用CO在催化剂条件下还原NO2:2NO2(g)+4CO(g) N2(g)+4CO2(g)∆H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2molNO2(g)和3molCO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:
N2(g)+4CO2(g)∆H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2molNO2(g)和3molCO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:

(2)①T1___ T2(填“>”或“<”);△H___ 0(填“>”或“<”),判定的依据是___ ;
②T1温度时,该反应的平衡常数K=___ (列出数字表达式即可);
③乙容器中,平衡时NO2的转化率为___ 。
方案Ⅲ:采用原电池原理的方法消除氮氧化物的污染,其工作原理如图所示:

(3)该电池的负极为___ 电极(填“A”或“B”)。负极发生的电极反应式为:___ 。
方案I.NH3—SCR法是工业上消除氮氧化物的常用方法。该法是利用氨的还原性,在一定条件下,将烟气中的NOx直接还原为N2,主要反应原理为:4NH3+4NO+O2
 4N2+6H2O。
4N2+6H2O。(1)已知有下列热化学方程式(a、b、c均大于0):
①4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(1)△H=-akJ/mol
4N2(g)+6H2O(1)△H=-akJ/mol②N2(g)+O2(g)
 2NO(g)△H=+bkJ/mol
2NO(g)△H=+bkJ/mol③H2O(g)
 H2O(1)△H=-ckJ/mol
H2O(1)△H=-ckJ/mol则氨气与氧气反应生成NO和气态水的热化学方程式为
方案Ⅱ:利用CO在催化剂条件下还原NO2:2NO2(g)+4CO(g)
 N2(g)+4CO2(g)∆H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2molNO2(g)和3molCO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:
N2(g)+4CO2(g)∆H。向容积均为2L的甲(温度为T1)、乙(温度为T2)两个恒容密闭容器中分别充入2molNO2(g)和3molCO(g)。反应过程中两容器内CO2的物质的量浓度随时间的变化关系如图所示:
(2)①T1
②T1温度时,该反应的平衡常数K=
③乙容器中,平衡时NO2的转化率为
方案Ⅲ:采用原电池原理的方法消除氮氧化物的污染,其工作原理如图所示:

(3)该电池的负极为
您最近一年使用:0次




