(1)已知部分弱酸的电离常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka = 1.8×10-5 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
①0.1 mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)
②常温下,pH相同的三种溶液A.CH3COONa B.NaCN C.Na2CO3,其物质的量浓度由大到小的顺序是
③室温下,—定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示。
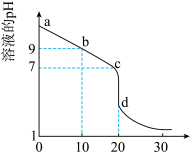
①d点所示的溶液中离子浓度由大到小的顺序依次为
②b点所示的溶液中c(NH3·H2O)-c(NH4+)=
③pH =10的氨水与pH =4的NH4C1溶液中,由水电离出的c(H+)之比为
相似题推荐
【推荐1】I.25℃时, 部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10⁻⁴mol·L⁻¹ | K₁=4.4×10-6mol•L⁻¹ K2=5.6×10-11mol•L-1 | 3.0×10-8mol·L⁻¹ |
请回答下列问题:
(1)同浓度的 CH3COOH、H2CO3、HClO 溶液的 pH 最大的是
(2)常温下 0.1mol/L的 CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是
A. c(H⁺) 

若该溶液升高温度,上述5种表达式的数据增大的是
(3)体积为 10mL pH=2 的醋酸溶液与一元酸 HX 溶液分别加水稀释至 1000mL, 稀释过程pH变化如图:则HX的电离平衡常数

(4)已知100℃时,水的离子积为1×10⁻¹²,该温度下测得某溶液 pH=7,该溶液显
Ⅱ. NaHCO3是生活中常用的膨松剂, 也可作为抑酸剂, 更是一种重要的化工原料。
(5)为探究NaHCO3溶液的酸碱性,某同学用
 的电离程度
的电离程度(6)向 2 支盛有 10mL1.0mol/LNaHCO3溶液的试管中,分别加入 3mL0.1mol/L的 CaCl2、FeCl3溶液, 现象如下表:
| 加入CaCl2溶液 | 加入FeCl3溶液 |
现象 | 有白色沉淀产生 | 有红褐色沉淀、气泡产生 |
说明 CaCl2溶液 的电离;请写出 FeCl3溶液和 NaHCO3溶液反应的离子方程式
的电离;请写出 FeCl3溶液和 NaHCO3溶液反应的离子方程式
(7)请写出 NaHCO3的电离方程式
(1)某温度(t℃)时,水的Kw=1×10-12,则该温度
(2)该温度下,c(H+)=1×10-7 mol·L-1的溶液呈
(3)25 ℃时,0.1 mol·L-1下列物质的溶液:①HCl、②H2SO4、③NaCl、④NaOH 、⑤Ba(OH)2,水电离出的c(H+)由大到小的关系是
(4)25 ℃时,pH=4的盐酸中水的电离程度
(1)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的电子式为
(2)B的一种氢化物的相对分子质量是 26,其分子中σ键和π键的数目之比为
(3)常温下,相同c(H+)的H2E溶液和硫酸溶液,稀释相同的倍数后的c(H+)前者与后者的关系
Ⅱ.(1)在某温度(T ℃)的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x 与y 关系如图所示。

该温度下,水的离子积为
(2)某温度下,纯水的c(H+)=2.0×10-7mol·L-1。在此温度下,某溶液中由水电离出的c(H+)=4.0×10-13 mol·L-1,则该溶液的pH可能是
 的含量及有效地开发利用
的含量及有效地开发利用 ,引起了全世界的普遍重视。将
,引起了全世界的普遍重视。将 转化为甲醇:CO2(g)+3H2(g)
转化为甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g),此研究对
CH3OH(g)+H2O(g),此研究对 的深度开发应用和构建生态文明社会具有重要的意义。
的深度开发应用和构建生态文明社会具有重要的意义。(1)在一恒温恒容密闭容器中充入1 mol
 和3 mol
和3 mol  进行上述反应。测得
进行上述反应。测得 (g)和
(g)和 (g)浓度随时间变化如图所示。
(g)浓度随时间变化如图所示。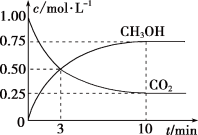
①0—10 min内,氢气的平均反应速率为
 (g)和2mol
(g)和2mol  (g),则平衡
(g),则平衡②一定温度下,若此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是
a.容器中压强不变 b.
 的体积分数不变 c.c(
的体积分数不变 c.c( )=3c(
)=3c( )
)d.容器中密度不变 e.2个C=O断裂的同时有3个H-H断裂
(2)若已知:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 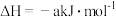
2H2(g)+O2(g)=2H2O(g)


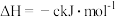
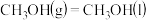
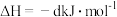
则表示
 (l)燃烧热的热化学方程式为
(l)燃烧热的热化学方程式为(3)如图,25℃时以甲醇燃料电池(电解质溶液为稀硫酸)为电源电解600 mL 一定浓度的NaCl溶液。
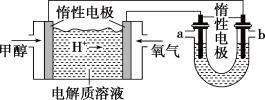
①U形管内发生的化学反应方程式为
②在电解一段时间后,NaCl溶液的pH变为12(假设电解前后NaCl溶液的体积不变),则理论上消耗甲醇的物质的量为
 气体,使所得溶液c(
气体,使所得溶液c( ):c(
):c( )=2:1,则此时溶液中的c(
)=2:1,则此时溶液中的c( )=
)=  。(室温下,H2CO3的
。(室温下,H2CO3的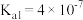 ;
;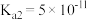 )。
)。
(1)NaClO溶液呈碱性,用离子方程式表示其原因
(2)5.2g乙炔(C2H2)气体完全燃烧生成二氧化碳和液态水,放出259.9kJ的热量,写出反应的热化学方程式
(3)H2O比H2S 的熔沸点高,原因是:
(4)25℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,若溶液中c(NH
 )= c(Cl-),则氨水的电离平衡常数
)= c(Cl-),则氨水的电离平衡常数(5)在25℃时,醋酸和亚硫酸的电离常数如下表:
| 醋酸 | 亚硫酸 |
| K=1.8×10-5 | K1=1.54×10-2 K2=1.02×10-7 |
⑴一定温度下,向0.1mol/LCH3COOH 溶液中加入少量CH3COONa 晶体时,下列说法正确的是
a.溶液的pH增大 b.CH3COOH的电离程度增大
c.溶液的导电能力减弱 d.溶液中c(OH-)·c(H+)不变
⑵25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中:
c(CH3COO-)/c(CH3COOH)=
⑶常温下,将20mL 0.1mol/L CH3COOH溶液 和20mL 0.1mol/LHNO2 溶液分别与 20mL 0.1mol/LNaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示,则表示CH3COOH溶液的曲线是

⑷体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示
 ,则HX的电离平衡常数
,则HX的电离平衡常数⑸25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7,则NH3·H2O的电离常数Kb =
I.部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | H2S | H2C2O4 | HClO |
| 电离平衡常数(25℃) | Ka=1.8×10−4 | Ka1=1.1×10−7 Ka2=1.3×10−13 | Ka1=5.6×10−2 Ka2=1.5×10−4 | Ka=4.0×10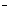 8 8 |
(1)用离子方程式说明Na2C2O4溶液显碱性的原因
(2)常温下,pH相同的HCOONa和NaClO溶液,
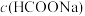
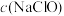 ,一定浓度的NaHS溶液pH
,一定浓度的NaHS溶液pH(3)已知Ksp(CaC2O4)=a。将0.03 mol∙L−1的CaCl2溶液与0.02 mol∙L−1的Na2C2O4溶液等体积混合,混合溶液中
 的浓度约为
的浓度约为Ⅱ.现用浓度为0.0100 mol/L酸性KMnO4溶液滴定未知浓度的草酸(H2C2O4),请回答下列问题:
(4)KMnO4标准溶液应装在
(5)记录数据如下:
| 滴定次数 | 待测溶液体积/mL | KMnO4溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.50 | 23.70 |
| 2 | 25.00 | 1.02 | 26.03 |
| 3 | 25.00 | 0.00 | 24.99 |
(6)下列操作会导致测定草酸浓度偏高的是___________。
| A.装高锰酸钾溶液的滴定管滴定前尖嘴中有气泡,滴定后气泡消失 |
| B.配制标准溶液时俯视刻度线 |
| C.未用标准液润洗滴定管 |
| D.滴定前盛放草酸溶液的锥形瓶用蒸馏水洗净后没有干燥 |
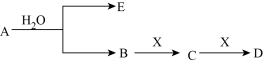
请回答下列问题:
(1)这种金属离子的离子结构示意图为
(2) 请写出A的电子式
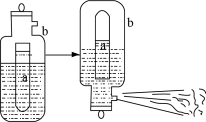
(3)D常用于一种泡沫灭火器,构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火。从液态试剂在灭火器中长久放置和快速灭火两个角度分析,则a中盛
(4)将一定量的气体X通入2 L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。

请回答:b点溶液中所含溶质的化学式为
(1)常温下,0.01mol/LNaOH溶液的

 倍后
倍后
 溶液中水电离产生的
溶液中水电离产生的 是
是 的
的 溶液中水电离产生的
溶液中水电离产生的 的
的(2)将等
 等体积的
等体积的 和
和 分别稀释
分别稀释 倍和
倍和 倍,稀释后两溶液的
倍,稀释后两溶液的 仍相等,则m
仍相等,则m ”、“
”、“ ”或“
”或“ ”)。
”)。(3)已知
 时,水的离子积为
时,水的离子积为 ,该温度下测得某溶液
,该温度下测得某溶液 ,该溶液显
,该溶液显 的
的 溶液
溶液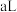 与
与 的
的 溶液
溶液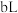 混合,若所得混合液
混合,若所得混合液 ,则a:b=
,则a:b= )常用作动力锂离子电池的正极材料,利用
)常用作动力锂离子电池的正极材料,利用 废料(还含铝、石墨等成分)回收锂、铁等元素的工艺流程如下。
废料(还含铝、石墨等成分)回收锂、铁等元素的工艺流程如下。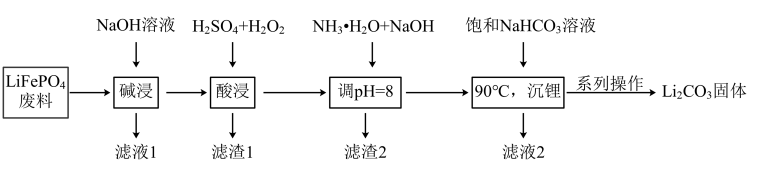
已知:
 不溶于NaOH溶液。
不溶于NaOH溶液。回答下列问题:
(1)
 中Fe元素的化合价为
中Fe元素的化合价为(2)“滤液1”含有的阴离子主要有:
 、
、(3)在“酸浸”中,磷元素转化为
 。
。①实际操作时,所加
 的量要比理论计算值多,可能原因是
的量要比理论计算值多,可能原因是②
 发生反应的离子方程式为
发生反应的离子方程式为(4)“滤渣2”的主要成分是
(5)碳酸锂溶解度(用溶液中溶质的物质的量分数
 表示)曲线如下图所示。
表示)曲线如下图所示。
①“沉锂”采用90℃的优点有
②308K时,碳酸锂溶解度为
(6)沉锂温度达到100℃时,碳酸锂沉淀率下降,可能的原因是
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25 ℃) | Ka=1.77 ×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(1)室温下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1 NaHCO3溶液的pH由大到小的关系为
(2)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为
(3)少量CO2通入到过量的NaClO溶液中发生反应的离子方程式
(4)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为
(Ⅱ)某小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。
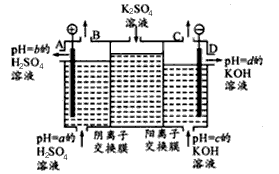
①该电解槽中通过阴离子交换膜的离子数
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为
③电解一段时间后,B出口与C出口产生气体的质量比为
I.常温下,浓度均为0.l mol·L-1的下列五种水溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
(2)根据表中数据判断,浓度均为0.01 mol·L-1的下列四种物质的溶液中,酸性最弱的是
A.HCN B.HClO C.H2CO3 D.CH3COOH
(3)要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为
II.已知水在25℃和95℃时,其电离平衡曲线如图所示:
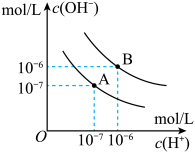
(1)95℃时水的电离平衡曲线应为
(2)25℃时,将pH=10的NaOH溶液与pH=6的盐酸溶液混合,若所得混合溶液的pH=7,则NaOH溶液与盐酸溶液的体积比为
(3)95℃时,若1体积pH=a的某强酸溶液与10x体积pH=b的某强碱溶液混合后溶液呈中性,则混合前,a与b之间应满足的关系是



