氨分子中的一个氢原子被甲基取代后,所得甲胺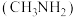 的性质与氨相似,
的性质与氨相似,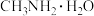 也是一元弱碱,25℃时,电离常数
也是一元弱碱,25℃时,电离常数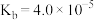 。现用
。现用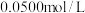 的稀硫酸滴定
的稀硫酸滴定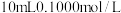 的甲胺溶液,溶液中
的甲胺溶液,溶液中 的负对数
的负对数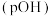 与所加稀硫酸的体积
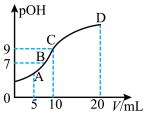
与所加稀硫酸的体积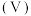 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
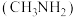 的性质与氨相似,
的性质与氨相似,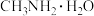 也是一元弱碱,25℃时,电离常数
也是一元弱碱,25℃时,电离常数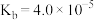 。现用
。现用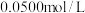 的稀硫酸滴定
的稀硫酸滴定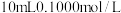 的甲胺溶液,溶液中
的甲胺溶液,溶液中 的负对数
的负对数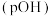 与所加稀硫酸的体积
与所加稀硫酸的体积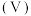 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
A.甲胺在水中的电离方程式为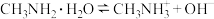 ,因此溶液呈碱性 ,因此溶液呈碱性 |
B.C点所在溶液中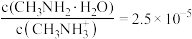 |
C.A、B、C、D四点对应的溶液中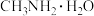 电离常数相等 电离常数相等 |
D.A点溶液中存在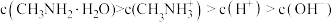 |
更新时间:2020/01/22 10:19:16
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】亚砷酸 在溶液中存在多种微粒形态,
在溶液中存在多种微粒形态, 溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液
溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液 关系如图所示。下列说法
关系如图所示。下列说法不正确 的是

 在溶液中存在多种微粒形态,
在溶液中存在多种微粒形态, 溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液
溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液 关系如图所示。下列说法
关系如图所示。下列说法
A. 的 的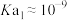 |
B.由图象信息可知 为三元弱酸 为三元弱酸 |
C.当 调至8~11时,主要反应的离子方程式为 调至8~11时,主要反应的离子方程式为 |
D. 时,溶液中 时,溶液中 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关电解质溶液的说法正确的是( )
| A.25℃,pH=2的CH3COOH溶液中,由水电离的OH-浓度为10-2mol·L-1 |
| B.向1L1mol·L-1的KOH热溶液中通入一定量Cl2,恰好完全反应生成氯化钾、次氯酸钾和氯酸钾(氯酸为强酸)的混合溶液:c(K+)+c(H+)=6c(ClO3-)+2c(ClO-)+c(HClO)+c(OH-) |
C.向AgCl、AgBr的溶液中加入少量AgNO3溶液,溶液中 一定不变 一定不变 |
D.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小 减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】HClO4、H2SO4、HCl和HNO3都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数,下列说法不正确的是
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | Ka1:6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A.温度会影响这四种酸在冰醋酸中的电离常数 |
| B.在冰醋酸中HClO4是这四种酸中最强的酸 |
C.在冰醋酸中H2SO4的电离方程式为H2SO4 2H++ 2H++ |
| D.这四种酸在冰醋酸中都没有完全电离,但仍属于强电解质 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】HA为一元弱酸,其电离是吸热过程,平衡体系中各成分的组成分数为 ,常温条件下,
,常温条件下, 与pH的关系如图所示,
与pH的关系如图所示, (其中X为HA或A-)。下列说法正确的是
(其中X为HA或A-)。下列说法正确的是

 ,常温条件下,
,常温条件下, 与pH的关系如图所示,
与pH的关系如图所示, (其中X为HA或A-)。下列说法正确的是
(其中X为HA或A-)。下列说法正确的是
A. 为HA的分布曲线 为HA的分布曲线 | B.若升高温度,a点移动趋势向左 |
| C.pH=5时,溶液中c(HA)>c(A-) | D.HA的电离常数的数量级为10-4 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】一甲胺(CH3NH2)在医药、农药、燃料、炸药等工业领域广泛应用,是一种弱碱,相同情况下比氨水碱性略强,与足量盐酸反应生成一甲胺盐酸盐CH3NH3Cl。下列说法正确的是
| A.CH3NH3Cl水溶液显酸性,pH一定比NH4Cl溶液大 |
| B.CH3NH3Cl属于弱电解质,在水溶液中存在电离平衡 |
| C.0.1mol/LCH3NH3Cl水溶液中有:c(H+)=c(CH3NH2)+c(OH-) |
| D.一甲胺是一元碱,常温下0.001mol/L一甲胺水溶液pH=11 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,分别向25mL0.3mol/LNa2CO3溶液和25mL0.3mol/LNaHCO3溶液中逐滴滴加0.3mol/L稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图所示,下列说法正确的是


| A.Y曲线为NaHCO3溶液的滴定曲线 |
| B.b、c两点溶液中水的电离程度:b>c |
C.a点溶液中:c(Na+)+c(H+)>c(OH-)+c(HCO )+2c(CO )+2c(CO ) ) |
D.c→d段离子方程式为:CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
您最近半年使用:0次

 时有关弱酸的电离平衡常数如下表,下列推断正确的是
时有关弱酸的电离平衡常数如下表,下列推断正确的是



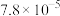
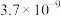
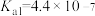 ;
;
 两种弱酸,其物质的量浓度:
两种弱酸,其物质的量浓度:

 溶液中加入足量
溶液中加入足量
 溶液中通入过量
溶液中通入过量 ,反应的离子方程式:
,反应的离子方程式: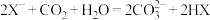
 是二元弱酸,常温下,用
是二元弱酸,常温下,用 溶液滴定草酸溶液,溶液中
溶液滴定草酸溶液,溶液中 或
或 与混合溶液
与混合溶液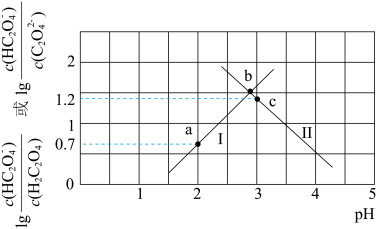



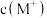 ,取若干点,根据推导情况进行数据处理,发现298K时,
,取若干点,根据推导情况进行数据处理,发现298K时, 可拟合成一条直线,如下图中实线所示。
可拟合成一条直线,如下图中实线所示。
 和
和
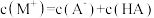
 与
与 之比为该函数的斜率,P点存在
之比为该函数的斜率,P点存在


