按要求回答下列问题:
(1)浓度为0.1mol/L醋酸钠溶液中质子守恒表达式为___________ ;
(2)等浓度的NaHCO3、Na2CO3混合溶液中的物料守恒表达式为____________ ;
(3) 浓度为0.1mol/LNa2CO3溶液电荷守恒表达式为__________ ;
(4) 泡沫灭火器灭火时发生反应的离子方程是______________ 。
(5)常温下,NaHSO3溶液中粒子浓度由大到小的顺序_________ 。
(6)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持在100 ℃的恒温。欲使混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为________ 。(已知100℃,KW=1.0×10-12)
(1)浓度为0.1mol/L醋酸钠溶液中质子守恒表达式为
(2)等浓度的NaHCO3、Na2CO3混合溶液中的物料守恒表达式为
(3) 浓度为0.1mol/LNa2CO3溶液电荷守恒表达式为
(4) 泡沫灭火器灭火时发生反应的离子方程是
(5)常温下,NaHSO3溶液中粒子浓度由大到小的顺序
(6)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持在100 ℃的恒温。欲使混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为
更新时间:2020-02-21 20:23:04
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】请回答下列问题:
(1)已知水存在如下平衡:H2O⇌H++OH- △H﹥0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_____。
(2)物质的量浓度相同的①NaOH②H2SO4③CH3COOH④NaCl⑤CH3COONa⑥(NH4)2SO4六种稀溶液中,水电离的OH-浓度由大到小的顺序_____ (填序号)
(3)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为_____ ,由水电离出的c(OH-)=_____ mol·L-1.
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为:Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式_____ 。MnO2可做超级电容器材料,用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是_____ 。
(5)已知:H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020mol·L-1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS—浓度为1.0×10-4mol·L-1时,Mn2+开始沉淀,则a=_____ 。[已知:Ksp(MnS)=1.4×10-15]
(1)已知水存在如下平衡:H2O⇌H++OH- △H﹥0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_____。
| A.向水中加入NaHSO4固体 |
| B.向水中加NaHCO3固体 |
| C.加热至100℃[其中c(H+)=1×10-6mol/L] |
| D.向水中加入NH4Cl固体 |
(3)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为:Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式
(5)已知:H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020mol·L-1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS—浓度为1.0×10-4mol·L-1时,Mn2+开始沉淀,则a=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】25℃,几种物质的pH和浓度如下表所示。
回答下列问题:
(1) c1_____ (填“>”“<”或“=”) c2。
(2)溶液中水的电离程度②_____ (填“>”“<”或“=”)③。
(3)分别加水稀释10倍,稀释后四种溶液的pH由大到小的顺序为________ (填序号)。
(4) ①溶液与④溶液等体积混合,溶液的pH_______ (填“>"'<"或“ =”, 下 同 )7,混合溶液中c(NH4+)____ c(Cl-)。
| 序号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| 浓度 | c1 | c2 | c3 | c4 |
回答下列问题:
(1) c1
(2)溶液中水的电离程度②
(3)分别加水稀释10倍,稀释后四种溶液的pH由大到小的顺序为
(4) ①溶液与④溶液等体积混合,溶液的pH
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】醋酸和碳酸都是常见的酸。
(1)碳酸的电离方程式为__________________________________________________ 。
(2)向0.1 mol·L-1 CH3COOH溶液中加水稀释,c(CH3COO-) / c(CH3COOH)的比值将______ (填“变大”、“不变”或“变小”)。
(3)下列事实一定能说明CH3COOH是弱电解质的是____________ (填字母)。
A. 相同温度下,浓度均为1 mol·L-1的盐酸和醋酸的导电性对比:盐酸>醋酸
B. 1 mol·L-1 CH3COOH溶液能使紫色石蕊试液变红
C. 25℃时,1 mol·L-1 CH3COOH溶液的pH约为2
D. 10 mL 1mol·L-1的CH3COOH溶液恰好与10 mL 1mol·L-1 NaOH溶液完全反应
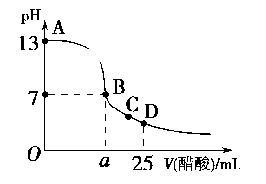
(4)常温下,在25 mL氢氧化钠溶液中逐滴加入0.2 mol/L醋酸溶液,滴定曲线如下图所示。
①该氢氧化钠溶液的物质的量浓度为________ mol·L-1
②在B点,a________ 12.5 mL(填“大于”、“小于”或“等于”)。醋酸和NaOH恰好完全反应后溶液呈______ (填“酸”或“碱”)性,原因是______________________ (用离子方程式表示),此时溶液中各离子浓度大小为__________________________ 。
③A、B、C、D几点中,水的电离程度最大的是____________ 。
(1)碳酸的电离方程式为
(2)向0.1 mol·L-1 CH3COOH溶液中加水稀释,c(CH3COO-) / c(CH3COOH)的比值将
(3)下列事实一定能说明CH3COOH是弱电解质的是
A. 相同温度下,浓度均为1 mol·L-1的盐酸和醋酸的导电性对比:盐酸>醋酸
B. 1 mol·L-1 CH3COOH溶液能使紫色石蕊试液变红
C. 25℃时,1 mol·L-1 CH3COOH溶液的pH约为2
D. 10 mL 1mol·L-1的CH3COOH溶液恰好与10 mL 1mol·L-1 NaOH溶液完全反应
(4)常温下,在25 mL氢氧化钠溶液中逐滴加入0.2 mol/L醋酸溶液,滴定曲线如下图所示。
①该氢氧化钠溶液的物质的量浓度为
②在B点,a
③A、B、C、D几点中,水的电离程度最大的是

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4=H++HSO ,HSO
,HSO ⇌H+ + SO
⇌H+ + SO 。
。
请回答下列有关问题:
(1)Na2SO4溶液呈______ (填“弱酸性”、“中性”或“弱碱性”),其理由是_______ (用离子方程式表示)。
(2)H2SO4溶液与BaC12溶液反应的离子方程式为_______ 。
(3)在0.l0mol·L-1的Na2SO4溶液中,下列离子浓度关系正确的是_______ (填写编号)。
A.c(Na+)=c(SO )+c(HSO
)+c(HSO )+c(H2SO4) B.c(OH-)=c(HSO
)+c(H2SO4) B.c(OH-)=c(HSO )+c(H+)
)+c(H+)
C.c( Na+)+c(H+)=c(OH-)+c(HSO )+2c(SO
)+2c(SO ) D.c( Na+)=2c(SO
) D.c( Na+)=2c(SO )+2c(HSO
)+2c(HSO )
)
(4)若25℃时,0.10 mol·L-1的NaHSO4溶液中c( SO )=0. 029 mol·L-1,则0. 10 mol·L-1的H2SO4溶液中c( SO
)=0. 029 mol·L-1,则0. 10 mol·L-1的H2SO4溶液中c( SO )
)_______ 0.029 mol·L-1(填“<’,、“>”或“=”),其理由是_______ 。
(5)若25℃时,0.10 mol·L-1H2SO4溶液的pH=-lg0.11,则0.10 mol·L-1的H2SO4溶液中c(SO )=
)=_______ mol·L-1
 ,HSO
,HSO ⇌H+ + SO
⇌H+ + SO 。
。请回答下列有关问题:
(1)Na2SO4溶液呈
(2)H2SO4溶液与BaC12溶液反应的离子方程式为
(3)在0.l0mol·L-1的Na2SO4溶液中,下列离子浓度关系正确的是
A.c(Na+)=c(SO
 )+c(HSO
)+c(HSO )+c(H2SO4) B.c(OH-)=c(HSO
)+c(H2SO4) B.c(OH-)=c(HSO )+c(H+)
)+c(H+)C.c( Na+)+c(H+)=c(OH-)+c(HSO
 )+2c(SO
)+2c(SO ) D.c( Na+)=2c(SO
) D.c( Na+)=2c(SO )+2c(HSO
)+2c(HSO )
)(4)若25℃时,0.10 mol·L-1的NaHSO4溶液中c( SO
 )=0. 029 mol·L-1,则0. 10 mol·L-1的H2SO4溶液中c( SO
)=0. 029 mol·L-1,则0. 10 mol·L-1的H2SO4溶液中c( SO )
)(5)若25℃时,0.10 mol·L-1H2SO4溶液的pH=-lg0.11,则0.10 mol·L-1的H2SO4溶液中c(SO
 )=
)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】某品牌苏打水的配料中含食盐、碳酸氢钠、碳酸和氯化钙等。某学习小组在分析该品牌苏打水的配料之后,设计下列实验,探究氯化钙溶液与小苏打溶液混合后是否发生反应。
实验1:25℃,测定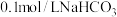 溶液的pH为8.3。
溶液的pH为8.3。
实验2:将 溶液与
溶液与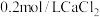 溶液等体积混合,产生白色沉淀,一段时间后有气泡产生。
溶液等体积混合,产生白色沉淀,一段时间后有气泡产生。
实验3:将 通入模拟苏打水(含
通入模拟苏打水(含 的
的 溶液)中,pH和
溶液)中,pH和 随通入
随通入 的变化关系如图所示。
的变化关系如图所示。

查阅资料:①25℃时, 、
、 ,
,
②25℃时, 的自偶电离:
的自偶电离: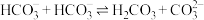

回答下列问题:
(1)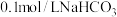 溶液中,
溶液中,
_______ ,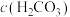
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(2)从平衡移动角度解释“实验2”生成气体的原因是_______ 。
(3)25℃,x=_______ ;忽略溶液中其他平衡,请用 自偶电离平衡计算“实验2”中两溶液刚混合时,
自偶电离平衡计算“实验2”中两溶液刚混合时,
_______ [溶液中 ,计算时,体系中
,计算时,体系中 的浓度用碳元素的总浓度代替]。
的浓度用碳元素的总浓度代替]。
(4)bc段 增大的原因是
增大的原因是_______ 。
实验1:25℃,测定
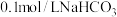 溶液的pH为8.3。
溶液的pH为8.3。实验2:将
 溶液与
溶液与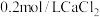 溶液等体积混合,产生白色沉淀,一段时间后有气泡产生。
溶液等体积混合,产生白色沉淀,一段时间后有气泡产生。实验3:将
 通入模拟苏打水(含
通入模拟苏打水(含 的
的 溶液)中,pH和
溶液)中,pH和 随通入
随通入 的变化关系如图所示。
的变化关系如图所示。
查阅资料:①25℃时,
 、
、 ,
,
②25℃时,
 的自偶电离:
的自偶电离: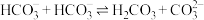

回答下列问题:
(1)
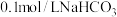 溶液中,
溶液中,
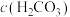
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(2)从平衡移动角度解释“实验2”生成气体的原因是
(3)25℃,x=
 自偶电离平衡计算“实验2”中两溶液刚混合时,
自偶电离平衡计算“实验2”中两溶液刚混合时,
 ,计算时,体系中
,计算时,体系中 的浓度用碳元素的总浓度代替]。
的浓度用碳元素的总浓度代替]。(4)bc段
 增大的原因是
增大的原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】完成下列各问题:
(1)①泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,其反应的离子方程式为:__________ ;
②TiCl4水解生成TiO2·xH2O的化学方程式__________ ;
③酸性高锰酸钾溶液与草酸溶液反应的化学方程式____________ ;
④硫代硫酸钠溶液与稀硫酸反应的化学方程式____________ ;
(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出
①电荷数守恒_________ ;
②物料守恒___________ ;
③质子守恒___________ ;
④下列粒子浓度由大到小的顺序为c(Na+)、c(HCO3-)、c(CO32-),c(H2CO3)、c(OH-)_________ 。
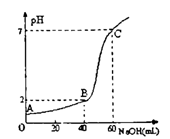
(3)常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示。所用NaOH溶液浓度为____________ 。
(1)①泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,其反应的离子方程式为:
②TiCl4水解生成TiO2·xH2O的化学方程式
③酸性高锰酸钾溶液与草酸溶液反应的化学方程式
④硫代硫酸钠溶液与稀硫酸反应的化学方程式
(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出
①电荷数守恒
②物料守恒
③质子守恒
④下列粒子浓度由大到小的顺序为c(Na+)、c(HCO3-)、c(CO32-),c(H2CO3)、c(OH-)
(3)常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示。所用NaOH溶液浓度为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】25℃时,有浓度均为0.1mol•L-1的下列4种溶液:
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④Na2CO3溶液
(1)H3PO2是一元中强酸,具有较强的还原性。写出其电离方程式______ 。
(2)上述4种溶液pH最小的是______ (填序号),其中②由水电离的H+浓度为_____ mol•L-1。
(3)①中各离子浓度由大到小的顺序是______ 。
(4)现有浓度为0.02mol/L的HCN与0.01moL/LNaOH等体积混合后(忽略体积变化),测得c(Na+)>c(CN-),下列关系正确的是______ 。(填标号)
(5)25℃时,测得HCN和NaCN的混合溶液的pH=11,则 约为
约为_____ (计算结果保留两位小数)。向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:_____ 。
(6)已知t℃时,Kw=1×10-13,则t℃_____ 25℃(填“>”、“<”或“=”)。在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 =
=_____ 。
(7)25℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH值pH1与强碱的pH值pH2之间应满足的关系是_____ 。
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④Na2CO3溶液
| HCN | H2CO3 | CH3COOH |
| Ka=4.9×10-10 | Ka1=4.4×10-7 Ka2=4.7×10-11 | Ka=1.75×10-5 |
(2)上述4种溶液pH最小的是
(3)①中各离子浓度由大到小的顺序是
(4)现有浓度为0.02mol/L的HCN与0.01moL/LNaOH等体积混合后(忽略体积变化),测得c(Na+)>c(CN-),下列关系正确的是
| A.c(H+)>c(OH-) | B.c(H+)<c(OH-) |
| C.c(H+)+c(HCN)=c(OH-) | D.c(HCN)+c(CN-)=0.01mol/L |
 约为
约为(6)已知t℃时,Kw=1×10-13,则t℃
 =
=(7)25℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH值pH1与强碱的pH值pH2之间应满足的关系是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】亚磷酸及其钠盐可用于农药中间体以及有机磷水处理剂的原料。
I.已知亚磷酸(H3PO3)是二元弱酸,常温下向1L0.5mol•L-1H3PO3溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示:

(1)b点c(Na+)___ 2c(HPO )+c(H2PO
)+c(H2PO )(填“>”、“<”或“=”);反应H3PO3+HPO
)(填“>”、“<”或“=”);反应H3PO3+HPO
 2H2PO
2H2PO 的平衡常数的数值为
的平衡常数的数值为____ 。
II.用白磷合成亚磷酸某种钠盐X的流程如图:

回答下列问题:
(2)“制取NaH2PO2”过程中氧化剂与还原剂的物质的量之比为___ 。
(3)“合成H3PO3”发生反应的化学方程式为___ 。
(4)“减压蒸馋”过程,I-回收率为95%,则剩余固体的主要成分钠盐X为___ 。(填化学式)。
I.已知亚磷酸(H3PO3)是二元弱酸,常温下向1L0.5mol•L-1H3PO3溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示:

(1)b点c(Na+)
 )+c(H2PO
)+c(H2PO )(填“>”、“<”或“=”);反应H3PO3+HPO
)(填“>”、“<”或“=”);反应H3PO3+HPO
 2H2PO
2H2PO 的平衡常数的数值为
的平衡常数的数值为II.用白磷合成亚磷酸某种钠盐X的流程如图:

回答下列问题:
(2)“制取NaH2PO2”过程中氧化剂与还原剂的物质的量之比为
(3)“合成H3PO3”发生反应的化学方程式为
(4)“减压蒸馋”过程,I-回收率为95%,则剩余固体的主要成分钠盐X为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】某二元酸(H2A)在水中的电离方程式是H2A=H++HA-,HA- H++A2-。
H++A2-。
(1)Na2A溶液显_________ (填“酸性”“中性”或“碱性”)。理由是__________ (用离子方程式表示)。
(2)已知0.1mol/L的NaHA溶液的pH=2,则0.1mol/L的H2A溶液中c(H+ )_______ (填“<”“>”或“=”)0.11mol/L。
(3)在0.1mol/L的Na2A溶液中,下列微粒浓度关系式不正确的是__ (填字母)。
A.c(A2- )+c(HA-)=0.1mol/L
B.c(OH-)=c(H+) +c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)
D.c(Na+)=2c(A2-)+2c(HA-)
(4)若向0.1mol/L的H2A溶液中加入等体积等浓度的NaOH溶液,则溶液中各离子浓度由大到小的顺序为__________________ 。
 H++A2-。
H++A2-。(1)Na2A溶液显
(2)已知0.1mol/L的NaHA溶液的pH=2,则0.1mol/L的H2A溶液中c(H+ )
(3)在0.1mol/L的Na2A溶液中,下列微粒浓度关系式不正确的是
A.c(A2- )+c(HA-)=0.1mol/L
B.c(OH-)=c(H+) +c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)
D.c(Na+)=2c(A2-)+2c(HA-)
(4)若向0.1mol/L的H2A溶液中加入等体积等浓度的NaOH溶液,则溶液中各离子浓度由大到小的顺序为
您最近一年使用:0次



