在密闭容器中发生如下反应:aA(g)+bB(g) cC(g)。其他条件不变时,改变某一条件对上述反应的影响,得到下列图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。下列分析正确的是
cC(g)。其他条件不变时,改变某一条件对上述反应的影响,得到下列图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。下列分析正确的是
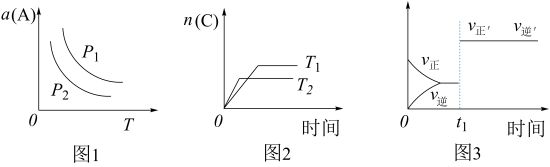
 cC(g)。其他条件不变时,改变某一条件对上述反应的影响,得到下列图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。下列分析正确的是
cC(g)。其他条件不变时,改变某一条件对上述反应的影响,得到下列图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。下列分析正确的是
| A.如图1反应:若p1>p2,则该反应只能在高温下自发进行 |
| B.如图2反应:此反应的△H<0,且T1>T2 |
| C.如图3反应:表示t1时刻可能是使用催化剂对反应速率的影响 |
| D.如图3反应:表示t1时刻增大B的浓度对反应速率的影响 |
更新时间:2020-02-28 10:59:17
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:
①v1<v2 ②v1<v3 ③c2<2c1 ④c2>2c3 ⑤p2>2p3 ⑥p2<2p1 ⑦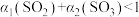 ⑧
⑧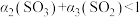 ⑨
⑨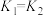 ⑩
⑩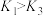
以上说法正确的有
 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2mol 、1mol 、1mol | 4mol | 2mol 、1mol 、1mol |
平衡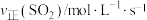 | v1 | v2 | v3 |
平衡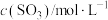 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
物质的平衡转化率 | 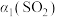 | 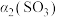 | 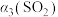 |
| 平衡常数K | 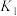 | 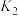 |  |
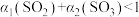 ⑧
⑧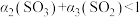 ⑨
⑨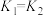 ⑩
⑩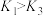
以上说法正确的有
| A.6 | B.7 | C.8 | D.9 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向一恒容密闭容器中加入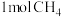 和一定量的
和一定量的 ,发生反应
,发生反应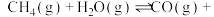
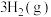 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法正确的是
随温度的变化曲线如图所示。下列说法正确的是

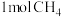 和一定量的
和一定量的 ,发生反应
,发生反应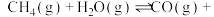
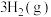 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法正确的是
随温度的变化曲线如图所示。下列说法正确的是
A. |
B.反应速率: |
C.点a、b、c对应的平衡常数: |
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态 ,当容器内压强不变时,反应达到平衡状态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列图示与对应的叙述相符的是
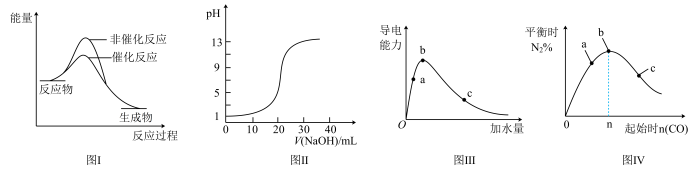

| A.图I表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图Ⅱ表示常温下,0.100mol/LNaOH溶液滴定20.00mL、0.0100mol/LHCl溶液所得到的滴定曲线 |
| C.图Ⅲ表示一定质量的冰醋酸加水稀释过程中,醋酸溶液电离程度:c < a < b |
D.图Ⅳ表示反应4CO(g)+2NO2(g)  N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c > b > a N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c > b > a |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】向一恒容密闭容器中加入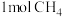 和一定量的
和一定量的 ,发生反应:
,发生反应: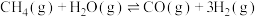 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法不正确的是
随温度的变化曲线如图所示。下列说法不正确的是

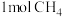 和一定量的
和一定量的 ,发生反应:
,发生反应: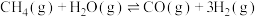 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法不正确的是
随温度的变化曲线如图所示。下列说法不正确的是
A.平衡时 的浓度: 的浓度: |
B.b、c两点的正反应速率: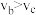 |
| C.此反应在任意温度下都可自发进行 |
| D.当容器内气体的平均相对分子质量不变时,反应达平衡状态 |
您最近一年使用:0次
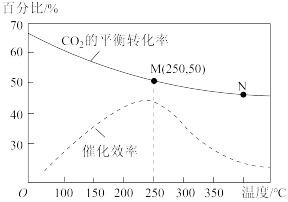
【推荐1】在1L恒容密闭容器中充入体积比为3:1的H2和CO2,二者在催化剂、加热条件下反应可以合成乙烯:6H2+2CO2 CH2=CH2+4H2O(g)△H<0,不同温度对CO2的平衡转化率及催化剂的催化效率的影响如图所示。下列有关说法正确的是
CH2=CH2+4H2O(g)△H<0,不同温度对CO2的平衡转化率及催化剂的催化效率的影响如图所示。下列有关说法正确的是
 CH2=CH2+4H2O(g)△H<0,不同温度对CO2的平衡转化率及催化剂的催化效率的影响如图所示。下列有关说法正确的是
CH2=CH2+4H2O(g)△H<0,不同温度对CO2的平衡转化率及催化剂的催化效率的影响如图所示。下列有关说法正确的是
| A.N点的反应速率一定比M点大 |
| B.M点时,产物乙烯的体积分数约为7.7% |
| C.其他条件相同时,N点的平衡常数比M点的大 |
| D.N点对应温度下的催化剂的催化效率比M点对应温度下的高 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
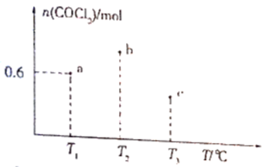
【推荐2】在体积均为2L的a、b、e三个恒容密闭容器中分别充入1molCO(g)和1molCl2(g),发生反应CO(g)+Cl2(g) COCl2(g),若三个容器的反应温度分别为T1℃、T2℃、T3℃且保持恒定不变,测得反应均进行到2min时,COCl2(g)的物质的量如图所示。下列说法正确的是
COCl2(g),若三个容器的反应温度分别为T1℃、T2℃、T3℃且保持恒定不变,测得反应均进行到2min时,COCl2(g)的物质的量如图所示。下列说法正确的是
 COCl2(g),若三个容器的反应温度分别为T1℃、T2℃、T3℃且保持恒定不变,测得反应均进行到2min时,COCl2(g)的物质的量如图所示。下列说法正确的是
COCl2(g),若三个容器的反应温度分别为T1℃、T2℃、T3℃且保持恒定不变,测得反应均进行到2min时,COCl2(g)的物质的量如图所示。下列说法正确的是
| A.a容器中,0~2min时平均反应速率v(COCl2)=0.3mol.·L-1·min-1 |
| B.反应进行到2min时,三个容器中一定达到化学平衡状态的是b容器 |
| C.当三个容器内的反应都达到化学平衡时,Cl2转化率最大的是a容器 |
| D.若开始时向b容器中充入CO(g)、Cl2(g)、COCl2(g)各0.5mol,则开始时v正<v逆 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在某容积一定的密闭容器中,有下列可逆反应xA(g)+B(g)⇌2C(g),反应曲线(T表示温度,P表示压强,C% 表示C的体积分数)如图所示,试判断对图的说法中一定正确的是( )
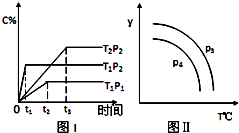

| A.该反应是吸热反应 |
| B.x=2 |
| C.P3<P4,y轴可表示混合气体的相对分子质量 |
| D.P3>P4,y轴可表示C物质在平衡体积中的百分含量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
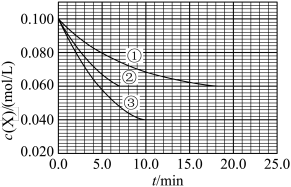
【推荐1】碳热还原制备氮化铝的总反应化学方程式为:Al2O3(s)+3C(s)+N2(g) 2AlN(s)+3CO(g)。在温度、容积恒定的反应体系中,CO浓度随时间的变化关系如图曲线甲所示。下列说法不正确的是
2AlN(s)+3CO(g)。在温度、容积恒定的反应体系中,CO浓度随时间的变化关系如图曲线甲所示。下列说法不正确的是

 2AlN(s)+3CO(g)。在温度、容积恒定的反应体系中,CO浓度随时间的变化关系如图曲线甲所示。下列说法不正确的是
2AlN(s)+3CO(g)。在温度、容积恒定的反应体系中,CO浓度随时间的变化关系如图曲线甲所示。下列说法不正确的是
| A.在不同时刻都存在关系:3v(N2)= v(CO) |
| B.c点切线的斜率表示该化学反应在t时刻的瞬时速率 |
| C.从a、b两点坐标可求得从a到b时间间隔内该化学反应的平均速率 |
| D.维持温度、容积不变,若减少N2的物质的量进行反应,曲线甲将转变为曲线乙 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】氨是最基本的化工原料之一。工业合成氨的反应为 3H2(g)+N2(g) 2NH3(g) ∆H<0,在一定条件下,将H2(g)和N2(g)充入恒容密闭容器中,反应过程中各物质的物质的量浓度随时间的变化如图所示∶
2NH3(g) ∆H<0,在一定条件下,将H2(g)和N2(g)充入恒容密闭容器中,反应过程中各物质的物质的量浓度随时间的变化如图所示∶

下列叙述正确的是
 2NH3(g) ∆H<0,在一定条件下,将H2(g)和N2(g)充入恒容密闭容器中,反应过程中各物质的物质的量浓度随时间的变化如图所示∶
2NH3(g) ∆H<0,在一定条件下,将H2(g)和N2(g)充入恒容密闭容器中,反应过程中各物质的物质的量浓度随时间的变化如图所示∶
下列叙述正确的是
| A.图中两次平衡时反应的化学平衡常数不相等 |
| B.第10min时改变的一个条件为加压或加入催化剂 |
| C.可用勒夏特列原理来解释工业合成氨需在高温下进行 |
| D.25至30min时间段,反应的平均速率v(H2)=0.015 mol/(L·min) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】固定容积为2 L的密闭容器中发生反应xA(g)+yB(g) zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是
zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是

 zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是
zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系。结合图象判断,下列结论正确的是
| A.200℃时,反应从开始到平衡的平均速率v(A)=0.08 mol•L-1•min-1 |
| B.200℃时,若在第6 min再向体系中充入1 mol He,此时v(正)>v(逆) |
C.若0~5 min内容器与外界的热交换总量为m kJ,则该反应的热化学方程式可表示为:2A(g)+B(g) C(g) ΔH= +5m kJ/mol C(g) ΔH= +5m kJ/mol |
| D.200℃时,平衡后再充入2 mol C,则再次达到平衡时,C的体积分数等于0.25 |
您最近一年使用:0次

 过程中零耗能是该方法的一个重要优点,原理如下:
过程中零耗能是该方法的一个重要优点,原理如下: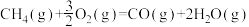
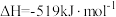
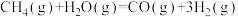

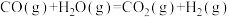

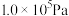 、按
、按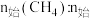 (空气)
(空气)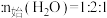 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的选择性[CO的选择性
的选择性[CO的选择性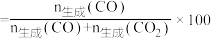 %]与温度的关系如题图所示。下列说法
%]与温度的关系如题图所示。下列说法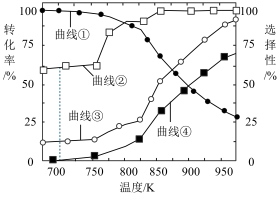
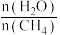 的值可提高
的值可提高

