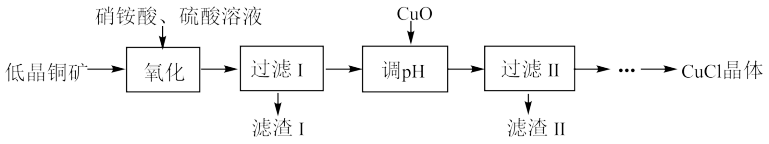
已知:①CuCl微溶于水,不溶于乙醇,露置于潮湿的空气中易被氧化。②氧化时,NH4NO3中N元素主要被还原为最低价态,少部分被还原为NO。
(1)“氧化”阶段的温度需控制在65℃,其适宜的加热方式为
(2)在实验室进行实验时,“氧化"阶段反应可在如图所示装置中进行。
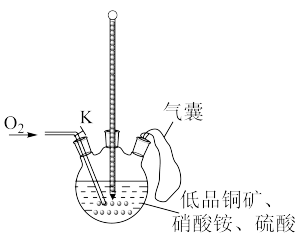
①实验开始时,温度计显示反应液温度低于室温,主要原因是
②通入氧气的目的是
(3)利用惰性电极电解CuCl2溶液也可制取CuCl,阴极电极反应式为
(4)已知常温下CuCl在水溶液中Ksp=1.2×10-6,工艺流程最后一步析出CuCl晶体后的溶液中,如果c(Cl-)=4.0 mol·L-1,则c(Cu+)=
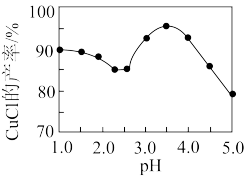
(5)已知pH对CuCl沉淀率的影响如图所示,请设计从“过滤II”所得的滤液中获取CuCl的实验方案;
相似题推荐
【推荐1】钪( )是一种功能强大的稀土金属,广泛用于航天、激光、导弹等尖端科学领域。钛铁矿主要成分为钛酸亚铁
)是一种功能强大的稀土金属,广泛用于航天、激光、导弹等尖端科学领域。钛铁矿主要成分为钛酸亚铁 ,还含有少量
,还含有少量 、
、 、
、 等杂质,从钛铁矿中提取
等杂质,从钛铁矿中提取 的流程如下图:
的流程如下图:
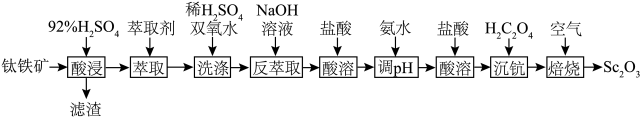
回答下列问题:
(1)“滤渣”的主要成分是
(2)“酸浸”后,钛主要以
 的形式存在于溶液中,
的形式存在于溶液中, 在一定条件下可完全水解生成
在一定条件下可完全水解生成 ,写出
,写出 水解的离子方程式:
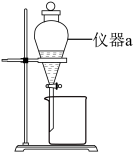
水解的离子方程式:(3)实验室萃取装置如下图所示,仪器a的名称为
(4)25℃时“调
 ”先加氨水调节
”先加氨水调节 ,过滤除去
,过滤除去 。再向滤液中加入氨水调节
。再向滤液中加入氨水调节 ,已知
,已知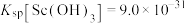 ,此时滤液中
,此时滤液中 的浓度为
的浓度为 。写出检验含
。写出检验含 滤液中是否含
滤液中是否含 的方法:
的方法:(5)“沉钪”时用到草酸,已知草酸的
 ;
; ,则在25℃时,
,则在25℃时, 的草酸溶液中
的草酸溶液中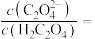
(6)
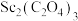 在空气中“焙烧”时生成
在空气中“焙烧”时生成 ,该反应的化学方程式为
,该反应的化学方程式为【推荐2】工业上用低品铜矿(主要含CuS、FeO等)制备氯化亚铜(CuCl)的一种工艺流程如图:
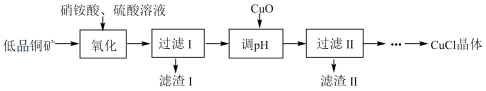
已知:①CuCl微溶于水,不溶于乙醇,露置于潮湿的空气中易被氧化。
②“氧化”时,NO 中N元素主要被还原为最低价态,少部分被还原为NO。
中N元素主要被还原为最低价态,少部分被还原为NO。
(1)①“氧化”阶段的温度需控制在65℃,其适宜的加热方式为
②该步骤中FeO被NH4NO3氧化,其主要反应的离子方程式:
(2)在实验室进行实验时,“氧化”阶段反应可在如图所示装置中进行:
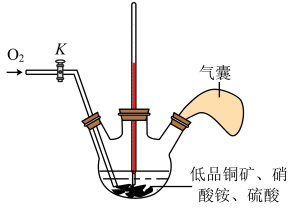
①实验开始时,温度计显示反应液温度低于室温,主要原因是
②通入氧气的目的是
③为便于观察和控制产生O2的速率,制备氧气的装置最好选用
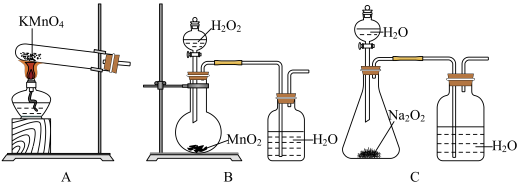
(3)已知常温下CuCl在水溶液中Ksp=1.2×10-6,工艺流程最后一步析出CuCl晶体后的溶液中,如果c(Cl-)=4.0mol·L-1,则c(Cu+)=
(4)已知pH对CuCl沉淀率的影响如图所示,请设计从“过滤II”所得的滤液中获取CuCl的实验方案:
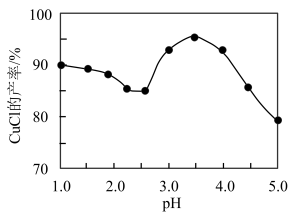
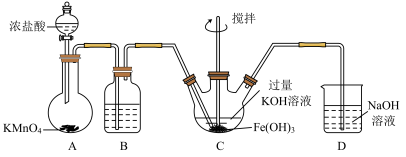
资料:K2FeO4可溶于水、微溶于浓KOH溶液,具有强氧化性,在碱性溶液中较稳定;在酸性或中性溶液中快速产生O2。
(1) K2FeO4中铁元素的化合价
(2)装置B中的试剂为
(3)装置C中制备K2FeO4时,发生反应的化学方程式为
(4)高铁酸钾与水反应其中一种产物为Fe(OH)3 (胶体),则离子方程式为
(5)制备 K2FeO4可以采用干式氧化法,初始反应为

 ,该反应中每消耗6molNa2O2时转移电子数为
,该反应中每消耗6molNa2O2时转移电子数为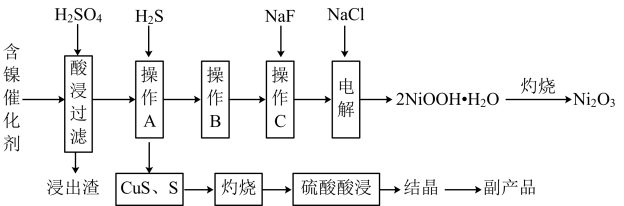
已知:①常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
请回答下列问题:
(1)浸出渣的成分是:
(2)“操作B”的过程是,先在40~50℃加入H2O2,其作用是
(3)电解沉镍的过程中,产物2NiOOH·H2O在电解池的
(4)操作C可除去溶液中的Ca2+,若控制溶液中F-浓度为3.0×10-3mol·L-1,则溶液中
 =
= 、CuO、
、CuO、 、MnO等)为原料可生产制备纳米ZnO的流程如图所示。
、MnO等)为原料可生产制备纳米ZnO的流程如图所示。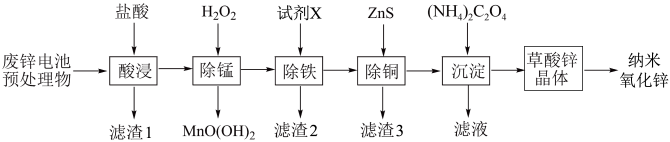
已知:ZnS和Cus的Ksp分别为
 、
、 。
。(1)“酸浸”过程中,为了提高浸取效率,可采取的措施有
(2)滤渣1的主要成分是
(3)“除锰”过程中
 的作用是
的作用是(4)“除铁”过程中加入试剂X可能是___________(填字母序号)。
A. | B. | C.NaOH | D. |
 ,常温下,该反应的平衡常数为
,常温下,该反应的平衡常数为(6)在通风橱中,将草酸锌晶体置于陶瓷仪器
(7)草酸锌晶体(
 )加热过程中固体质量随温度的变化情况如图所示。图中A转化为B的过程中发生反应的化学方程式为
)加热过程中固体质量随温度的变化情况如图所示。图中A转化为B的过程中发生反应的化学方程式为
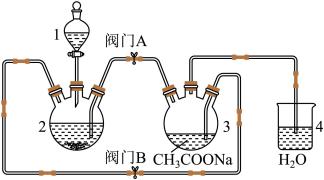
| 资料卡: ①醋酸亚铬晶体[[Cr(CH3COO)2]2•2H2O;深红色晶体,不溶于冷水,是常用的氧气吸收剂。 ②Cr2+不稳定,极易被氧气氧化,不与锌反应。 ③部分相关的化学反应: 2CrCl3+Zn═2CrCl2+ZnCl2 2Cr2++4CH3COO-+2H2O═[Cr(CH3COO)2]2•2H2O ④Ksp[Cr(OH)3]=6.3×10-31, 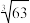 ≈4,lg2≈0.3 ≈4,lg2≈0.3 |
(l)仪器1的名称是
(2)实验时先往仪器2中加盐酸,一段时间后再加CrCl3溶液,目的是
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭阀门
(4)本实验中锌粒要过量,其原因除了使产生的H2将CrCl2 溶液压入装置3与CH3COONa溶液反应外,另一个作用是
(5)铬的离子会污染水资源。常温下要除去上述实验中多余的Cr2+,①先向废液中通入足量的
(1)已知:
| 化学键 | C-H | C=O | O=O | H-O |
 | a | b | c | d |
则
 的反应热
的反应热
 。
。(2)燃料电池具有较高的发电效率,因而受到重视。如图1为甲烷燃料电池(电解质溶液为稀硫酸,X、Y均为Pt电极)的原理示意图,该电池的正极反应为
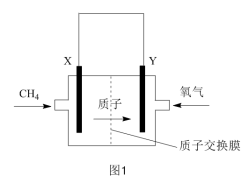
(3)利用上述燃料电池作电源,按图2所示装置进行电解,A、B、C、D均为铂电极。
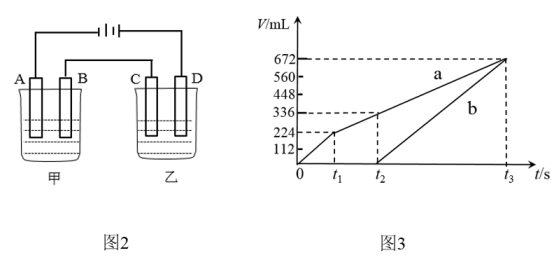
甲槽中有200mL一定浓度的NaCl与
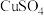 的混合溶液,理论上两极所得气体(a和b)的体积随时间变化的关系如图3所示(气体体积已换算成标准状况下的体积)。(注意:电解前后溶液的体积变化忽略不计)
的混合溶液,理论上两极所得气体(a和b)的体积随时间变化的关系如图3所示(气体体积已换算成标准状况下的体积)。(注意:电解前后溶液的体积变化忽略不计)①原混合溶液中NaCl的物质的量浓度为
②
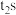 时所得溶液的pH=
时所得溶液的pH=③工业上用电解饱和食盐水的方法制烧碱、氯气。乙槽中有足量NaCl溶液。则阳极的电极反应式为
(1)标准摩尔生成焓是指在25℃和101kPa,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa
时下列反应:
①2C2H6(g)+7O2(g)=4CO2(g) +6H2O(l) △H=-3116 kJ·mol-1
②C(石墨,s)+O2(g) =CO2(g) △H=-393.5 kJ·mol-1
③2H2(g)+O2(g) =2H2O(l) △H=-571.6 kJ·mol-1
写出乙烷标准生成焓的热化学方程式:
(2)已知合成氨的反应为:N2+3H2
 2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
①图中代表反应在恒容绝热容器中进行的曲线是
②曲线a条件下该反应的平衡常数K=
③b容器中M点,v(正)
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为
(4)氨水是制备铜氨溶液的常用试剂,通过以下反应及数据来探究配制铜氨溶液的最佳途径。
已知:Cu(OH)2(s) ⇌Cu2++2OH- Ksp=2.2×10-20
Cu2++4NH3·H2O ⇌[Cu (NH3) 4]2+(深蓝色)+4H2O Kβ=7.24×1012
①请用数据说明利用该反应:Cu(OH)2(s) +4NH3·H2O ⇌[Cu (NH3) 4]2++4H2O+2OH-配制铜氨溶液是否可行:
②已知反应Cu(OH)2(S) +2NH3·H2O+2NH 4+⇌[Cu (NH3) 4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol·L-1的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为
(1)已知:

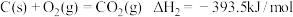

写出C与
 反应生成
反应生成 的热化学方程式
的热化学方程式(2)已知:
 。在
。在 恒容密闭容器中,投入
恒容密闭容器中,投入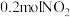 和
和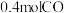 ,经过一段时间后达到平衡状态,测得
,经过一段时间后达到平衡状态,测得 的转化率为
的转化率为 。该温度下,反应的平衡常数为
。该温度下,反应的平衡常数为(3)原煤经热解、冷却得到的煤焦可用于
 的脱除。热解温度为
的脱除。热解温度为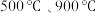 得到的煤焦分别用
得到的煤焦分别用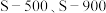 表示,相关信息如下表:
表示,相关信息如下表:| 煤焦 | 元素分析/% | 比表面积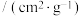 | |
| C | H | ||
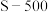 | 80.79 | 2.76 | 105.69 |
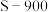 | 84.26 | 0.82 | 8.98 |
[已知:
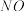 的脱除主要包含吸附和化学还原(
的脱除主要包含吸附和化学还原( )两个过程]
)两个过程]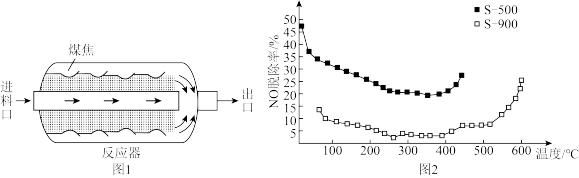
①已知煤焦表面存在的官能团有利于吸附NO,其数量与煤焦中氢碳质量比的值密切相关,比值小,表面官能团少。由图2可知,相同温度下,单位时间内
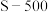 对NO的脱除率比
对NO的脱除率比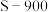 的高,可能原因是
的高,可能原因是②
 后,随着温度升高,单位时间内NO的脱除率增大的原因是
后,随着温度升高,单位时间内NO的脱除率增大的原因是(4)电解氧化吸收法:其原理如图3所示:
①从A口中出来的物质的是
②写出电解池阴极的电极反应式
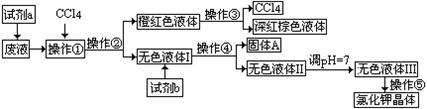
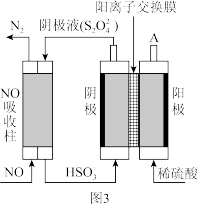
可供试剂a、b的选择试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2、KMnO4(H+)溶液、稀HNO3。
请根据以上流程,回答相关问题:
(1)试剂a应该选用
(2)操作①、②、③、④、⑤的名称是
A.萃取、过滤、分液、过滤、蒸发结晶 B.萃取、分液、蒸馏、过滤、蒸发结晶
C.分液、萃取、过滤、过滤、蒸发结晶 D.萃取、分液、分液、过滤、蒸发结晶
(3)欲除去无色液体I中的Ca2+、Mg2+、SO42-离子,选出b所代表的试剂,按滴加顺序依次是
(4)调节pH的作用是
(5)操作⑤中用到的瓷质仪器名称是
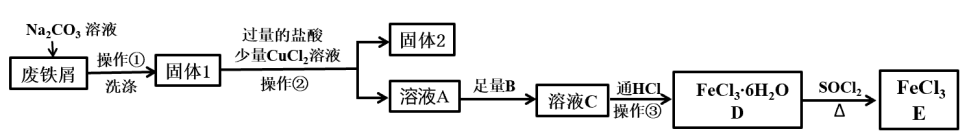
已知:SOCl2熔点-101℃,沸点76℃,易水解。
(1)Na2CO3溶液的作用为
(2)“操作②”前加入少量CuCl2溶液的目的为
(3)“固体2”的成分为
(4)为避免引入新的杂质,试剂B可以选用
a.KMnO4溶液 b.通氯气 c.H2O2溶液 d.稀硝酸
(5)操作③是蒸发结晶,加热的同时通入HCl(g)目的是
(6)D转化为E的化学方程式为

实验步骤如下:
①在上图所示的C中加入127g研细的单质I2和195g30%的KOH溶液,剧烈搅拌。
②I2完全反应后,打开弹簧夹向其中通入足量的H2S。
③将装置C中所得溶液用稀H2SO4酸化后,置于水浴上加热10min。
④在装置C的溶液中加入BaCO3,充分搅拌后,过滤、洗涤。
⑤将滤液用氢碘酸酸化,蒸发浓缩至表面出现结晶膜,________、________、洗涤、干燥。
⑥得产品145g。
回答下列问题:
(1)步骤①将碘研细的目的是
(2)装置A中发生反应的离子方程式为
装置B中的试剂是
(3)装置C中I2与KOH反应产物之一是KIO3,该反应的化学方程式为
(4)步骤④的目的是
(5)补充完整步骤⑤:



