1 . 某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液中﹣lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法正确的是
(已知:Ksp(ZnS)=3×10﹣25mol2/L2)
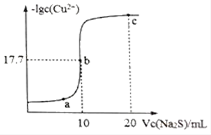
(已知:Ksp(ZnS)=3×10﹣25mol2/L2)

| A.a、b、c三点中,水的电离程度最大的为b点 |
| B.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
| C.该温度下Ksp(CuS)=10﹣35.4mol2/L2 |
| D.向100 mLZn2+、Cu2+浓度均为10-5mol/L的混合溶液中逐滴加入10-4mol/L的Na2S溶液,Zn2+先沉淀 |
您最近一年使用:0次
2019-02-02更新
|
371次组卷
|
2卷引用:【区级联考】安徽省宿州市埇桥区2018-2019学年高二(理)上学期期末考试化学试题
名校
解题方法
2 . 一定温度下,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),形成沉淀所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示。下列说法不正确的是
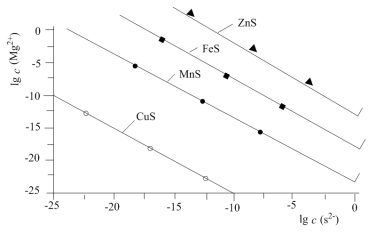

| A.若向沉淀剂Na2S溶液通入HCl气体至中性,存在关系: c(HS-)+2c(H2S)=c(Cl-) |
| B.该温度下,Ksp(MnS)大于1.0×10-35 |
| C.若将MnS、FeS的饱和溶液等体积混合,再加入足量的浓 Na2S溶液,发生的反应为MnS沉淀少于FeS |
| D.向l00mL浓度均为10-5mol·L-1Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol·L-1Na2S溶液,ZnS先沉淀 |
您最近一年使用:0次
2019-01-19更新
|
478次组卷
|
2卷引用:【全国百强校】四川省成都市第七中学2019届高三上学期11月份检测化学试题
3 . 某温度下,将打磨后的镁条放入盛有50 mL蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中的pH和浊度随时间的变化(如图所示,实线表示溶液pH随时间的变化)。下列有关描述正确的是
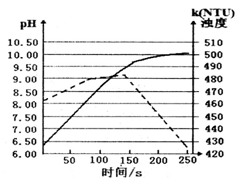

| A.该温度下Mg(OH)2的KSP的数量级约为10-10。 |
| B.该实验是在常温下进行的 |
| C.50 s时向溶液中滴入酚酞试液,溶液变红 |
| D.150 s后溶液浊度下降是因为生成的Mg(OH)2逐渐溶解 |
您最近一年使用:0次
2019-01-01更新
|
441次组卷
|
3卷引用:【校级联考】江西省吉安市五校2019届高三上学期联考化学试题
名校
解题方法
4 . t℃时,AgCl(s)与AgI(s)分别在溶液中达到沉淀溶解平衡,相关离子浓度的关系如下图所示。下列说法正确的是
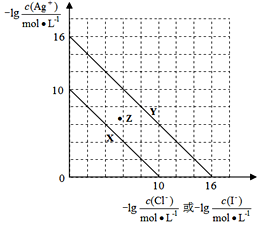

A.曲线Y表示 与 与 的变化关系 的变化关系 |
| B.t℃时,向Z点对应的溶液中加入蒸馏水,可使溶液变为曲线X对应的饱和溶液 |
C.t℃时,AgCl(s)+I-(aq) AgI(s)+Cl-(aq)的平衡常数K=1×106 AgI(s)+Cl-(aq)的平衡常数K=1×106 |
| D.t℃时,向浓度均为0.1mol/ L的KI与KCl混合溶液中加入AgNO3溶液,当Cl-刚好完全沉淀时,此时c(I-) = 1×10-5 mol/L |
您最近一年使用:0次
2018-12-12更新
|
689次组卷
|
2卷引用:【全国百强校】广东省深圳市高级中学2018-2019学年高二上学期期中考试化学试题
14-15高一上·浙江宁波·期末
解题方法
5 . 下列示意图与对应的反应情况正确的是


| A.含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2 |
| B.NaHSO4溶液中逐滴加入Ba(OH)2溶液 |
| C.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 |
| D.向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸 |
您最近一年使用:0次
6 . 某温度时,可用K2S沉淀Cu2+、Mn2+、Zn2+三种离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。下列说法正确的是
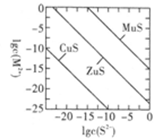

| A.三种离子对应的硫化物中Ksp(CuS)最小,约为1×10-20 |
| B.向MnS的悬浊液中加入少量水。沉淀溶解平衡向溶解的方向移动,c(S2-)增大 |
| C.可用MnS除去MnCl2溶液中混有的少量杂质ZnCl2 |
| D.向浓度均为1×10-5mol/L的Cu2+、 Zn2+、Mn2+混合溶液中逐滴加入1×10-4mol/的Na2S溶液,Mn2+最先沉淀 |
您最近一年使用:0次
2018-05-04更新
|
572次组卷
|
5卷引用:河北省邢台市2018届高三上学期第二次月考化学试题
河北省邢台市2018届高三上学期第二次月考化学试题【全国市级联考】新疆乌鲁木齐市2018届高三高考适应性训练理科综合化学试题人教版高二化学选修4 第三章 第四节 难溶电解质的溶解平衡练习题(已下线)专题8.4 难溶电解质的溶解平衡(讲)-《2020年高考一轮复习讲练测》2024届重庆市高三下学期二模考试化学试题
7 . 钨酸钙是非常重要的化学原料,主要用于生产钨铁、钨丝及钨合金等钨制品。在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙。发生反应:
Ⅰ.WO42ˉ(aq)+Ca(OH)2(s) CaWO4(s)+2OHˉ(aq) K1
CaWO4(s)+2OHˉ(aq) K1
已知:反应Ⅰ的平衡常数K1理论值如下表,请回答下列问题:
(1)判断反应Ⅰ的△S______ 0、△H______ 0(填“>”、“=”或“<”),在______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(2)氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,溶解度均随温度升高而减小。它们在水中存在如下沉淀溶解平衡:
Ⅱ.CaWO4(s) Ca2+(aq) + WO42ˉ(aq) K2
Ca2+(aq) + WO42ˉ(aq) K2
Ⅲ.Ca(OH)2(s) Ca2+(aq) + 2OHˉ(aq) K3
Ca2+(aq) + 2OHˉ(aq) K3
①根据反应Ⅰ~Ⅲ,可推导出K1、K2与K3之间的关系,则K1=______ (用K2、K3表示)。
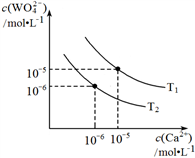
②根据反应Ⅱ,右图为不同温度下CaWO4的沉淀溶解平衡曲线。则T1____ T2(填“>”“=”或“<”)。T1时,向0.5 mol•Lˉ1钨酸钠的碱性溶液中,加入适量Ca(OH)2,反应达到平衡后WO42ˉ的转化率为60%,此时溶液中c(Ca2+)=_______ mol•Lˉ1。(假设反应前后体积不变)
(3)制取钨酸钙时,适时向反应混合液中添加适量的某种酸性物质,有利于提高WO42ˉ的转化率。反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3。
①在反应混合液中不直接通入CO2,其理由是_____________ ;
②用平衡移动原理解释添加酸性物质的理由______________ 。
Ⅰ.WO42ˉ(aq)+Ca(OH)2(s)
 CaWO4(s)+2OHˉ(aq) K1
CaWO4(s)+2OHˉ(aq) K1已知:反应Ⅰ的平衡常数K1理论值如下表,请回答下列问题:
温度/℃ | 25 | 50 | 90 | 100 |
K1 | 79.96 | 208.06 | 222.88 | 258.05 |
(1)判断反应Ⅰ的△S
(2)氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,溶解度均随温度升高而减小。它们在水中存在如下沉淀溶解平衡:
Ⅱ.CaWO4(s)
 Ca2+(aq) + WO42ˉ(aq) K2
Ca2+(aq) + WO42ˉ(aq) K2Ⅲ.Ca(OH)2(s)
 Ca2+(aq) + 2OHˉ(aq) K3
Ca2+(aq) + 2OHˉ(aq) K3①根据反应Ⅰ~Ⅲ,可推导出K1、K2与K3之间的关系,则K1=
②根据反应Ⅱ,右图为不同温度下CaWO4的沉淀溶解平衡曲线。则T1

(3)制取钨酸钙时,适时向反应混合液中添加适量的某种酸性物质,有利于提高WO42ˉ的转化率。反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3。
①在反应混合液中不直接通入CO2,其理由是
②用平衡移动原理解释添加酸性物质的理由
您最近一年使用:0次
8 . 明末宋应星的著书《天工开物》中记载了我国古代炼锌的方法,用炉甘石(主要成分是ZnCO3)和木炭混合加热分两步反应得到锌,写出其中氧化还原反应的化学方程式_____________ 。
现代工业上利用锌焙砂提炼金属锌的流程如下图所示(已知:①锌焙砂的主要成分是ZnO、ZnFe2O4,还含有少量FeO、CuO、NiO杂质;②金属活动性顺序:Zn>Ni>Cu),请回答下列问题:
(2)化合物ZnFe2O4中Fe的化合价为_________ ,酸浸时,ZnFe2O4发生反应的化学方程式为________ 。
(3)净化I操作分两步:首先用H2O2处理酸浸液,然后用物质A调节溶液的PH使Fe3+转化为Fe(OH)3沉淀过滤后除去。
①写出用H2O2处理酸浸液时发生反应的离子方程式______________ 。
②下图中的斜线是溶液中金属阳离子浓度(纵标)随pH值(横标)变化时的沉淀溶解平衡线,若加入物质A只使Fe3+沉淀完全,则物质A可能是_____________ (填出一种可能的化学式),调节后溶液的pH应控制在______________ 范围内(假设杂质离子浓度均不大于0.1mol· L-1 )。
③此流程中没有用调节pH来除去Cu2+的原因是_____________ 。
(4)净化II欲分离出Cu、Ni,加入的B物质的化学式_____________ 。
(5)本流程中可以循环利用的化合物有_______________ 。
现代工业上利用锌焙砂提炼金属锌的流程如下图所示(已知:①锌焙砂的主要成分是ZnO、ZnFe2O4,还含有少量FeO、CuO、NiO杂质;②金属活动性顺序:Zn>Ni>Cu),请回答下列问题:

(2)化合物ZnFe2O4中Fe的化合价为
(3)净化I操作分两步:首先用H2O2处理酸浸液,然后用物质A调节溶液的PH使Fe3+转化为Fe(OH)3沉淀过滤后除去。
①写出用H2O2处理酸浸液时发生反应的离子方程式
②下图中的斜线是溶液中金属阳离子浓度(纵标)随pH值(横标)变化时的沉淀溶解平衡线,若加入物质A只使Fe3+沉淀完全,则物质A可能是
③此流程中没有用调节pH来除去Cu2+的原因是

(4)净化II欲分离出Cu、Ni,加入的B物质的化学式
(5)本流程中可以循环利用的化合物有
您最近一年使用:0次
名校
解题方法
9 . 常温下,用Na2S沉淀 、
、 、
、 、
、 四种金属离子(M2+),所需
四种金属离子(M2+),所需 最低浓度的对数值
最低浓度的对数值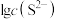 与
与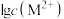 关系如下图所示,下列说法正确的是
关系如下图所示,下列说法正确的是

 、
、 、
、 、
、 四种金属离子(M2+),所需
四种金属离子(M2+),所需 最低浓度的对数值
最低浓度的对数值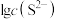 与
与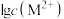 关系如下图所示,下列说法正确的是
关系如下图所示,下列说法正确的是
A.室温时,向ZnS悬浊液中加入ZnSO4固体,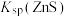 将随之减小 将随之减小 |
B.Na2S溶液中: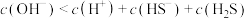 |
| C.为除去MnCl2溶液中混有的少量 CuCl2,可加入适量Na2S固体,充分搅拌后过滤 |
D.向100 mL浓度均为 的 的 、 、 混合溶液中逐滴加入 混合溶液中逐滴加入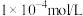 Na2S溶液, Na2S溶液, 先沉淀,证明 先沉淀,证明 |
您最近一年使用:0次
2017-02-17更新
|
585次组卷
|
2卷引用:2017届安徽省示范高中培优联盟高三冬季联赛化学试卷
10 . 已知:Fe(OH)3和Al(OH)3沉淀的生成与溶解的pH如下表。
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2溶液,形成沉淀的情况如下图所示。以下推断错误的是

| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | —— | —— |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2溶液,形成沉淀的情况如下图所示。以下推断错误的是

| A.AB段可能发生的反应:2Ba2++3OH-+2SO42-+Al3+=2BaSO4↓+Al(OH)3↓ |
| B.C点对应的沉淀:Fe(OH)3和BaSO4 |
| C.OA段可能发生的反应:3Ba2++6OH-+3SO42-+Al3++Fe3+=3BaSO4↓+Fe(OH)3↓+Al(OH)3↓ |
| D.据图计算原溶液中:c(Cl-)=c(SO42-) |
您最近一年使用:0次
2016-12-09更新
|
430次组卷
|
2卷引用:2017届江西省鹰潭一中高三上学期第二次月考化学试卷



