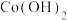名校
解题方法
1 . I.一种由菱镁矿(主要成分 、还含少量
、还含少量 及
及 )制备高纯氧化镁的工艺如下:
)制备高纯氧化镁的工艺如下:
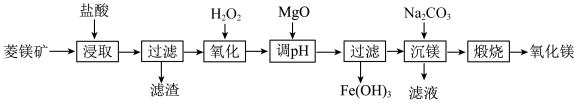
(1)“浸取”时加入盐酸需过量,原因是___________ 和___________ 。
(2)“调pH”时控制溶液的 。“调pH”时发生反应的离子方程式为
。“调pH”时发生反应的离子方程式为___________ 。
(3)“沉镁”时,溶液中有 和
和 析出。若此时溶液的
析出。若此时溶液的 ,则“沉镁”所得溶液中
,则“沉镁”所得溶液中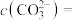
_______  。(已知
。(已知 ,
,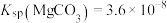 )
)
Ⅱ.
(4)一种以 溶液为原料制取氧化铁黄(FeOOH)的路线如下:
溶液为原料制取氧化铁黄(FeOOH)的路线如下:
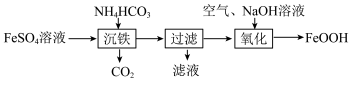
①“沉铁”时有 沉淀生成,该反应的化学方程式为
沉淀生成,该反应的化学方程式为___________ 。
②“氧化”反应的离子方程式为___________ 。
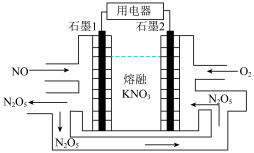
(5)一种以NO、 和熔融
和熔融 制成的燃料电池,其工作原理如图所示。该电池放电时的正极反应方程式为:
制成的燃料电池,其工作原理如图所示。该电池放电时的正极反应方程式为:___________ 。
 、还含少量
、还含少量 及
及 )制备高纯氧化镁的工艺如下:
)制备高纯氧化镁的工艺如下:
(1)“浸取”时加入盐酸需过量,原因是
(2)“调pH”时控制溶液的
 。“调pH”时发生反应的离子方程式为
。“调pH”时发生反应的离子方程式为(3)“沉镁”时,溶液中有
 和
和 析出。若此时溶液的
析出。若此时溶液的 ,则“沉镁”所得溶液中
,则“沉镁”所得溶液中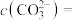
 。(已知
。(已知 ,
,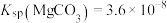 )
)Ⅱ.
(4)一种以
 溶液为原料制取氧化铁黄(FeOOH)的路线如下:
溶液为原料制取氧化铁黄(FeOOH)的路线如下:
①“沉铁”时有
 沉淀生成,该反应的化学方程式为
沉淀生成,该反应的化学方程式为②“氧化”反应的离子方程式为
(5)一种以NO、
 和熔融
和熔融 制成的燃料电池,其工作原理如图所示。该电池放电时的正极反应方程式为:
制成的燃料电池,其工作原理如图所示。该电池放电时的正极反应方程式为:
您最近一年使用:0次
名校
解题方法
2 . 以软锰矿(主要成分为 ,还含有少量的
,还含有少量的 、FeO、
、FeO、 和
和 )为原料制备马日夫盐[
)为原料制备马日夫盐[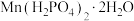 (磷酸二氢锰)]的主要流程如下:
(磷酸二氢锰)]的主要流程如下:
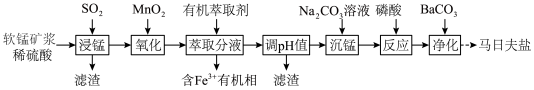
(1) “氧化”时反应的离子方程式
“氧化”时反应的离子方程式___________ 。
(2)如何检验“沉锰”已完成___________ 。
(3)加入 除
除 ,需控制温度在70~80℃,应采取的加热方式为
,需控制温度在70~80℃,应采取的加热方式为___________ 。
(4)铁离子的萃取率与接触时间和溶液的pH之间的关系如图1和图2所示,则应选择的接触时间为___________ ; ,铁离子的萃取率急剧下降的原因可能为
,铁离子的萃取率急剧下降的原因可能为___________ 。
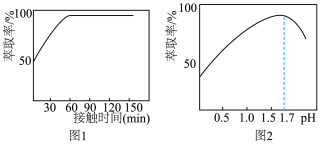
(5)结合图3的溶解度曲线,请补充完整由浸锰得到的溶液制备 的实验方案:边搅拌边先向溶液中滴加
的实验方案:边搅拌边先向溶液中滴加___________ ,再向滤液中加入___________ 粉末调节溶液的pH___________ ,过滤、洗涤,将滤液与洗涤液合并;控制温度在80~90℃蒸发结晶,趁热过滤,得到 ,用
,用___________ 的蒸馏水洗涤2~3次,放在___________ 中低温干燥。
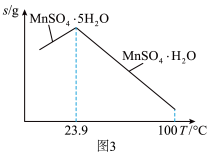
(实验中须使用的试剂:双氧水、 粉末、80~90℃的蒸馏水;除常用仪器外须使用的仪器:真空干燥箱)[已知该溶液中
粉末、80~90℃的蒸馏水;除常用仪器外须使用的仪器:真空干燥箱)[已知该溶液中 时
时 开始沉淀:
开始沉淀: 时
时 、
、 沉淀完全;
沉淀完全; 时
时 沉淀完全]。
沉淀完全]。
 ,还含有少量的
,还含有少量的 、FeO、
、FeO、 和
和 )为原料制备马日夫盐[
)为原料制备马日夫盐[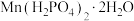 (磷酸二氢锰)]的主要流程如下:
(磷酸二氢锰)]的主要流程如下:
(1)
 “氧化”时反应的离子方程式
“氧化”时反应的离子方程式(2)如何检验“沉锰”已完成
(3)加入
 除
除 ,需控制温度在70~80℃,应采取的加热方式为
,需控制温度在70~80℃,应采取的加热方式为(4)铁离子的萃取率与接触时间和溶液的pH之间的关系如图1和图2所示,则应选择的接触时间为
 ,铁离子的萃取率急剧下降的原因可能为
,铁离子的萃取率急剧下降的原因可能为
(5)结合图3的溶解度曲线,请补充完整由浸锰得到的溶液制备
 的实验方案:边搅拌边先向溶液中滴加
的实验方案:边搅拌边先向溶液中滴加 ,用
,用
(实验中须使用的试剂:双氧水、
 粉末、80~90℃的蒸馏水;除常用仪器外须使用的仪器:真空干燥箱)[已知该溶液中
粉末、80~90℃的蒸馏水;除常用仪器外须使用的仪器:真空干燥箱)[已知该溶液中 时
时 开始沉淀:
开始沉淀: 时
时 、
、 沉淀完全;
沉淀完全; 时
时 沉淀完全]。
沉淀完全]。
您最近一年使用:0次
名校
3 . 硫铁矿(含 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
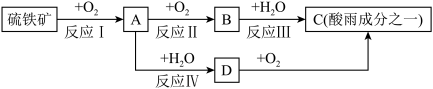
回答下列问题:
(1)硫铁矿 中硫元素化合价为
中硫元素化合价为_______ 。
(2)为了确定A中S元素的化合价,将其通入酸性高锰酸钾溶液中,发现溶液褪色,请写出该过程的离子方程式_______ 。
(3)已知反应Ⅲ是放热反应,该反应也是工业制硫酸的主要步骤之一,但在实际工业生产中常用98.3%的浓硫酸代替水来吸收B气体,其目的是_______ 。
(4)利用氧化亚铁硫杆菌 对硫铁矿进行催化脱硫的过程如下图所示:
对硫铁矿进行催化脱硫的过程如下图所示:
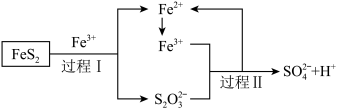
已知催化脱硫过程的总反应为: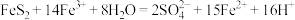
①则过程Ⅱ反应的离子方程式为_______ 。
②脱硫过程中产生的 在酸性溶液中会形成黄色沉淀和一种能使品红溶液褪色的气体,其原因可能是
在酸性溶液中会形成黄色沉淀和一种能使品红溶液褪色的气体,其原因可能是_______ (用离子方程式表示)。
③该催化过程中,要控制反应温度不能过高,原因是_______ 。
(5)接触法制硫酸生产中的关键工序是 的催化氧化:
的催化氧化: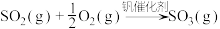
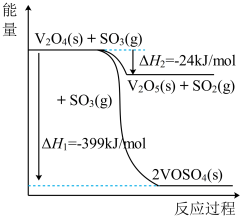
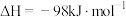 。钒催化剂参与反应的能量变化如图所示,
。钒催化剂参与反应的能量变化如图所示,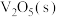 与
与 反应生成
反应生成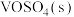 和
和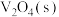 的热化学方程式为:
的热化学方程式为:_______ 。
 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
回答下列问题:
(1)硫铁矿
 中硫元素化合价为
中硫元素化合价为(2)为了确定A中S元素的化合价,将其通入酸性高锰酸钾溶液中,发现溶液褪色,请写出该过程的离子方程式
(3)已知反应Ⅲ是放热反应,该反应也是工业制硫酸的主要步骤之一,但在实际工业生产中常用98.3%的浓硫酸代替水来吸收B气体,其目的是
(4)利用氧化亚铁硫杆菌
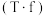 对硫铁矿进行催化脱硫的过程如下图所示:
对硫铁矿进行催化脱硫的过程如下图所示:
已知催化脱硫过程的总反应为:
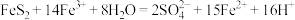
①则过程Ⅱ反应的离子方程式为
②脱硫过程中产生的
 在酸性溶液中会形成黄色沉淀和一种能使品红溶液褪色的气体,其原因可能是
在酸性溶液中会形成黄色沉淀和一种能使品红溶液褪色的气体,其原因可能是③该催化过程中,要控制反应温度不能过高,原因是
(5)接触法制硫酸生产中的关键工序是
 的催化氧化:
的催化氧化: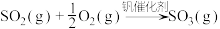
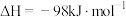 。钒催化剂参与反应的能量变化如图所示,
。钒催化剂参与反应的能量变化如图所示,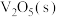 与
与 反应生成
反应生成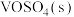 和
和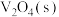 的热化学方程式为:
的热化学方程式为:
您最近一年使用:0次
名校
解题方法
4 . 我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。___________ (填化学式),俗称___________
(2)①~③所涉及的操作方法中,包含过滤的是___________ (填序号)。
(3)该生产过程中,可循环使用的物质是下列说法中,正确的是___________ (填字母)。
A. 可循环使用
可循环使用
B. 副产物可用作肥料
副产物可用作肥料
C.溶液B中一定不含 、
、
(4)已知 极易溶于水,
极易溶于水, 微溶于水,在饱和食盐水中,建议先通入气体
微溶于水,在饱和食盐水中,建议先通入气体___________ (填名称)。
(5)①利用下图比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为___________ 。
②若要除去碳酸钠溶液中的碳酸氢钠,发生反应的离子方程式为___________ 。
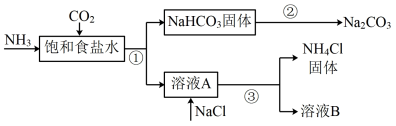
(2)①~③所涉及的操作方法中,包含过滤的是
(3)该生产过程中,可循环使用的物质是下列说法中,正确的是
A.
 可循环使用
可循环使用 B.
 副产物可用作肥料
副产物可用作肥料C.溶液B中一定不含
 、
、
(4)已知
 极易溶于水,
极易溶于水, 微溶于水,在饱和食盐水中,建议先通入气体
微溶于水,在饱和食盐水中,建议先通入气体(5)①利用下图比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为
②若要除去碳酸钠溶液中的碳酸氢钠,发生反应的离子方程式为
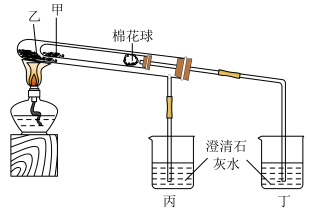
A. | B. | C.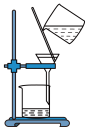 | D.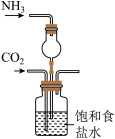 |
您最近一年使用:0次
解题方法
5 . 钴是生产多种合金和钴盐的重要原料,水钴矿主要成分为CoOOH,同时含有少量Fe、Al、Mn、Mg、Ca的氧化物及其他杂质。用水钴矿制取Co的工艺流程如图所示:
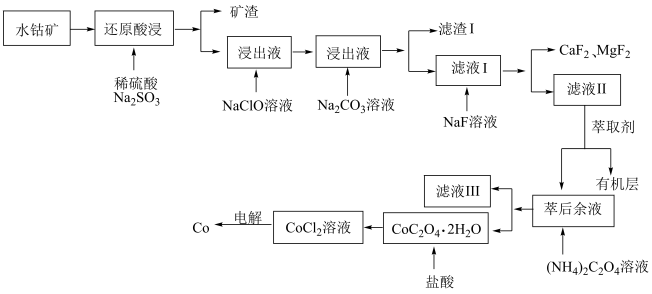
已知:①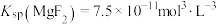 ;
;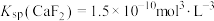
②部分阳离子以氢氧化物形成沉淀时,溶液的pH见下表。
请回答下列问题:
(1)CoOOH中Co的化合价为_____ , 溶液的作用是
溶液的作用是______ ,请写出“还原酸浸”中发生的主要氧化还原反应的化学方程式:______ 。
(2)浸出过程中加入 溶液调pH的范围是
溶液调pH的范围是______ ≤pH<______
(3)当加入过量NaF后,所得滤液Ⅱ中 与
与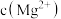 之比为
之比为______ 。
(4)萃取剂对金属离子的萃取率与pH的关系如图1所示,加萃取剂的目的是______ ,其使用的最佳pH范围是______ (填字母代号)。
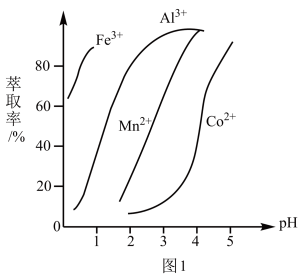
a.2.0~2.5 b.3.0~3.5 c.4.0~4.5
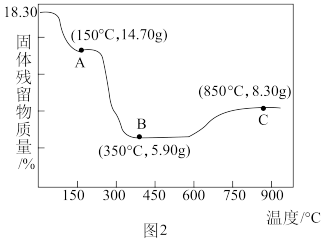
(5)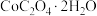 热分解质量变化过程如图2所示。其中600℃以前是隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物,C点所示产物的化学式是
热分解质量变化过程如图2所示。其中600℃以前是隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物,C点所示产物的化学式是______ 。

已知:①
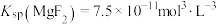 ;
;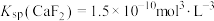
②部分阳离子以氢氧化物形成沉淀时,溶液的pH见下表。
沉淀物 |
|
|
|
|
|
开始沉淀时的pH | 7.0 | 2.7 | 7.6 | 7.7 | 4.0 |
沉淀完全时的pH | 9.6 | 3.7 | 9.2 | 9.8 | 5.2 |
(1)CoOOH中Co的化合价为
 溶液的作用是
溶液的作用是(2)浸出过程中加入
 溶液调pH的范围是
溶液调pH的范围是(3)当加入过量NaF后,所得滤液Ⅱ中
 与
与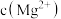 之比为
之比为(4)萃取剂对金属离子的萃取率与pH的关系如图1所示,加萃取剂的目的是

a.2.0~2.5 b.3.0~3.5 c.4.0~4.5
(5)
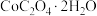 热分解质量变化过程如图2所示。其中600℃以前是隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物,C点所示产物的化学式是
热分解质量变化过程如图2所示。其中600℃以前是隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物,C点所示产物的化学式是
您最近一年使用:0次
2023-12-05更新
|
108次组卷
|
2卷引用:黑龙江省龙西北名校联合体2023-2024学年高三上学期期中考试化学试题
解题方法
6 . 氟化镁( )是用途广泛的无机化工原料。由菱镁矿(主要成分为
)是用途广泛的无机化工原料。由菱镁矿(主要成分为 ,含少量Ca、Si、Fe、Mn和Al等元素)制备氟化镁的流程如下图:
,含少量Ca、Si、Fe、Mn和Al等元素)制备氟化镁的流程如下图: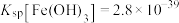 ,
,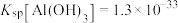 。回答下列问题:
。回答下列问题:
(1)“煅烧”时,菱镁矿主要成分发生反应的化学方程式是___________ 。
(2)“蒸氨”过程中“尾气”的主要成分是___________ (填化学式)。
(3) 溶液除“氧化除锰”外,还有
溶液除“氧化除锰”外,还有___________ 的作用。生产中,所需 用量远超理论值的原因是
用量远超理论值的原因是___________ 。
(4)“除铁铝”过程中,当 恰好沉淀完全时,溶液中
恰好沉淀完全时,溶液中
___________ (计算结果保留两位有效数字)。
(5)“除铁铝”时,用氨水调节溶液的pH,但pH不宜过高,原因是___________ 。
(6)“沉淀”时,发生反应的离子方程式是___________ 。
 )是用途广泛的无机化工原料。由菱镁矿(主要成分为
)是用途广泛的无机化工原料。由菱镁矿(主要成分为 ,含少量Ca、Si、Fe、Mn和Al等元素)制备氟化镁的流程如下图:
,含少量Ca、Si、Fe、Mn和Al等元素)制备氟化镁的流程如下图: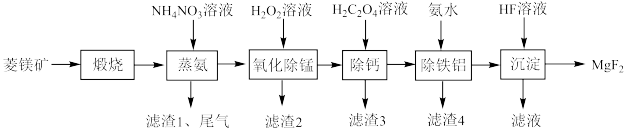
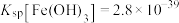 ,
,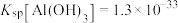 。回答下列问题:
。回答下列问题:(1)“煅烧”时,菱镁矿主要成分发生反应的化学方程式是
(2)“蒸氨”过程中“尾气”的主要成分是
(3)
 溶液除“氧化除锰”外,还有
溶液除“氧化除锰”外,还有 用量远超理论值的原因是
用量远超理论值的原因是(4)“除铁铝”过程中,当
 恰好沉淀完全时,溶液中
恰好沉淀完全时,溶液中
(5)“除铁铝”时,用氨水调节溶液的pH,但pH不宜过高,原因是
(6)“沉淀”时,发生反应的离子方程式是
您最近一年使用:0次
名校
解题方法
7 . 利用蛇纹石提镁后的中和渣(主要成分为 及
及 等杂质)提取高附加值的铁红
等杂质)提取高附加值的铁红 的一种工艺流程如下图所示。
的一种工艺流程如下图所示。
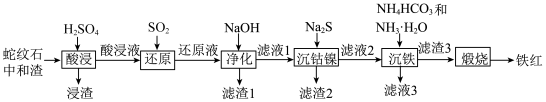
已知:(1)

(2)溶液中离子浓度 时可认为完全沉淀
时可认为完全沉淀
请回答下列问题:
(1)滤渣1的成分为_________ (填化学式),滤液2中主要的金属阳离子为_________ .
(2)还原过程中发生反应的离子方程式为_________ ,可用试剂_________ 检验还原是否完全。
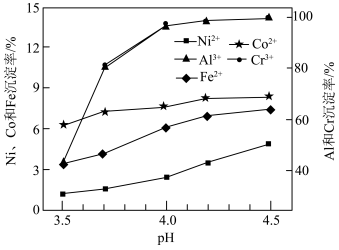
(3)欲制备高纯铁红,净化过程溶液中各离子的去除率与 的关系如下图,则应控制
的关系如下图,则应控制 为
为_________ .
(4)沉钴镍时,若溶液中 浓度均为
浓度均为 逐渐加入
逐渐加入 ,则先沉淀的离子为
,则先沉淀的离子为_________ ,计算说明两种离子能否彻底先后分离__________________ .
(5)煅烧过程中发生的化学方程式为__________________ .
 及
及 等杂质)提取高附加值的铁红
等杂质)提取高附加值的铁红 的一种工艺流程如下图所示。
的一种工艺流程如下图所示。
已知:(1)


(2)溶液中离子浓度
 时可认为完全沉淀
时可认为完全沉淀请回答下列问题:
(1)滤渣1的成分为
(2)还原过程中发生反应的离子方程式为
(3)欲制备高纯铁红,净化过程溶液中各离子的去除率与
 的关系如下图,则应控制
的关系如下图,则应控制 为
为
(4)沉钴镍时,若溶液中
 浓度均为
浓度均为 逐渐加入
逐渐加入 ,则先沉淀的离子为
,则先沉淀的离子为(5)煅烧过程中发生的化学方程式为
您最近一年使用:0次
解题方法
8 . 纳米 被广泛应用于光催化、精细陶瓷等领域。
被广泛应用于光催化、精细陶瓷等领域。
(1)用 水解法制备纳米
水解法制备纳米 的工艺流程如图所示(成功的控制水解速率是制备纳米
的工艺流程如图所示(成功的控制水解速率是制备纳米 的前提):
的前提):
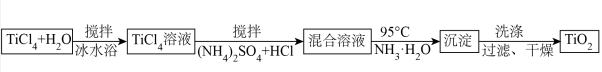
已知: 难溶于冷水,在热水中易水解;
难溶于冷水,在热水中易水解; 的水解按以下三步进行:
的水解按以下三步进行:
第Ⅰ步(水解):
第Ⅱ步(电离):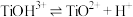
第Ⅲ步(水解):
①第Ⅰ步为快反应,对第Ⅱ、Ⅲ步反应的影响是_______ 。
②流程中加入硫酸铵的目的是_______ 。
③若取上述流程中“混合溶液”加水稀释,会产生少量偏钛酸( )沉淀,该反应的离子方程式为
)沉淀,该反应的离子方程式为_______ 。
(2)测定产品中 纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含
纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含 溶液。加入金属铝,将
溶液。加入金属铝,将 全部转化为
全部转化为 。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
 标准溶液滴定至终点,将
标准溶液滴定至终点,将 氧化为
氧化为 。重复操作2~3次,消耗标准溶液平均体积为20.00mL。
。重复操作2~3次,消耗标准溶液平均体积为20.00mL。
①金属铝还原 的离子方程式为
的离子方程式为_______ 。
②滴定时所用的指示剂为_______ (填编号)。
a.酚酞溶液 b.KSCN溶液 c. 溶液 d.淀粉溶液
溶液 d.淀粉溶液
③样品中 的纯度为
的纯度为_______ 。
(3)纳米 在室温下可有效催化降解空气中的甲醛。
在室温下可有效催化降解空气中的甲醛。 和甲醛都可在催化剂表面吸附,光照时,吸附的
和甲醛都可在催化剂表面吸附,光照时,吸附的 与
与 产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:
产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:_______ 。

 被广泛应用于光催化、精细陶瓷等领域。
被广泛应用于光催化、精细陶瓷等领域。(1)用
 水解法制备纳米
水解法制备纳米 的工艺流程如图所示(成功的控制水解速率是制备纳米
的工艺流程如图所示(成功的控制水解速率是制备纳米 的前提):
的前提):
已知:
 难溶于冷水,在热水中易水解;
难溶于冷水,在热水中易水解; 的水解按以下三步进行:
的水解按以下三步进行:第Ⅰ步(水解):

第Ⅱ步(电离):
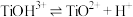
第Ⅲ步(水解):

①第Ⅰ步为快反应,对第Ⅱ、Ⅲ步反应的影响是
②流程中加入硫酸铵的目的是
③若取上述流程中“混合溶液”加水稀释,会产生少量偏钛酸(
 )沉淀,该反应的离子方程式为
)沉淀,该反应的离子方程式为(2)测定产品中
 纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含
纯度的方法是:准确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含 溶液。加入金属铝,将
溶液。加入金属铝,将 全部转化为
全部转化为 。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
。待过量金属铝完全溶解并冷却后,加入指示剂,用0.1000
 标准溶液滴定至终点,将
标准溶液滴定至终点,将 氧化为
氧化为 。重复操作2~3次,消耗标准溶液平均体积为20.00mL。
。重复操作2~3次,消耗标准溶液平均体积为20.00mL。①金属铝还原
 的离子方程式为
的离子方程式为②滴定时所用的指示剂为
a.酚酞溶液 b.KSCN溶液 c.
 溶液 d.淀粉溶液
溶液 d.淀粉溶液③样品中
 的纯度为
的纯度为(3)纳米
 在室温下可有效催化降解空气中的甲醛。
在室温下可有效催化降解空气中的甲醛。 和甲醛都可在催化剂表面吸附,光照时,吸附的
和甲醛都可在催化剂表面吸附,光照时,吸附的 与
与 产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:
产生HO·,从而降解甲醛。空气的湿度与甲醛降解率的关系如图所示,试解释甲醛降解率随空气湿度变化的原因:
您最近一年使用:0次
名校
解题方法
9 . 下面是用饱和NaCl溶液来制备一种重要的含氯消毒剂 的工艺流程图:
的工艺流程图:
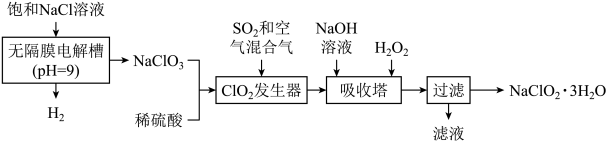
下列说法正确的是
 的工艺流程图:
的工艺流程图:
下列说法正确的是
A.发生器中通入空气的目的是氧化 |
B.吸收塔内发生反应的离子方程式: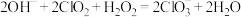 |
C.过滤后的滤液中大量存在: 、 、 、 、 、 、 、 、 |
D.电解槽中总的离子方程式: |
您最近一年使用:0次
名校
解题方法
10 . 我国重晶石(BaSO4含量为90%以上)资源丰富,某工厂以重晶石为原料,生产“电子陶瓷工业支柱”——钛酸钡(BaTiO3)的工艺流程如下:
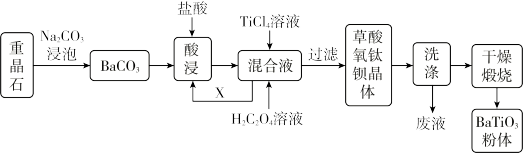
查阅资料可知:
①常温下: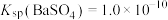 ,
,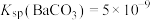 。
。
②草酸氧钛钡晶体的化学式为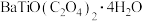 。
。
回答下列问题:
(1)为提高BaCO3的酸浸速率,可采取的措施为_____ (写出一条)。
(2)配制TiCl4溶液时通常将TiCl4固体溶于浓盐酸再加水稀释,其目的是_____ 。
(3)工业上用饱和Na2CO3溶液处理重晶石(假设杂质不与Na2CO3溶液作用),待达到平衡后,移走上层清液,重复多次操作,将BaSO4转化为易溶于酸的BaCO3,该过程用离子方程式可表示为_____ ,此反应的平衡常数K=_____ (填写计算结果)。若不考虑 的水解,则至少需要使用
的水解,则至少需要使用_____ mol·L-1的Na2CO3溶液浸泡BaSO4才能实现该转化过程。
(4)可循环使用的物质X是_____ (填化学式),设计实验方案验证草酸氧钛钡晶体是否洗涤干净:_____ 。
(5)在隔绝空气条件下,煅烧草酸氧钛钡晶体时有两种气体(水蒸气除外)生成,该反应的化学方程式为_____ 。

查阅资料可知:
①常温下:
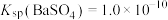 ,
,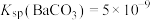 。
。②草酸氧钛钡晶体的化学式为
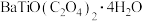 。
。回答下列问题:
(1)为提高BaCO3的酸浸速率,可采取的措施为
(2)配制TiCl4溶液时通常将TiCl4固体溶于浓盐酸再加水稀释,其目的是
(3)工业上用饱和Na2CO3溶液处理重晶石(假设杂质不与Na2CO3溶液作用),待达到平衡后,移走上层清液,重复多次操作,将BaSO4转化为易溶于酸的BaCO3,该过程用离子方程式可表示为
 的水解,则至少需要使用
的水解,则至少需要使用(4)可循环使用的物质X是
(5)在隔绝空气条件下,煅烧草酸氧钛钡晶体时有两种气体(水蒸气除外)生成,该反应的化学方程式为
您最近一年使用:0次
2023-12-02更新
|
158次组卷
|
2卷引用:广东省清远市名校2023-2024学年高二上学期期中调研联考化学试题