1 . 2021年9月28日,国务院新闻办公室发表《中国的全面小康》白皮书,宣布中国全面进入小康社会。化学学科正以独特学科价值为全面小康社会保驾护航。
I.屠呦呦制备青蒿素是高效的抗疟药。青蒿素为无色针状晶体,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差。已知:乙醚沸点为35℃,乙醚浸取法是从青蒿中提取青蒿素的方法。其主要工艺如图所示:
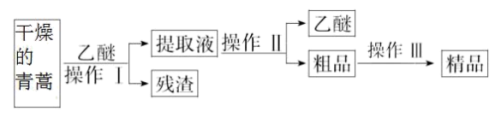
(1)乙醚浸取青蒿时,为增大青蒿素的浸出率,可采取的措施是___________ 。
(2)操作I需要的玻璃仪器主要有烧杯、玻璃棒、_____ ,操作II的名称是_______ 。
(3)操作III的主要过程可能是___________ (填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
II.我国正努力争取2060年前实现碳中和,用化学手段实现碳中和主要是对 进行捕获收集和资源化利用。
进行捕获收集和资源化利用。
(4)利用低浓度氨水吸收烟气中 生成
生成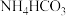 ,其离子方程式为
,其离子方程式为___________ 。
(5)下列说法有利于实现碳中和的是___________ 。
A.积极鼓励植树造林,降低空气中 含量
含量
B.研发利用二氧化碳合成淀粉的人工路线,实现 的资源化利用
的资源化利用
C.开发可燃冰(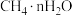 )作为新的替代能源
)作为新的替代能源
I.屠呦呦制备青蒿素是高效的抗疟药。青蒿素为无色针状晶体,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差。已知:乙醚沸点为35℃,乙醚浸取法是从青蒿中提取青蒿素的方法。其主要工艺如图所示:

(1)乙醚浸取青蒿时,为增大青蒿素的浸出率,可采取的措施是
(2)操作I需要的玻璃仪器主要有烧杯、玻璃棒、
(3)操作III的主要过程可能是
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
II.我国正努力争取2060年前实现碳中和,用化学手段实现碳中和主要是对
 进行捕获收集和资源化利用。
进行捕获收集和资源化利用。(4)利用低浓度氨水吸收烟气中
 生成
生成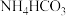 ,其离子方程式为
,其离子方程式为(5)下列说法有利于实现碳中和的是
A.积极鼓励植树造林,降低空气中
 含量
含量B.研发利用二氧化碳合成淀粉的人工路线,实现
 的资源化利用
的资源化利用C.开发可燃冰(
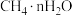 )作为新的替代能源
)作为新的替代能源
您最近一年使用:0次
名校
2 . 回答下列问题:
(1)实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4和NH4HCO3的NaCl,某学生设计了如图所示方案以提取得到纯净的NaCl溶液。(已知:NH4HCO3=NH3↑+CO2↑+H2O)。

a.150℃时,一定量的NH4HCO3完全分解后所得气体的摩尔质量为___________ (保留至小数点后一位)。
b.操作③所得的悬浊液与胶体的本质区别是___________ 。
c.进行操作②后,判断SO 是否已除尽操作是
是否已除尽操作是___________ 。
(2)高锰酸钾在酸性介质中的强氧化性广泛应用于分析化学中配平该反应方程式___________ 。
 KMnO4+
KMnO4+ H2C2O4+
H2C2O4+ H2SO4=
H2SO4= K2SO4+
K2SO4+ MnSO4+
MnSO4+ CO2↑+
CO2↑+ H2O(未配平)。
H2O(未配平)。
(3)用电弧法合成碳纳米管,常伴有大量杂质碳纳米颗粒,实验室中通常采用氧化气化法提纯,其化学反应方程式为:2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑。
①用双线桥法表示出电子的转移情况___________ 。
2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
②此反应的氧化产物和还原产物的物质的量之比为___________ 。
③要使10mL1.0mol•L-1K2Cr2O7溶液全部被还原,则至少要加入___________ mL2.0mol•L-1的H2SO4溶液,消耗C的质量为___________ g。
④若产生6.72CO2(标准状况下)气体,该反应转移的电子的物质的量为___________ 。
⑤H2SO4在上述反应中表现出来的性质是___________ (填字母)。
A.酸性 B.氧化性 C.还原性 D.吸水性
(1)实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4和NH4HCO3的NaCl,某学生设计了如图所示方案以提取得到纯净的NaCl溶液。(已知:NH4HCO3=NH3↑+CO2↑+H2O)。

a.150℃时,一定量的NH4HCO3完全分解后所得气体的摩尔质量为
b.操作③所得的悬浊液与胶体的本质区别是
c.进行操作②后,判断SO
 是否已除尽操作是
是否已除尽操作是(2)高锰酸钾在酸性介质中的强氧化性广泛应用于分析化学中配平该反应方程式
 KMnO4+
KMnO4+ H2C2O4+
H2C2O4+ H2SO4=
H2SO4= K2SO4+
K2SO4+ MnSO4+
MnSO4+ CO2↑+
CO2↑+ H2O(未配平)。
H2O(未配平)。(3)用电弧法合成碳纳米管,常伴有大量杂质碳纳米颗粒,实验室中通常采用氧化气化法提纯,其化学反应方程式为:2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑。
①用双线桥法表示出电子的转移情况
2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
②此反应的氧化产物和还原产物的物质的量之比为
③要使10mL1.0mol•L-1K2Cr2O7溶液全部被还原,则至少要加入
④若产生6.72CO2(标准状况下)气体,该反应转移的电子的物质的量为
⑤H2SO4在上述反应中表现出来的性质是
A.酸性 B.氧化性 C.还原性 D.吸水性
您最近一年使用:0次



