名校
解题方法
1 . Al与NaOH的水溶液能反应,而镁不反应。然而一位同学将镁条放入饱和碳酸氢钠溶液时,却观察到反应迅速发生,且有大量气体放出。查阅资料显示:①镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物;②Mg与沸水能明显发生反应。为探究反应原理,同学们设计了如下实验方案并验证产物。
【实验I】:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
(1)提出假设
该同学对反应中产生的白色不溶物作出如下猜测:
猜测1:可能是_______ 。
猜测2:可能是 。
。
猜测3:可能是碱式碳酸镁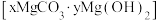 。
。
(2)设计定性实验确定产物并验证猜测:
(3)设计定量实验确定实验I的产物:称取实验I中所得干燥、纯净的白色不溶物31.0g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验前后装置A增重1.8g,装置B增重13.2g,试确定白色不溶物的化学式_______ 。
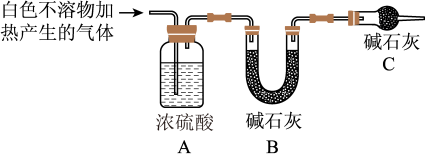
(4)根据资料显示以及实验现象,有同学认为,上述反应可能就是镁分别与水、与碳酸氢钠两个直接反应的共同结果。请你分别写出这两个可能发生的化学反应的化学方程式:_______ ,_______ 。
【实验I】:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
(1)提出假设
该同学对反应中产生的白色不溶物作出如下猜测:
猜测1:可能是
猜测2:可能是
 。
。猜测3:可能是碱式碳酸镁
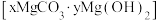 。
。(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 预期现象和结论 |
| 【实验II】 | 将实验I中收集的气体点燃 | 现象及结论 |
| 【实验III】 | 取实验I中的白色不溶物,洗涤,加入足量 |  |
| 【实验IV】 | 取实验I中的滤液,向其中加入BaCl2稀溶液 | 产生白色沉淀;溶液中存在 |

(4)根据资料显示以及实验现象,有同学认为,上述反应可能就是镁分别与水、与碳酸氢钠两个直接反应的共同结果。请你分别写出这两个可能发生的化学反应的化学方程式:
您最近一年使用:0次
2023-01-12更新
|
367次组卷
|
2卷引用:重庆市南开中学2022-2023学年高一上期期末考试化学试题
名校
解题方法
2 . 化学在医学上起到至关重要的作用。如:小苏打、氢氧化铝等可治疗胃酸(主要成分为稀盐酸)过多;硫酸亚铁可补铁、防治贫血;三价铬用于加强胰岛素的作用。试回答下列问题:
(1)写出小苏打与胃酸作用的离子方程式:_______ ,但该药剂缺点是易导致胃胀气,胃溃疡患者不能使用,而氢氧化铝很好的解决了这个问题,它在中和胃酸的同时,保护溃疡面,写出氢氧化铝与胃酸作用的化学方程式为_______ 。
(2)利用提供试剂设计实验证明补铁剂中铁元素都以+2存在(可选试剂:硫氰化钾、过氧化氢):_______ (填写实验操作、现象和结论)。
(3)三价铬是人体必需的微量元素,六价铬则严重危害人体健康,铬元素化合价循环示意图如下【已知: 可溶于水;
可溶于水; 难溶于水】:
难溶于水】:
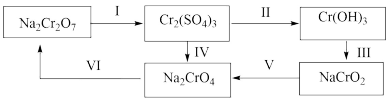
①步骤I所用的试剂是硫酸酸化的 ,请写出该反应的离子方程式;
,请写出该反应的离子方程式;_______
②现有含 和
和 的溶液,逐滴滴加NaOH溶液至过量,由上图信息可知,铁元素、铬元素的存在形态分别是
的溶液,逐滴滴加NaOH溶液至过量,由上图信息可知,铁元素、铬元素的存在形态分别是_______ 、_______ ;
③向50mL0.03mol/L的 溶液中,加入50mL0.2mol/L的NaOH溶液,写出相应离子反应方程式
溶液中,加入50mL0.2mol/L的NaOH溶液,写出相应离子反应方程式_______ 。
(1)写出小苏打与胃酸作用的离子方程式:
(2)利用提供试剂设计实验证明补铁剂中铁元素都以+2存在(可选试剂:硫氰化钾、过氧化氢):
(3)三价铬是人体必需的微量元素,六价铬则严重危害人体健康,铬元素化合价循环示意图如下【已知:
 可溶于水;
可溶于水; 难溶于水】:
难溶于水】:
①步骤I所用的试剂是硫酸酸化的
 ,请写出该反应的离子方程式;
,请写出该反应的离子方程式;②现有含
 和
和 的溶液,逐滴滴加NaOH溶液至过量,由上图信息可知,铁元素、铬元素的存在形态分别是
的溶液,逐滴滴加NaOH溶液至过量,由上图信息可知,铁元素、铬元素的存在形态分别是③向50mL0.03mol/L的
 溶液中,加入50mL0.2mol/L的NaOH溶液,写出相应离子反应方程式
溶液中,加入50mL0.2mol/L的NaOH溶液,写出相应离子反应方程式
您最近一年使用:0次
2023-01-12更新
|
426次组卷
|
2卷引用:重庆市南开中学2022-2023学年高一上期期末考试化学试题
名校
解题方法
3 . 某工厂的工业废水中含有大量的 和较多的
和较多的 。为减少污染并变废为宝,工厂计划从该废水中回收金属铜,并制备
。为减少污染并变废为宝,工厂计划从该废水中回收金属铜,并制备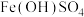 ,流程如下:
,流程如下:
 和较多的
和较多的 。为减少污染并变废为宝,工厂计划从该废水中回收金属铜,并制备
。为减少污染并变废为宝,工厂计划从该废水中回收金属铜,并制备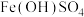 ,流程如下:
,流程如下: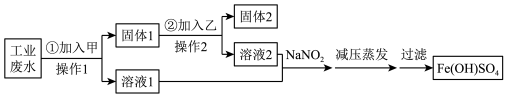
A.甲为铁粉,乙为 溶液 溶液 |
| B.操作1和操作2均用到漏斗、烧杯和玻璃棒,且固体2为铜 |
C.往溶液1与溶液2中加入 反应生成NO,欲制备1.5mol 反应生成NO,欲制备1.5mol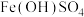 ,理论上至少需要2mol ,理论上至少需要2mol |
D.为检验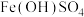 中是否含有 中是否含有 ,加入盐酸溶解,再加入过量NaOH溶液,观察沉淀颜色变化 ,加入盐酸溶解,再加入过量NaOH溶液,观察沉淀颜色变化 |
您最近一年使用:0次
2023-01-12更新
|
418次组卷
|
4卷引用:重庆市南开中学2022-2023学年高一上期期末考试化学试题
10-11高三·江西·阶段练习
名校
解题方法
4 . 两种硫酸盐按一定比例混合后共熔,可制得化合物X,且X溶于水能电离出K+、Cr3+、SO ,若将2.83gX中的Cr3+全部氧化为Cr2O
,若将2.83gX中的Cr3+全部氧化为Cr2O 后,溶液中的Cr2O
后,溶液中的Cr2O 可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为Cr2O
可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为Cr2O +6I-+14H+=2Cr3++3I2+7H2O。若向溶有2.83gX的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀。由此可推断出X的化学式为
+6I-+14H+=2Cr3++3I2+7H2O。若向溶有2.83gX的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀。由此可推断出X的化学式为
 ,若将2.83gX中的Cr3+全部氧化为Cr2O
,若将2.83gX中的Cr3+全部氧化为Cr2O 后,溶液中的Cr2O
后,溶液中的Cr2O 可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为Cr2O
可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为Cr2O +6I-+14H+=2Cr3++3I2+7H2O。若向溶有2.83gX的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀。由此可推断出X的化学式为
+6I-+14H+=2Cr3++3I2+7H2O。若向溶有2.83gX的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀。由此可推断出X的化学式为| A.K2SO4•2Cr2(SO4)3 | B.K2SO4•Cr2(SO4)3 |
| C.2K2SO4•Cr2(SO4)3 | D.K2SO4• Cr2(SO4)3 Cr2(SO4)3 |
您最近一年使用:0次
2022-11-21更新
|
286次组卷
|
11卷引用:重庆市南开中学2022-2023学年高一上期期末考试化学试题
重庆市南开中学2022-2023学年高一上期期末考试化学试题(已下线)2012届江西省白鹭洲中学高三第一次月考化学试卷(已下线)2012届安徽省宿州市高三第一次教学质量检测化学试卷(已下线)2015届江西省奉新县第一中学高三上学期第一次月考化学试卷甘肃省天水一中2017-2018学年高一下学期入学考试化学试题辽宁省六校2021届高三上学期期中联考化学试题广东省中山纪念中学2021届高三上学期第一次月考化学试题(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)宁夏石嘴山市第三中学2021-2022学年高三上学期期中考试化学(理)试题豫中名校2022-2023学年高一上学期期中考试化学试题
5 . 现有如下反应: (提示:BrF3中F为
(提示:BrF3中F为 价),下列判断错误的是
价),下列判断错误的是
 (提示:BrF3中F为
(提示:BrF3中F为 价),下列判断错误的是
价),下列判断错误的是| A.BrF3既是氧化剂,又是还原剂 |
| B.被氧化的原子数与被还原的原子数之比为3∶2 |
| C.每当消耗3molBrF3,就有5molH2O被还原 |
| D.若反应转移3mol电子,则生成标准状况下11.2LO2 |
您最近一年使用:0次
名校
解题方法
6 . 大多数离子液体含有体积很大的阴、阳离子(如图所示)。其中X、Y、Z为原子序数依次增大的短周期非金属元素,X、Z同主族。下列说法正确的是
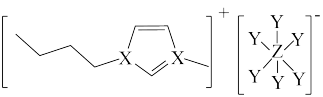

| A.原子半径:Z>X>Y | B.气态氢化物的稳定性:Z>X>Y |
| C.Z的氯化物的分子式一定为ZCl3 | D.此阴离子中Y、Z均满足8电子稳定结构 |
您最近一年使用:0次
2022-07-10更新
|
1346次组卷
|
7卷引用:重庆市第一中学2022-2023学年高二上学期期末考试化学试题
名校
7 . 在半导体的发展史中金属锗(Ge)是第一个被广泛使用的半导体材料,它在硅的下一周期,且与硅同主族。下列叙述不正确 的是
| A.锗位于金属区与非金属区的交界处 | B.锗的最高价含氧酸是强酸 |
| C.锗的单质具有半导体的性能 | D.热稳定性: |
您最近一年使用:0次
2022-01-24更新
|
463次组卷
|
4卷引用: 重庆市第一中学校2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . 固体粉末可能由 中的几种等物质的量混合而成,进行如下实验:
中的几种等物质的量混合而成,进行如下实验:
①取 固体溶于足量水中,得到澄清透明溶液,将溶液分为三等份。
固体溶于足量水中,得到澄清透明溶液,将溶液分为三等份。
②在第一份溶液中滴加足量稀盐酸无明显现象,再滴加足量 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 固体。
固体。
③在第二份溶液中滴加 溶液无明显现象,继续滴加双氧水,溶液显血红色。
溶液无明显现象,继续滴加双氧水,溶液显血红色。
④在第三份溶液中滴加足量 溶液,过滤、洗涤、灼烧,得到固体
溶液,过滤、洗涤、灼烧,得到固体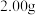 。
。
下列说法正确的是
 中的几种等物质的量混合而成,进行如下实验:
中的几种等物质的量混合而成,进行如下实验:①取
 固体溶于足量水中,得到澄清透明溶液,将溶液分为三等份。
固体溶于足量水中,得到澄清透明溶液,将溶液分为三等份。②在第一份溶液中滴加足量稀盐酸无明显现象,再滴加足量
 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 固体。
固体。③在第二份溶液中滴加
 溶液无明显现象,继续滴加双氧水,溶液显血红色。
溶液无明显现象,继续滴加双氧水,溶液显血红色。④在第三份溶液中滴加足量
 溶液,过滤、洗涤、灼烧,得到固体
溶液,过滤、洗涤、灼烧,得到固体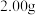 。
。下列说法正确的是
A.固体粉末中肯定没有 |
B.根据④中的沉淀颜色能判断固体粉末中是否含有 |
C.固体粉末中肯定含有 |
D.上述实验无法确定固体粉末是否含有 ,需进一步通过焰色试验确定 ,需进一步通过焰色试验确定 |
您最近一年使用:0次
2022-01-22更新
|
1114次组卷
|
5卷引用: 重庆市第一中学校2022-2023学年高一上学期期末考试化学试题
13-14高三·宁夏银川·阶段练习
名校
解题方法
9 . 足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和二氧化氮、一氧化氮的混合气体2.24L(标准状况),这些气体与一定体积(标准状况)氧气混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol·L-1氢氧化钠溶液至铜离子恰好完全沉淀,则消耗氢氧化钠溶液的体积是50mL,下列说法正确的是
| A.混合气体中含二氧化氮1.12L |
| B.消耗氧气的体积为1.68L |
| C.此反应过程中转移的电子为0.3mol |
| D.参加反应的硝酸是0.4mol |
您最近一年使用:0次
2021-08-25更新
|
797次组卷
|
30卷引用:重庆市第七中学校2021-2022学年高一下学期3月月考化学试题
重庆市第七中学校2021-2022学年高一下学期3月月考化学试题(已下线)2015届宁夏银川一中高三第四次月考化学试卷2014-2015吉林省松原市扶余县一中高一上学期期末化学试卷2015届山东省滕州市三中上学期高三第四次月考理综化学试卷2016届河南省扶沟县高级中学高三上学期开学考试化学试卷2016届河南省三门峡市陕州中学高三上学期第一次精英对抗赛化学试卷2016届重庆市万州第二高级中学高三上学期期中测试理综化学试卷2015-2016学年河北省冀州中学高一下开学考试化学试卷2016届河南省信阳市鸡公山风景区学校高三下2月月考化学试卷2015-2016学年安徽省六安一中高一下周末作业二化学试卷2015-2016学年安徽师大附中高一下学期期中考查化学试卷2015-2016学年山东省淄博六中高一下学科竞赛化学试卷2017届广西桂林市第十八中学高三上第二次月考化学试卷2018届高三一轮复习化学:考点21-铜及其化合物性质探究(已下线)《考前20天终极攻略》-5月26日 元素及其化合物福建省三明市第一中学2018-2019学年高二上学期开学考化学试题云南省新平县一中2018-2019学年高一上学期12月月考化学试题贵州省黔南布依族苗族自治州龙里中学2019-2020学年高一上学期期末考试化学试题辽宁省大连市一〇三中学2019-2020学年高一下学期期中考试化学试题河南省漯河市临颍县南街高级中学2020届高三阶段性测试化学试题安徽省芜湖市2021届高三第二次月考化学试题江西省高安中学2020-2021学年高一上学期期末考试化学试题四川省邻水实验学校2020-2021学年高一下学期第一次月考化学试题福建省福州第三中学2020-2021学年高一下学期期中考化学试题(已下线)专题02 氮及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)(已下线)专题13 氮及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练 浙江省诸暨市第二高级中学2020-2021学年高二下学期期中考试化学试题内蒙古自治区包钢第一中学2021-2022学年高三上学期10月月考化学试题云南省普洱市镇沅彝族哈尼族拉祜族自治县第一中学2021-2022学年高一下学期4月份考试化学试题湖南省怀化市沅陵县第一中学2021-2022学年高一下学期第一次月考化学试题
名校
10 . 钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,如图为钠投入液氨中的溶剂化图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是
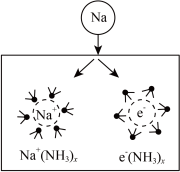

| A.钠的密度比液氨大 |
| B.溶液的导电性增强 |
| C.钠和液氨可发生以下反应:2NH3+2Na=2NaNH2+H2↑ |
| D.0.1mol钠投入液氨生成0.01molH2时,Na共失去0.02mol电子 |
您最近一年使用:0次
2021-05-07更新
|
1591次组卷
|
15卷引用:重庆市第一中学校 2021-2022学年高二上学期入学摸底考试化学试题
重庆市第一中学校 2021-2022学年高二上学期入学摸底考试化学试题山东省临沂市部分县区2020-2021学年高一下学期期中考试化学试题广东省广州市广州大学附属中学2020-2021学年高一下学期4月月考试题(已下线)课时14 钠及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省实验中学2021-2022高三上学期第三次月考(开学考)化学试题天津市耀华中学2021-2022学年高三上学期第一次月考化学试题浙江省湖州市三贤联盟2021-2022学年高一上学期期中考试化学试题吉林省吉林市普通中学2022-2023学年高三第一次调研测试化学试题吉林省吉林市普通中学2022-2023学年高三上学期10月调研化学试题天津市耀华中学2022-2023学年高一上学期期中考试化学试题吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题河南省许昌市禹州市高级中学2023-2024学年高三上学期9月月考化学试题福建省莆田第一中学2023-2024学年高一上学期期末考试化学试题



