名校
解题方法
1 . 利用金属矿渣(含有FeS2、SiO2及Cu2O)制备(NH4)2Fe(SO4)2晶体的流程如下。

已知:SiO2不与稀硫酸反应;Cu2O+H2SO4=CuSO4+Cu+H2O
下列说法不正确的是

已知:SiO2不与稀硫酸反应;Cu2O+H2SO4=CuSO4+Cu+H2O
下列说法不正确的是
A.“煅烧”过程中FeS2转化为Fe2O3的反应为4FeS2+11O2 2Fe2O3+8SO2 2Fe2O3+8SO2 |
| B.若“酸浸”后溶液中无Fe2+,说明“煅烧”过程中Cu2O全部转化为CuO |
C.“还原”得到溶液中的离子主要有:Fe2+、 |
| D.“过滤”后滤渣的成分为SiO2及铁屑 |
您最近一年使用:0次
2024-04-06更新
|
130次组卷
|
3卷引用:江苏省黄埭中学2022-2023学年高一下学期期中调研测试化学试题
解题方法
2 . 下列有关物质的性质和用途具有对应关系的是
| A.NaClO能使蛋白质变性,可用于环境消毒 |
| B.75%的乙醇具有强氧化性,可用于杀药消毒 |
| C.NaHCO3水解显碱性,可用于腹泻患者的治疗 |
| D.O2具有强氧化性,可用于肺炎重症患者的急救 |
您最近一年使用:0次
名校
解题方法
3 . 如图是卤素单质(F2、Cl2、Br2、I2)的沸点与相对分子质量的关系图,下列说法不正确 的是
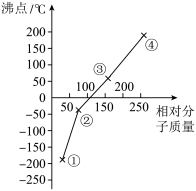

| A.单质①是最活泼的非金属单质 |
| B.单质②能使石蕊试液先变红后褪色 |
| C.单质③常温下是液态 |
| D.单质④的氢化物在卤素氢化物中热稳定性最强 |
您最近一年使用:0次
2024-04-05更新
|
75次组卷
|
2卷引用:陕西省宝鸡市金台区2023-2024学年高一上学期期末检测化学试题
名校
4 . 下列说法不正确的是
A. 的摩尔质量是 的摩尔质量是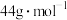 | B. 的物质的量一定为 的物质的量一定为 |
C.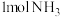 中含有的分子数约为 中含有的分子数约为 | D.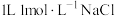 溶液中含有 溶液中含有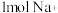 |
您最近一年使用:0次
2024-04-04更新
|
105次组卷
|
2卷引用:2023年北京市第二次普通高中学业水平测试高一下学期化学试题
5 . 回答下列问题
(1)6.02×1023个Fe的物质的量为___________ ,3.01×1023个O2所含氧分子的物质的量为___________ ,2mol H2O中含有水分子___________ 个(用NA表达)。
(2)0.5mol H2O的质量为___________ ,其中含有水分子___________ 个(用NA表达),H原子的物质的量为___________ 。
(3)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是___________ ,在相同温度和相同压强条件下,体积最大的是___________ 。
(4)1molCO2与2molSO3的分子数比是___________ ,原子数比是___________ 。
(1)6.02×1023个Fe的物质的量为
(2)0.5mol H2O的质量为
(3)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是
(4)1molCO2与2molSO3的分子数比是
您最近一年使用:0次
名校
6 . 研究发现,镭能蜕变为 ,故将
,故将 称为镭射气;钍能蜕变为
称为镭射气;钍能蜕变为 ,故将
,故将 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为 ,故将
,故将 称为锕射气。下列有关说法正确的是
称为锕射气。下列有关说法正确的是
 ,故将
,故将 称为镭射气;钍能蜕变为
称为镭射气;钍能蜕变为 ,故将
,故将 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为 ,故将
,故将 称为锕射气。下列有关说法正确的是
称为锕射气。下列有关说法正确的是| A.Rn的中子数为136 | B.Rn位于元素周期表第七周期 |
C. 、 、 、 、 互为同位素 互为同位素 | D. 、 、 、 、 属于同种原子 属于同种原子 |
您最近一年使用:0次
名校
解题方法
7 . 已知下列物质:
①He;②NH4Cl;③AlCl3;④NaOH;⑤Cl2;⑥H2O2;⑦H2S;⑧CaC2;⑨K2S;⑩NaHSO4。
回答下列问题:
(1)共价化合物有___________ (填序号,下同),既含离子键又含共价键的有___________ 。
(2)含有非极性共价键的有___________ 。
(3)没有化学键的有___________ 。
(4)所有组成元素均满足8电子稳定结构的有___________ 。
(5)加热②使其分解,破坏的化学键是___________ 。
(6)用电子式表示⑨的形成过程___________ 。
①He;②NH4Cl;③AlCl3;④NaOH;⑤Cl2;⑥H2O2;⑦H2S;⑧CaC2;⑨K2S;⑩NaHSO4。
回答下列问题:
(1)共价化合物有
(2)含有非极性共价键的有
(3)没有化学键的有
(4)所有组成元素均满足8电子稳定结构的有
(5)加热②使其分解,破坏的化学键是
(6)用电子式表示⑨的形成过程
您最近一年使用:0次
8 . 已知NA为阿伏加德罗常数的值,下列说法正确的是
| A.2.0 g H218O与D2O的混合物中所含中子数为NA |
B.235 g核素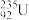 发生裂变反应: 发生裂变反应: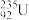 + + 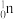 → → 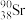 + + 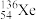 + 10 + 10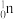 ,净产生的中子( ,净产生的中子(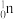 )数为10NA )数为10NA |
| C.标况下,4.48 L CO2分子中含有的共用电子对数为0.4NA |
| D.1.4 g锂单质在足量的氧气中燃烧,生成的产物中含有的非极性键数目为0.1NA |
您最近一年使用:0次
名校
9 . 下列说法正确的有
①质量数为133、中子数为78的铯原子符号: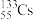
②S2-的结构示意图: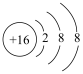
③用电子式表示HCl的形成过程:
④CaCl2的电子式:
⑤次氯酸分子的结构式:H-O-Cl
⑥熔融NaHSO4破坏离子键和共价键
⑦PCl3和CO2均满足8电子稳定结构
①质量数为133、中子数为78的铯原子符号:
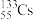
②S2-的结构示意图:

③用电子式表示HCl的形成过程:

④CaCl2的电子式:

⑤次氯酸分子的结构式:H-O-Cl
⑥熔融NaHSO4破坏离子键和共价键
⑦PCl3和CO2均满足8电子稳定结构
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近一年使用:0次
名校
解题方法
10 . “化学——人类进步的关键”。下列化学知识的说法中正确的有
①任何原子核内均含质子和中子
②门捷列夫根据质子数制作出第一张元素周期表
③科学家在周期表中金属与非金属分界线处找到了半导体材料
④原子序数为22的元素位于元素周期表的第4周期ⅡB族
⑤带相反电荷离子之间的静电吸引叫做离子键
⑥同主族两种元素原子的核外电子数的差值可能为36
⑦同一周期的甲、乙两种元素,甲位于第ⅡA族,序数为x,乙位于第ⅢA族,则乙的序数可能为x+10
⑧砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀酸
⑨Na2O和Na2O2中阴阳离子个数比都是1:2
⑩卤素单质的熔点从F2到I2逐渐升高,碱金属单质的熔点从Li到Cs也逐渐升高
①任何原子核内均含质子和中子
②门捷列夫根据质子数制作出第一张元素周期表
③科学家在周期表中金属与非金属分界线处找到了半导体材料
④原子序数为22的元素位于元素周期表的第4周期ⅡB族
⑤带相反电荷离子之间的静电吸引叫做离子键
⑥同主族两种元素原子的核外电子数的差值可能为36
⑦同一周期的甲、乙两种元素,甲位于第ⅡA族,序数为x,乙位于第ⅢA族,则乙的序数可能为x+10
⑧砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀酸
⑨Na2O和Na2O2中阴阳离子个数比都是1:2
⑩卤素单质的熔点从F2到I2逐渐升高,碱金属单质的熔点从Li到Cs也逐渐升高
| A.③⑥⑧⑨ | B.①③④⑦⑨ | C.②⑤⑥⑨ | D.③⑥⑧⑩ |
您最近一年使用:0次



